- Преподавателю
- Начальные классы
- Получение источника электричества в домашних условиях»
Получение источника электричества в домашних условиях»
| Раздел | Начальные классы |
| Класс | - |
| Тип | Конспекты |
| Автор | Савкина Е.М. |
| Дата | 07.03.2015 |
| Формат | docx |
| Изображения | Есть |
МБОУ «Троицкая средняя общеобразовательная школа №2»
Научно - практическая конференция
«Я познаю мир».
Научно-исследовательская работа по теме:
«Получение источника электричества в домашних условиях»
Работа ученика 3А класса
МБОУ ТСОШ №2
Сапрыгина Артема
Руководитель: Савкина Е.М.
с. Троицкое
2015г.
Содержание
- Введение.....................................................................................3 стр.
- Обоснование выбора темы.........................................................4 стр.
- Актуальность …………………………………………………………………………………4 стр.
- Гипотеза………………………………………………………………………………………….4 стр.
- Цель…………………………………………………………………………………………………4 стр.
- Предмет…………………………………………………………………………………………..4 стр.
- Объект………………………………………………………………………………………………4стр.
- Задачи………………………………………………………………………………………………4стр.
- План работы……………………………………………………………………………………5стр.
- Приложения………………………………………………………………………………….. 5стр.
- Гальванический элемент……………………………………………………………… 5стр.
- Батарейки………………………………………………….………………………………….. 6стр.
- Электричество ………………………….………………………………………………….. 6стр.
- Изготовление батарейки……………………………………………………………….7стр.
- Увеличение напряжения……………………………………………………………….11стр.
- Вывод………………………………………………………………………………………………12стр.
- Результат исследовательской работы………………………………………….12стр.
- Новизна……………………………………………………………………………………….….12стр.
- Практическое значение…………………………………………………………………13стр.
- Дальнейшее развитие проекта……………………………………………………..13стр.
-
Список литературы…………………………………………………………………………14стр.
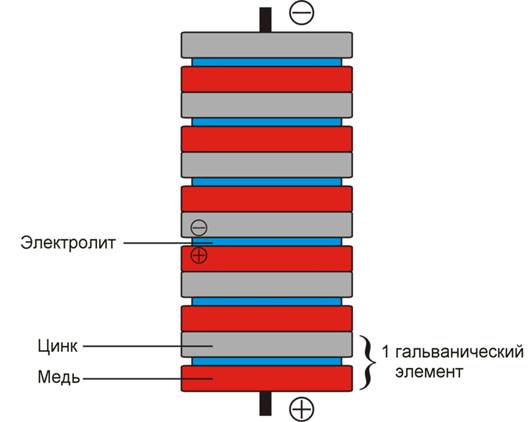
Введение Данная работа представляет собой исследование в области получения электричества при химических реакциях. В 1800 году Алессандро Вольта опустил в банку с кислотой две пластинки - цинковую и медную - и соединил их проволокой. После этого цинковая пластина начала растворяться, а на медной стали выделяться пузырьки газа. Вольта предположил и показал, что по проволоке протекает электрический ток. Так был изобретён «элемент Вольта» - первый гальванический элемент. Для удобства Вольта придал ему форму вертикального цилиндра (столба), состоящего из соединённых между собой колец цинка, меди и сукна, пропитанных кислотой (рис. 5). Вольтов столб высотою в полметра развивал напряжение, чувствительное для человека.
 В 1803 году русский физик Василий Петров создал самый мощный в мире вольтов столб, составленный из 4 200 медных и цинковых кругов и развивающий напряжение до 2 500 вольт. С помощью этого прибора ему удалось открыть такое важное явление, как электрическая дуга, применяемая в электросварке; а в Российской армии стал применяться электрический запал пороха и взрывчатки. В природе электрической дугой является молния во время грозы. Вот уже более двух столетий идёт развитие гальванических элементов, их чаще называют батарейками. Сейчас широко распространены следующие гальванические элементы: солевые, щелочные, никелевые и литиевые. Достоинства гальванических элементов: малый размер, большая электрическая ёмкость, относительная дешевизна. Недостатки гальванических элементов: отсутствие возможности перезаряда, после разряда гальванический элемент становится бесполезным.
В 1803 году русский физик Василий Петров создал самый мощный в мире вольтов столб, составленный из 4 200 медных и цинковых кругов и развивающий напряжение до 2 500 вольт. С помощью этого прибора ему удалось открыть такое важное явление, как электрическая дуга, применяемая в электросварке; а в Российской армии стал применяться электрический запал пороха и взрывчатки. В природе электрической дугой является молния во время грозы. Вот уже более двух столетий идёт развитие гальванических элементов, их чаще называют батарейками. Сейчас широко распространены следующие гальванические элементы: солевые, щелочные, никелевые и литиевые. Достоинства гальванических элементов: малый размер, большая электрическая ёмкость, относительная дешевизна. Недостатки гальванических элементов: отсутствие возможности перезаряда, после разряда гальванический элемент становится бесполезным.
Обоснование выбора темы Электричество является одним из самых важных изобретений человека. Невозможно даже представить в настоящее время жизнь без него. Во времена, когда его не было, люди учились при свечах, ездили на лошадях и паровозах. А о компьютерах и телевизорах даже не мечтали. Мне стало интересно узнать, можно ли получить электричество в домашних условиях. Так была выбрана тема моего исследования: «Химический источник электричества» Актуальность моей работы заключается в том, чтобы находить интересное и необычное рядом, в доступных для наблюдения и изучения предметах, а электричество очень важно для современного человека.
Гипотеза моего исследования: Изучив состав гальванических элементов разного типа, я предположил, что из подручных материалов можно попробовать изготовить солевой элемент.
Цель моего исследования: Получить химический источник напряжения и запитать от него светодиод красного цвета. Предмет исследования: химический источник напряжения. Объект исследования: электрическая энергия. Задачи: узнать, что такое электрическая энергия, как её получают и как измеряют ее количество; изготовить из подручных материалов электрическую батарейку и превратить электрическую энергию в видимый свет; сделать вывод по полученным результатам; выступить с продуктом проекта (презентация) на факультативе «Учусь создавать проекты». Методы исследования:
- Анализ научной литературы и газетных статей.
- Использование Интернета в поиске информации.
- Эксперимент
- Наблюдение
- Фиксирование результатов.
- Анализ.
- Выводы.
- Какими бывают гальванические элементы
- Выбрать материалы, из которых можно изготовить гальванический элемент.
- Подобрать дома доступные материалы и оборудование.
- Познакомиться и использовать необходимые меры безопасности и защиты при проведении эксперимента.
- Изготовить гальванический элемент и превратить электрическую энергию в видимый свет.
- Проанализировать полученные результаты.
- Выступление с презентацией.



На картинке мы видим три батарейки у которых разное напряжение (1,5 вольта, 3 вольта и 9 вольт) кроме того мы знаем что в электрической розетке напряжение 220 вольт. Мне стало интересно, что же такое напряжение, от чего оно зависит и как его измерить.
Электричество На уроках окружающего мира мы изучали, что вещества состоят из молекул, а молекулы из атомов. Но оказывается, что атомы это далеко не самые мелкие частицы. В состав атома входят электроны, которые при определенных условиях и создают электрическое напряжение. Я выяснил, что скопление большого количества электронов в электроде образуют электрическое напряжение, чем больше скапливается электронов, тем больше получается напряжение. Для измерения напряжения существуют специальные приборы - вольтметры. Если в одном электроде электронов больше чем в другом, значит, между электродами существует напряжение и если соединить такие электроды проводником, то по проводнику электроны начнут перетекать так, чтобы в обоих электродах их стало поровну. Движение электронов в проводнике называют электрическим током. Но как же заставить электроны перейти с одного электрода на другой, если они хотят, чтобы в обоих электродах их было всегда поровну. Как раз эту задачу выполняет химическая реакция. Теперь изучив теоретический материал можно переходить к практической части проекта.
Для изготовления солевой батарейки нужны следующие вещества: цинк и медь из которых состоят сами электроды и раствор соли, в котором будет проходить реакция. Именно из за соли батарейка называется соляной. С медью все оказалось просто она входит состав некоторых монет. У меня как раз оказалось несколько старинных пятикопеечных монет. Соль есть на любой кухне. А вот цинк найти не получилось. И мы решили его заменить на алюминиевую фольгу, которая используется в упаковках для продуктов, например шоколада или на монетку, в которой содержится никель. Кроме того мы поэкспериментируем с концентрацией соли, ведь у нас дома есть прибор с помощью которого можно измерять напряжение. С одним электродом мы уже определились (это 5 копеек) проведем эксперимент по выбору второго электрода. Это будут: монета с никелем (2 рубля), фольга от шоколада и фольга от упаковки чая (у неё с одной стороны фольга, а с другой бумага)  На монету- 2 рубля и фольгу от шоколада кладем по кусочку салфетки, а фольгу от чая просто кладем бумажным слоем кверху. Капаем на каждую по одной капли соляного раствора, накрываем «пятаками» и проводим измерения.
На монету- 2 рубля и фольгу от шоколада кладем по кусочку салфетки, а фольгу от чая просто кладем бумажным слоем кверху. Капаем на каждую по одной капли соляного раствора, накрываем «пятаками» и проводим измерения.
- Монета - 2 рубля

- Фольга от шоколада

- Фольга от чая

Из результатов измерения видно, что монета с никелем дала самое низкое напряжение. Фольга от шоколада и чая показали почти одинаковые результаты. Так как с фольгой от чая работать удобнее (не надо использовать салфетку для соляного раствора), будем использовать её в дальнейших экспериментах. Теперь проведем эксперимент с различной концентрацией соли в растворе
- Одна чайная ложка соли на полстакана воды

- Две чайных ложки соли на полстакана воды

- Три чайных ложки соли на полстакана воды
 Из опыта видно, что напряжение не сильно зависит от концентрации соли в растворе.
Из опыта видно, что напряжение не сильно зависит от концентрации соли в растворе.
Как увеличить напряжение Для того, чтобы получить напряжение необходимое для свечения светодиода, собираем девять таких элементов в столб. Фольга бумагой кверху - каплю раствора - медную монету. Затем снова: фольга бумагой кверху - каплю раствора - медную монету и так девять раз.
Измеряем напряжение.  Этого вполне достаточно для свечения светодиода. Подключаем вместо прибора его. Результат на видео:
Этого вполне достаточно для свечения светодиода. Подключаем вместо прибора его. Результат на видео: 
Вывод Соляной раствор вступает в химическую реакцию с алюминиевой фольгой и в результате этого между фольгой и медной монетой появляется напряжение. Складывая элементы в столб напряжение каждого элемента складывается и если сложить 500 монет, то можно получить напряжение, как и в электрической розетке. При подключении к батарее светодиода, через него начинает протекать электрический ток (электроны) вызывая тем самым его свечение. Новизна работы состоит в том, что позволила почувствовать себя в роли экспериментатора и самостоятельно получить источник электрической энергии. Практическое значение исследования в том, что мне удалось узнать много нового об электричестве. Может быть, эти исследования помогут мне выбрать в будущем специальность. Приобретенные знания, умения и навыки обязательно пригодятся в дальнейшей учёбе. Дальнейшее развитие проекта У меня появилось желание работать над этой темой дальше и осуществить ещё несколько идей: получить электричество из других веществ и попытаться найти этому практическое применение.
Список литературы 1. Р.И. Сизова, Р.Ф. Селимова. Юным умникам и умницам «Учусь создавать проекты» Учебник-тетрадь для младших школьников.- Самара: Издательство «Учебная литература».- 2004. 2. Интернет-ресурсы: ru.wikipedia.org/wiki/
18


