- Преподавателю
- Химия
- Подготовка к ЕГЭ по химии. Жиры
Подготовка к ЕГЭ по химии. Жиры
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Кисакова О.А. |
| Дата | 04.12.2014 |
| Формат | doc |
| Изображения | Есть |
Жиры.
Жиры - сложные эфиры глицерина и высших одноосновных карбоновых кислот (так называемых ЖИРНЫХ кислот).
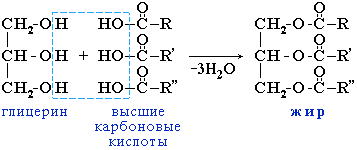
Общее название таких соединений - триглицериды или триацилглицерины, где ацил - остаток карбоновой кислоты -
- С= О
Жирные кислоты.
Предельные кислоты:
Непредельные кислоты:
1. Масляная кислота
С3Н7 -СООН
2. Пальмитиновая кислота
С15Н31 - СООН
3. Стеариновая кислота
С17Н35 - СООН
5. Олеиновая кислота С17Н33СООН
(1 = связь)
СН3-(СН2)7-СН = СН-(СН2)7-СООН
6. Линолевая кислота С17Н31СООН
(2 = связи)
СН3-(СН2)4-СН = СН-СН2-СН = СН-СООН
7. Линоленовая кислота С17Н29СООН
(3 = связи)
СН3СН2СН = CHCH2CH = CHCH2CH=СН(СН2)4СООН
Физические свойства.
Животные жиры
Растительные жиры (масла)
Твёрдые, образованы предельными кислотами - стеариновой и пальмитиновой.
Жидкие, образованы непредельными кислотами - олеиновой, линолевой и другими.
Жиры растворимы в органических растворителях и нерастворимы в воде.
Химические свойства.
-
Гидролиз (омыление) жиров в кислой или в щелочной среде, или под действием ферментов:
а) кислотный гидролиз: под действием кислоты жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
б) щелочной гидролиз - омыление. Получается глицерин и СОЛИ карбоновых кислот, входивших в состав жира.
Кислотный гидролиз
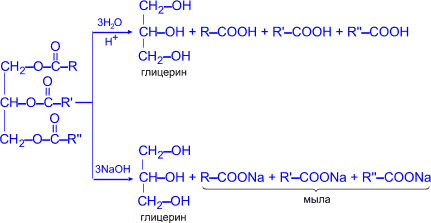
Щелочной гидролиз
В щелочной среде образуются мыла - соли высших жирных кислот (натриевые - твёрдые, калиевые - жидкие).
-
Гидрирование (гидрогенизация) - процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
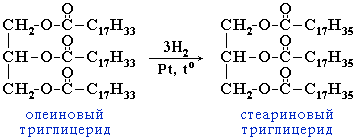
Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее сколько г йода может присоединиться по двойным связям к 100 г жира.
Синтетические моющие средства.
Обычное мыло плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы кальция и магния дают с высшими кислотами нерастворимые в воде соли: С17Н35COONa + CaSO4 (С17Н35COO)2Ca↓ + Na2SO4
Поэтому наряду с мылом из синтетических кислот производят синтетические моющие средства из других видов сырья, например из алкилсульфатов - солей сложных эфиров высших спиртов и серной кислоты. В общем виде образование таких солей можно изобразить уравнениями:
R-CH2-OH + H2SO4 R-CH2-O-SO2-OH + H2O
спирт серная кислота алкилсерная кислота
R-CH2-O-SO2-OH + NaOH R-CH2-O-SO2-ONa + H2O
алкилсульфат
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.


