- Преподавателю
- Химия
- Тестовая диагностическая работа по химии
Тестовая диагностическая работа по химии
| Раздел | Химия |
| Класс | - |
| Тип | Тесты |
| Автор | Орлова Н.В. |
| Дата | 26.10.2014 |
| Формат | doc |
| Изображения | Есть |
ИНСТРУКЦИЯ ПО ВЫПОЛНЕНИЮ
ДИАГНОСТИЧЕСКОЙ РАБОТЫ
На выполнение работы отводится 45 минут. Работа состоит из трех частей и включает 12 заданий.
Часть I (поле А) включает 9 заданий. К каждому заданию предлагается 4 варианта ответа, из которых необходимо выбрать только один правильный. Внимательно прочитайте каждое задание и проанализируйте все варианты предложенных ответов. Обратите внимание на то, что некоторые задания предлагаются в форме отрицания (не)!
Часть 2 (поле В) состоит из двух заданий, на которые надо дать ответ в виде последовательности букв.
Часть 3 (поле С) содержит 1 задание, наиболее сложное. Оно представляет собой расчетную задачу, требующую развернутого решения (с записью разделов «дано», «решение», «ответ»).
Постарайтесь выполнять задания в той последовательности, в которой они даны. Для экономии времени пропускайте задание, которое не удается выполнить сразу, и переходите к следующему. К пропущенному заданию вы сможете вернуться после выполнения всей работы, если останется время.
При выполнении всей работы вы можете пользоваться периодической системой химических элементов Д.И. Менделеева, таблицей растворимости солей, кислот и оснований в воде, электрохимическим рядом напряжений металлов (они прилагаются к тексту работы), а также непрограммируемым калькулятором.
Ответы заданий частей I и 2 заносите в сетку ответов. Решение задания части 3 выполняйте на специально отведенном на бланке ответов месте.
За выполнение различных по сложности заданий дается от одного до трех баллов. Баллы, полученные вами, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов.
11 класс
Вариант 1
Часть 1 (поле А)
1.Элементу, электронная формула которого 1s22s22p53s23p3, соответствует высший оксид
(1) ЭО3 (2) Э2О5 (3) Э2О3 (4) ЭО2
2.В ряду веществ водород, аммиак, хлорид кальция, азот, метан количество веществ с ковалентной неполярной связью равно:
(1) одному (2) двум (3) трем (4) четырем
3.Атомную кристаллическую решетку имеет:
(1) кислород (2) графит
(3) оксид углерода (IV) (4) хлороводород
4.Высшую степень окисления хлор проявляет в кислоте:
(1) HCl (2) HClО (3) HClО4 (4) HClО3
5.Основным является каждый из двух оксидов:
(1) Cs2O и CaO (2) SO3 и P2O5
(3) ZnO и K2O (4) Al2O3 и BaO
6.Гидроксид бария не взаимодействует с:
(1) HCl (2) CO2 (3) CaCl2 (4) H2SO4
7.В схеме превращений Na ![]() NaOH
NaOH 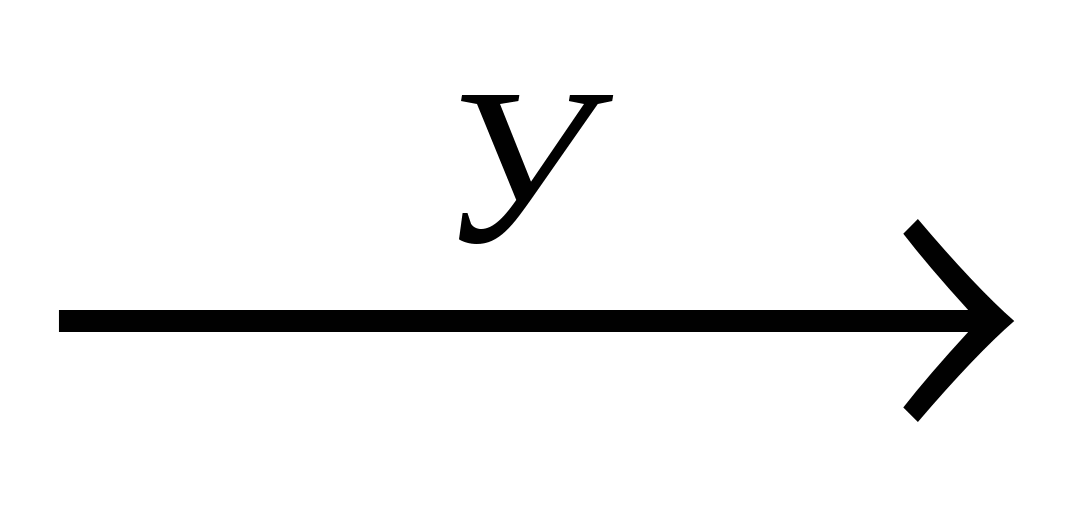 Na2CO3 веществами «Х» и «У» являются соответственно:
Na2CO3 веществами «Х» и «У» являются соответственно:
(1) Н2О и СО2 (2) Na2O и CO2
(3) H2O и CO (4) H2O и CaCO3
8.Изомером гексана является:
(1) 2-метилгексан (2) гексен-2
(3) гептан (4) 2-метилпентан
9.Взорвали 3 л водорода и 2 л кислорода: 2H2 + O2  2H2O. Вычислите объем непрореагировавшего газа. Ответ запишите с точностью до десятых.
2H2O. Вычислите объем непрореагировавшего газа. Ответ запишите с точностью до десятых.
Часть 2 (поле В)
1.Установите соответствие между реагирующими исходными веществами и образовавшимися продуктами реакции:
Исходные вещества
Продукты реакции
1
Na2CO3 + H2O + CO2
А
NaNO3 + CO2 + H2O
2
Na2CO3 + HNO3 (избыток) 
Б
не взаимодействуют
3
Na2CO3 + Ca(OH)2 
В
CaCO3 + NaOH
4
Na2CO3 + Fe 
Г
NaHCO3
Д
FeCO3 + NaOH
2.Установите соответствие между схемой реакции и изменением степени окисления восстановителя:
Схема реакции
Изменение степени окисления восстановителя
1
FeCL3 + HI  FeCl2 + I2 + HCl
FeCl2 + I2 + HCl
А
Fe+3  Fe+2
Fe+2
2
FeCl2 + Cl2  FeCl3
FeCl3
Б
2I- ![]() I2
I2
3
CO + O2  CO2
CO2
В
O2 ![]() 2O-2
2O-2
4
Fe2O3 + HI  FeI2 + I2 + H2O
FeI2 + I2 + H2O
Г
Fe+2  Fe+3
Fe+3
Д
C+2 ![]() C+4
C+4
Е
Сl2 ![]() 2Cl-
2Cl-
Часть 3 (поле С)
1.Органическое вещество содержит 84,21% С и 15,79% Н. Плотность паров вещества по воздуху составляет 3,93. Определите формулу этого вещества.
Вариант 2
Часть 1 (поле А)
1.Какую электронную конфигурацию имеет самый активный неметалл:
(1) 1s22s22p3 (2) 1s22s22p4 (3) 1s22s22p6 (4) 1s22s22p5.
2.В каком ряду представлены только вещества с ковалентной полярной связью:
(1) Cl2, NH3, HCl (2) HBr, NO, Br2
(3) H2S, H2O, S8 (4) HCl, H2O, PH3
3.Атомную кристаллическую решетку имеет:
(1) алмаз (2) аммиак
(3) хлорид аммония (4) сероводород
4.Низшую степень окисления фосфор проявляет в соединении:
(1) Н3РO4 (2) Р2О3 (3) Р2О5 (4) РН3
5.Только кислоты расположены в ряду:
(1) H2SO4, SO2, NaCl (2) K2S, HNO3, KHS
(3) H3PO4, HI, H2S (4) HCl, KCl, HClO
6.Хлорид железа (II) реагирует с каждым из двух веществ:
(1) MgO и HCl (2) CO2 и HNO3 (3) CaO и CO2 (4) AgNO3 и Zn
7.В схеме превращений CuCl2 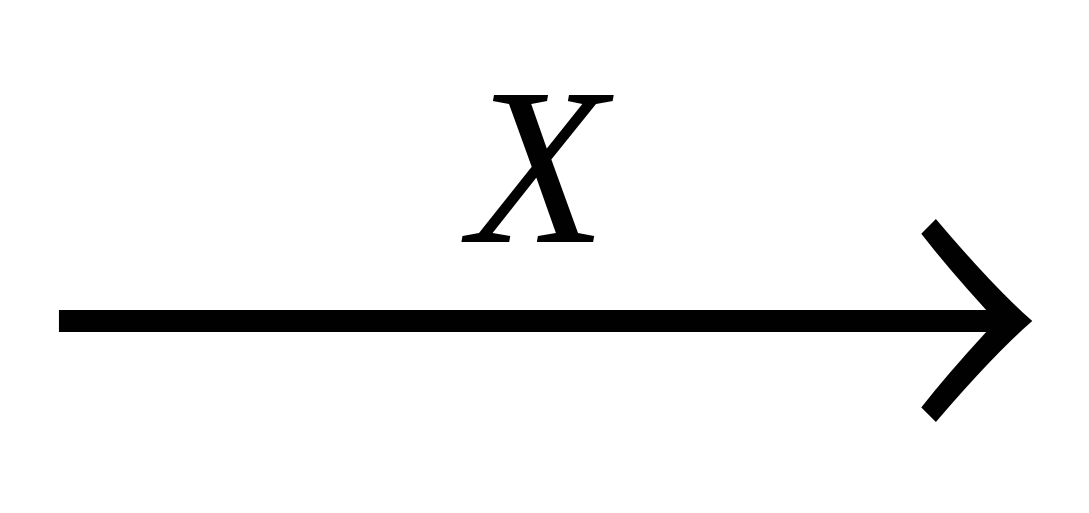 Cu(OH)2
Cu(OH)2 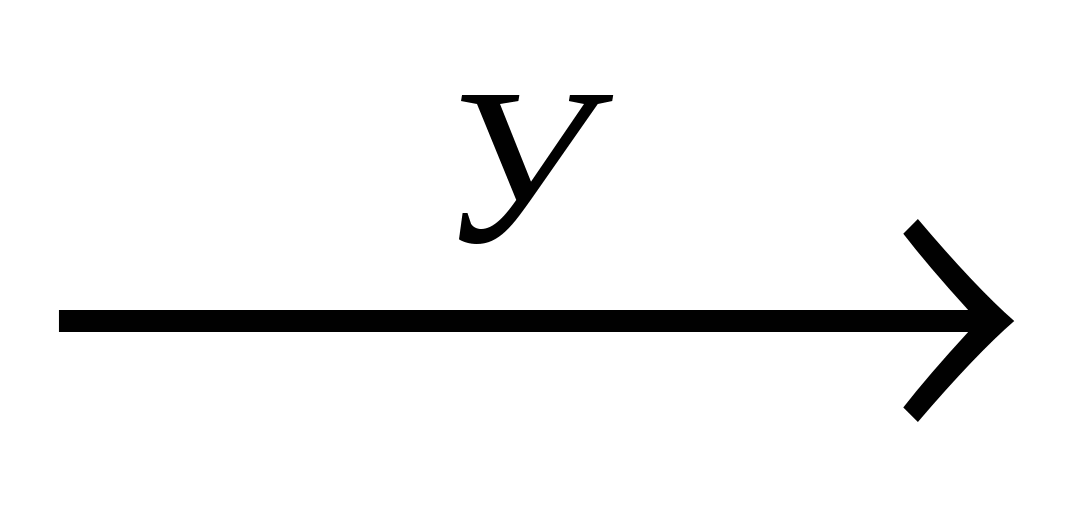 CuCl2 веществами «Х» и «У» являются соответственно:
CuCl2 веществами «Х» и «У» являются соответственно:
(1) NaOH и NaCl (2) H2O и HCl (3) NaOH и HCl (4) H2O и NaCl
8.К гомологическому ряду алканов не относится:
(1) 2,3-диметилпентан (2) гексан
(3) гексен-1 (4) 2-метил-3-этилгептан
9.В реакцию 2CO + O2  2CO2 ввели 3 л оксида углерода (II) и 2 л кислорода. Вычислите объем непрореагировавшего газа. Ответ запишите с точностью до десятых.
2CO2 ввели 3 л оксида углерода (II) и 2 л кислорода. Вычислите объем непрореагировавшего газа. Ответ запишите с точностью до десятых.
Часть 2 (поле В)
1.Установите соответствие между реагирующими исходными веществами и образовавшимися продуктами реакции:
Исходные вещества
Продукты реакции
1
CaCO3 + HCl 
А
CaO + CO
2
CaCO3 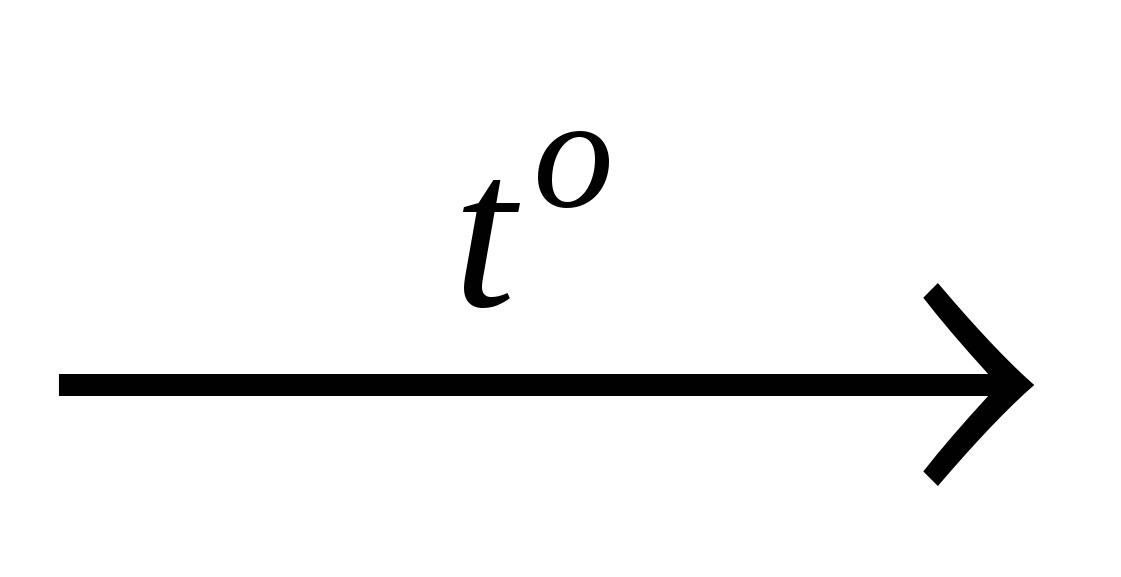
Б
Na2CO3 + Ca(OH)2
3
CaCO3 + NaOH ![]()
В
CaCl2 + CO2 + Н2О
4
CaCO3 + NaCl ![]()
Г
CaO + CO2
Д
не взаимодействуют
2.Установите соответствие между схемой реакции и изменением степени окисления окислителя:
Схема реакции
Изменение степени окисления окислителя
1
H2S + Cl2 + H2O  HCl + H2SO4
HCl + H2SO4
А
2Cl-  Cl2
Cl2
2
KMnO4 + HCl 
 KCl + MnCl2 + Cl2 + H2O
KCl + MnCl2 + Cl2 + H2O
Б
S-2 ![]() S+6
S+6
3
H2SO3 + Cl2 + H2O 
 H2SO4 + + HCl
H2SO4 + + HCl
В
O2 ![]() 2O-2
2O-2
4
SO2 + O2  SO3
SO3
Г
S+4 ![]() S+6
S+6
Д
Cl2 ![]() 2Cl-
2Cl-
Е
Mn+7  Mn+2
Mn+2
Часть 3 (поле С)
1.Вещество содержит 30,4% N и 69,6% О. Плотность паров этого вещества по азоту равна 3,285. Определите молекулярную формулу вещества.
Вариант 3
Часть 1 (поле А)
1.Наименьший радиус имеет атом с электронной конфигурацией:
(1) 1s22s22p63s23p1 (2) 1s22s22p63s23p2
(3) 1s22s22p63s23p3 (4) 1s22s22p53s23p4.
2.В ряду веществ хлороводород, сульфид натрия, бром, хлорид кальция, этан, оксид углерода (IV) количество веществ с ионной связью равно:
(1) одному 2) двум (3) трем (4) четырем
3.Атомную кристаллическую решетку имеет:
(1) алмаз (2) аммиак
(3) хлорид аммония (4) сероводород
4.Максимальную степень окисления азот проявляет в соединении:
(1) Са3N2 (2) N2О (3) Ca(NO3)2 (4) NaNO2
5.Амфотерными гидроксидами являются:
(1) Ca(OH)2 и NaOH (2) KOH и Fe(OH)3
(3) Be(OH)2 и Al(OН)3 (4) Zn(OH)2 и CsOH
6.Оксид углерода (II) реагирует с:
(1) HCl (2) CuO (3) K2SO4 (4) SO3
7.В схеме превращений Zn ![]() ZnSO4
ZnSO4 ![]() Zn(OН)2 веществами «Х» и «У» являются соответственно:
Zn(OН)2 веществами «Х» и «У» являются соответственно:
(1) SO3 и NaOH (2) H2SO4 и NaOH
(3) SO2 и Fe(OH)2 (4) H2SO4 и Mg(OH)2
8.Не является изомером гексана:
(1) гексен-1 (2) 2-метилпентан
(3) 2,2-диметилбутан (4) 2,3-диметилбутан
9.Для получения аммиака в реакцию 3H2 + N2  2NH3
2NH3
ввели 3,3 л водорода и 2 л азота. Вычислите объем образовавшегося аммиака. Ответ запишите с точностью до десятых.
Часть 2 (поле В)
1.Установите соответствие между реагирующими исходными веществами и образовавшимися продуктами реакции:
Исходные вещества
Продукты реакции
1
AlCl3 + NaOH ![]()
А
Al2(SO4)3 + HCl
2
AlCl3 + AgNO3 
Б
не взаимодействуют
3
AlCl3 + H2SO4 (раствор) 
В
AgCl + Al(NO3)3
4
AlCl3 + Zn(NO3)2 
Г
Al(OH)3 + NaCl
Д
ZnCl2 + Al(NO3)3
2.Установите соответствие между схемой реакции и изменением степени окисления восстановителя:
Схема реакции
Изменение степени окисления восстановителя
1
Fe2O3 + CO  Fe + CO2
Fe + CO2
А
Cu0 ![]() Cu+2
Cu+2
2
Сu + H2SO4  CuSO4 + SO2 + H2O
CuSO4 + SO2 + H2O
Б
Fe+2  Fe+3
Fe+3
3
FeCl2 + Cl2  FeCl3
FeCl3
В
Cl2 ![]() 2Cl-
2Cl-
4
Fe(NO3)2 + Zn  Zn(NO3)2 + Fe
Zn(NO3)2 + Fe
Г
C+2 ![]() C+4
C+4
Д
Fe+3  Fe+2
Fe+2
Е
Zn0 ![]() Zn+2
Zn+2
Часть 3 (поле С)
1.Массовая доля углерода в углеводороде составляет 83,33%. Плотность паров этого углеводорода по водороду равна 36. Определите формулу углеводорода.
Вариант 4
Часть 1 (поле А)
1.Элементу, электронная формула которого 1s22s22p53s23p4, соответствует водородное соединение:
(1) HЭ (2) ЭH3 (3) H2Э (4) ЭH4.
2.В каком ряду представлены только вещества с ковалентной неполярной связью:
(1) HCl, O2, CO2 (2) N2, O3, H2
(3) Cu, NaI, H2O (4) CH4, NH3, F2
3.Ионную кристаллическую решетку имеет:
(1) графит (2) бромоводород
(3) железо (4) бромид аммония
4.Минимальную степень окисления сера проявляет в соединении:
(1) K2SO4 (2) Na2SО3 (3) SO2 (4) CaS
5.К солям относится каждое из двух веществ:
(1) КCl и NaHSO3 (2) H2SO3 и Cr(OH)3
(3) NH3 и MgBr2 (4) H2S и CaCO3
6.Могут взаимодействовать друг с другом:
(1) Fe и Ca(OH)2 (2) Al и KNO3 3) Al и NaOH (4) Cu и HCl
7.В схеме превращений Cl2 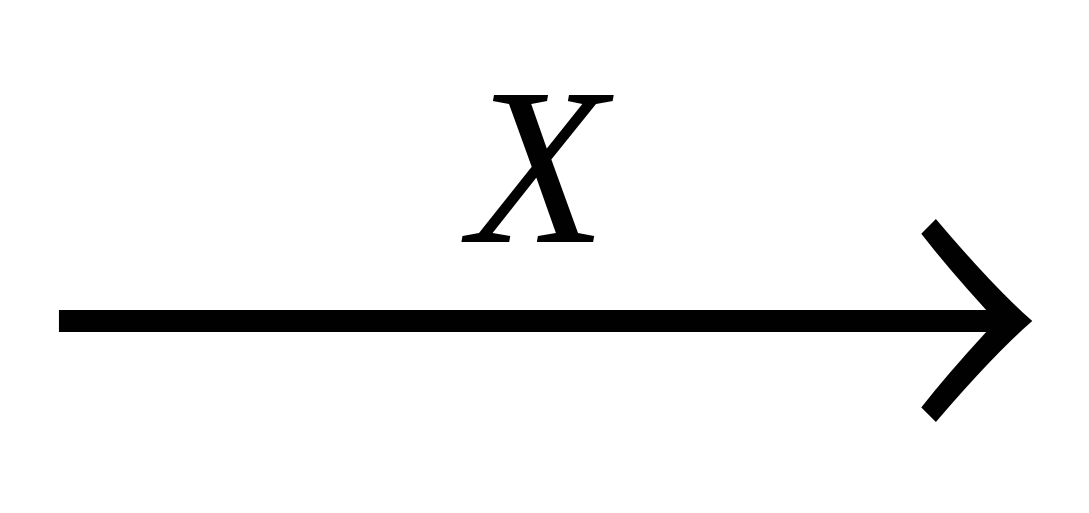 NaCl
NaCl 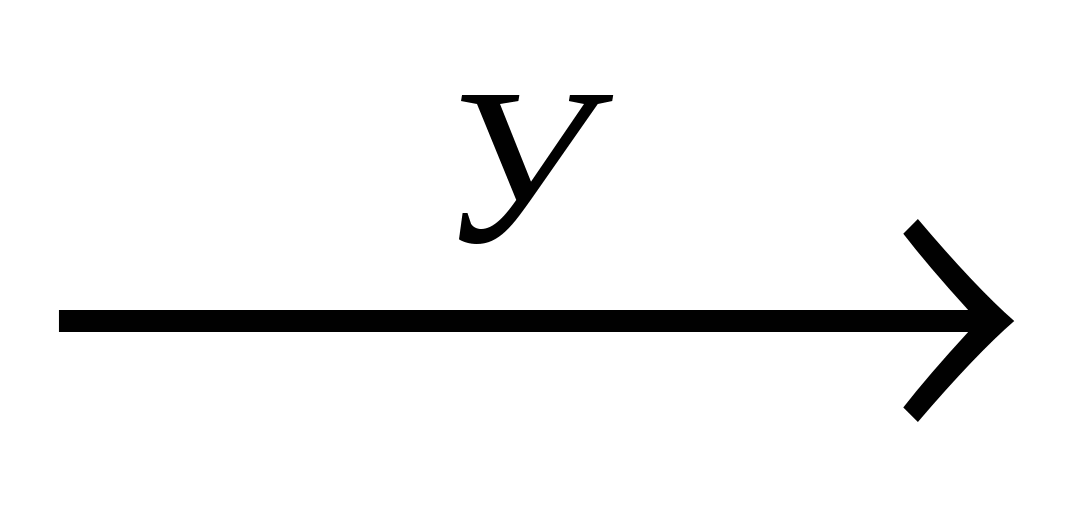 AgCl веществами «Х» и «У» являются соответственно:
AgCl веществами «Х» и «У» являются соответственно:
(1) NaOH и Ag (2) Na и Ag
(3) Na2SO4 и AgNO3 (4) Na и AgNO3
8.2-метилпентан и гексан являются:
(1) гомологами (2) структурными изомерами
(3) геометрическими изомерами (4) одним и тем же веществом
9.В реакцию 2SO2 + O2  2SO3 ввели 3 л оксида серы (IV) и 2 л кислорода. Вычислите объем непрореагировавшего газа. Ответ запишите с точностью до десятых
2SO3 ввели 3 л оксида серы (IV) и 2 л кислорода. Вычислите объем непрореагировавшего газа. Ответ запишите с точностью до десятых
Часть 2 (поле В)
1.Установите соответствие между реагирующими исходными веществами и образовавшимися продуктами реакции:
Исходные вещества
Продукты реакции
1
MgO + SO2
А
MgSO3 + H2О
2
MgO + SO3
Б
MgSO4 + H2
3
MgO + H2SO4
В
MgSO3
4
MgO + H2SO3
Г
MgSO4
Д
MgSO4 + H2O
2.Установите соответствие между схемой реакции и изменением степени окисления окислителя:
Схема реакции
Изменение степени окисления окислителя
1
КМnO4 + HBr  KBr + MnBr2 + H2O
KBr + MnBr2 + H2O
А
Mn+2 ![]() Mn+4
Mn+4
2
MnCl2 + Zn ZnCl2 + Mn
ZnCl2 + Mn
Б
Mn+7  Mn+2
Mn+2
3
КNO2 + KMnO4 + H2SO4 
 KNO3 + MnSO4 + K2SO4 + H2O
KNO3 + MnSO4 + K2SO4 + H2O
В
Cl2 ![]() 2Cl-
2Cl-
4
MnCl2 + Cl2  MnCl4
MnCl4
Г
Mn+2  Mn0
Mn0
Д
N+3 ![]() N+5
N+5
Е
Zn  Zn+2
Zn+2
Часть 3 (поле С)
1.Вещество содержит 85,71% С и 14,29% Н. Относительная плотность паров этого вещества по водороду равна 14. Определите молекулярную формулу вещества.


