- Преподавателю
- Химия
- Исследовательская работа по теме Исследование влияния художественных произведений на развитие познавательных интересов учащихся к химии
Исследовательская работа по теме Исследование влияния художественных произведений на развитие познавательных интересов учащихся к химии
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Лукашевич О.А. |
| Дата | 14.01.2016 |
| Формат | docx |
| Изображения | Есть |
Исследование влияния художественных произведений
на развитие познавательных интересов учащихся к химии
ОГЛАВЛЕНИЕ
1.Введение
2. Химия в художественной литературе
2.1 Химия в поэзии и прозе
2.2 Химические ошибки в литературных произведениях
2.3 Химия в произведениях Артура Конан Дойля
3. Исследование влияния художественных произведений на развитие познавательных интересов учащихся к химии
3.1 Организация экспериментального исследования
3.2 Сравнительный анализ результатов эксперимента
4. Выводы
5. Список литературы
1.Введение
«Не могу представить себе химика, не знакомого с высотами поэзии, с картинами живописи, с хорошей музыкой. Вряд ли он создаст что-либо значительное в своей области…» (Академик А.Е. Арбузов)
Многие химики были не только великими учеными, но и одаренными поэтами, музыкантами. Достаточно вспомнить имена М.В. Ломоносова, А.П. Бородина, Н.А. Морозова, Л.П. Радина и др. Современники Д.И. Менделеева вспоминали о том, что великий химик высоко ценил У.Шекспира, И.Ф. Шиллера, И.В. Гете, В.М. Гюго, Д. Байрона, а также наших классиков, начиная с В.А. Жуковского и А.С. Пушкина, Менделеев очень любил Ф.И. Тютчева, А.А. Фета. А в молодые годы сам писал стихи. Отдыхать Менделеев любил за чтением авторов приключенческого жанра: Ж. Верна, Ф. Купера, А. Дюма и др. И, безусловно, произведения этих и других авторов изобилуют химическими описаниями. На занятиях по химии мы активно устанавливаем метапредметные связи. И вот мы решили узнать, как связаны химия и литература.
Цель работы: провести исследование по выявлению степени сформированности у учащихся познавательных интересов к изучению химии средствами художественной литературы, для достижения поставленной цели необходимо решить следующие задачи 1) выявить родство двух наук - литературы и химии, 2) проследить их связь друг с другом на примере художественных произведений.
Объектом исследования данного проекта являются произведения русской и зарубежной литературы, в которых присутствуют описания химических веществ и их превращений, что делает стихи и прозу более яркими, образными, колоритными, позволяя читателю иметь полное представление о каких-либо событиях. Предмет исследования: процесс формирования элементов познавательной активности в сознании учащихся 8-11 классов через преподавание школьного курса химии средствами художественной литературы.
Гипотеза: если целенаправленно использовать фрагменты художественных произведений на уроках химии, что может способствовать систематическому чтению дополнительной литературы по предмету, то можно сформировать устойчивый познавательный интерес, усилить познавательную потребность и на их основе развить познавательную активность учащихся.
В ходе исследования использовались следующие методы:1) теоретические методы: анализ и изучение литературных источников, проектирование, прогнозирование результатов; 2) эмпирические: анкетирование, тестирование, наблюдение, эксперимент; 3) математические: методы проверки результатов исследования»
Результатом работы будет рассмотрение некоторых литературных произведений с точки зрения химии и их сравнительная характеристика. Результаты работы будут представлены в печатном виде для придания прикладного характера изучаемому материалу. Работа может использоваться на внеклассном обучении, и направлена на то, чтобы помочь привлечь интерес к химии учеников младших классов. Актуальность работы определяется тем, что являясь ученицей, я осознала важность заинтересованности изучаемыми предметами. Такого интереса можно добиться разными путями. Один из них - на основе художественных произведений. Литература помогает нам по - новому раскрыть привычную для нас науку, показать ее в увлекательном, игровом ключе. Апробация результатов исследования осуществлялась в МБОУ Садковской СОШ среди учащихся 8-9 классов.
2. Химия в художественной литературе
2.1 Химия в поэзии и прозе
Химия на протяжении всей истории человечества представлялась предметом романтическим. Эта особенность химии побуждала писателей и поэтов включать в свои произведения образы, навеянные размышлениями о веществе и его превращениях, сравнения, эмоциональные описания явлений, процессов. Всё это делало их произведения более яркими, образными, колоритными.
Часто можно встретить такие литературные выражения: «стальной характер», «железные нервы», «золотое сердце», «свинцовый кулак», «серебряный иней», «золотая заря», «свинцовые тучи».
Связь химии и литературы - настоящая кладезь для реализации творческих замыслов учителя по развитию познавательного интереса учащихся и их мыслительных способностей. Если на уроках химии использовать художественную литературу, то это поможет пробудить и поддержать стойкий познавательный интерес к предмету.
В восьмом классе изучение темы «Периодический закон и периодическая система Д.И. Менделеева» можно начать стихотворениями С. Щипачева, Н. Глазкова, или В. Чивилихина, обратив внимание на величие данного открытия.
Пусть зимний день с метелями
Не навевает грусть -
Таблицу Менделеева
Я знаю наизусть.
Зачем ее я выучил?
Могу сказать зачем.
В ней стройность и величие
Любимейших поэм.
Без многословья книжного
В ней смысла торжество.
И элемента лишнего
В ней нет ни одного.
В ней пробужденье дерева
И вешних льдинок хруст.
Таблицу Менделеева
Я знаю наизусть.
Н. Глазков
Значение периодического закона заключено в словах А.Е. Ферсмана:
«Будут появляться, и умирать новые теории, блестящие сообщения будут сменять наши понятия, величайшие открытия будут сводить на нет прошлые и открывать невиданные по новизне и широте горизонты - все это будет приходить, и уходить, Периодический закон Д.И. Менделеева будет всегда жить, развиваться и совершенствоваться».
Тема: Вода. Свойства воды
1. Физические свойства
«Коммунисты - подпольщики занимались саботажем в организованных немцами мастерских. Отремонтированную немцами водокачку, оставили наполненной водой, а ночью ударили морозы, в результате чего трубы раздулись и полопались, вся система пришла в негодность, все нужно было начинать сначала» (А. Фадеев «Молодая гвардия»).
Можно зачитать отрывок А.С. Пушкина из романа «Евгений Онегин»:
В тот год осенняя погода
Стояла долго на дворе,
Зимы ждала, ждала природа,
Снег выпал только в январе.
На третье в ночь, проснувшись рано,
В окно увидела Татьяна
Поутру побелевший двор,
Картины, кровли и забор,
На стеклах легкие узоры,
Деревья в зимнем серебре,
Сорок веселых на дворе
И мягко устланные горы
Зимы блистательным ковром.
Все ярко, все бело кругом [13].
Это может служить иллюстрацией того, как вода переходит из одного агрегатного состояния в другое.
2. Химические свойства воды.
Ты знаешь, газ мельчайший, водород,
В соединенье с кислородом - это
Июньский дождь от всех своих щедрот,
Сентябрьские туманы на рассветах.
3. Значение воды.
У тебя нет ни вкуса, ни цвета, ни запаха, тебя не опишешь, тобою наслаждаешься, не понимая, что ты такое. Ты не просто необходима для жизни, ты и есть жизнь. С тобою во всем существе разливается блаженство, которое не объяснить только нашими пятью чувствами. Ты нам возвращаешь силы и свойства, на которых мы уже поставили было крест. Твоим милосердием снова отворяются иссякшие родники сердца.
От значения воды необходимо перейти к вопросам экономного ее расходования и бережного отношения к ней, особо подчеркнув о загрязнении воды и возможных при этом последствиях.
Нам снится немая, как камень Земля.
И небо, нагое без птицы,
И море без рыб и без корабля,
Сухие, пустые глазницы.
«Предупреждение» А. Тарковский.
4. Агрегатное состояние воды
В кружево будто одеты
Деревья, кусты, провода,
И кажется сказкою это,
А, в сущности, только вода.
Безбрежная ширь океана
И тихая заводь пруда,
Каскад водопада и брызги фонтана
А все это - только вода.
В бирюзовой дали исчезая
Лебедями плывут облака.
Вот туча идет грозовая
А, в сущности - только вода.
Высокие гребни вздымая,
Бушует морская вода
И топит, как будто играя,
Большие морские суда.
Как пухом зимой одевает
Снег белый родные поля,
Но время придет - все растает
И будет простая вода [4].
5. В романе Ж.Верна вода рассматривается как эффективное топливо будущего « -Какое топливо заменит уголь?
-Вода, - ответил инженер.
-Вода? Переспросил Пенкроф…
-Да, но вода, разложенная на составные части, - пояснил Сайерс Смит. - Без сомнения, это будет делаться при помощи электричества, которое в руках человека станет могучей силой. Да, я уверен, что наступит день, и вода заменит топливо; водород и кислород, из которых оно состоит, будут применятся и раздельно; они окажутся неисчерпаемым и таким мощным источником тепла и света, что углю до них далеко! Наступит день, друзья мои, и в трюмы пароходов станут грузить не уголь, а баллоны с двумя этими сжатыми газами, и они будут сгорать с огромнейшей тепловой отдачей…Вода - это уголь грядущих веков» [4].
Писатель-фантаст Ж.Верн обладал великим даром предвидения. В его произведениях содержится более ста научных предсказаний, многие из которых уже получили технические решения.
Известна важностью своей на всей Земле вода.
Живет в воде для нас, людей, и радость, и беда.
Накопит силы - забурлит, размечет все подряд;
И без усилий растворит в себе и мед, и яд…
Лихую жажду утолит живительным глотком,
И все живое умертвит нещадныи кипятком…
Любой сосуд - то ей не труд - без щелочки займет,
А в лед замерзнет - свой сосуд на части разорвет…
Что охлажденье, что нагрев - закон не писан ей.
Любая жидкость, затвердев, становится плотней.
Любая, только не вода. В ней самый твердый лед,
Когда наступят холода, по верху поплывет...
И замерзает не со дна глубокий водоем,
И корка льда хранит всегда в мороз живое в нем.
И химия в чести везде живет уже века.
А вот аналога воде не знаем мы пока.
Н.К. Шабалина
Тема «Азот и его соединения»
Урок «Оксиды азота».
«Что за проклятый газ? У меня стоит шум в голове. Я, право, чувствую себя как после пяти дюжин кружек пива: заплетается язык и земля качается под ногами» (А.П. Казанцев «Пылающий остров») [6].
Особенно интересно подбирать выдержки литературных произведений, содержащие научную ошибку.
«Воздух состоит из азота и кислорода. Соединение этих двух газов, до сих пор проходивших с большим трудом, и есть горение воздуха». (А.П.Казанцев «Пылающий остров») [6].
Открыл его Лавуазье, он нужен всюду и везде.
В белках он - составная часть, и в воздухе его напасть.
Профессий у него не счесть, им можно красить, можно съесть.
А можно в лампах применить, и в холодильниках хранить,
А также сплавам жизнь продлить, и фрукт, и овощ подкормить.
О ком же речь идет? Кто незнакомец тот?
Весьма ленивый газ АЗОТ.
Тройные связи не дают ему свой темперамент проявить.
Но можно и его расшевелить; тепло, давление системе сообщить,
И уж тогда его остановить нам не придется:
Он то взорвется, то развеселит, то оживит, то попросту прольется.
О.В. Недогибченко[10]
Тема: Сера и ее соединения
Урок «Производство серной кислоты»
При изучении производства серной кислоты можно использовать отрывок из повести К.Паустовского «Бросок на Юг», иллюстрирующий окислительно-восстановительные реакции, происходящие с соединениями серы:
«На поворотах Келасура намывала маленькие песчаные косы. Они горели под солнцем, как золотой песок. В первый раз, попав на Келасури, я намыл из этого берегового песка горсть темно-золотых чешуек - веселых и невеселых. Но через час они почернели и стали похожи на железные опилки. В Сухуми мне объяснили, что это не золото, а серный колчедан». (К.Паустовский «Бросок на юг»).
Урок «Соединения серы».
…Тогда услышал я, о, диво, запах скверный
Как будто тухлое разбилось яйцо
Иль карантинный страж курил жаровней серной.
Я, нос себе, сжав, отворотил лицо [13].
Рассказ - задача
Одно лишь слово
Корней Петрович пригласил Петю Верхоглядкина в кабинет химии.
-Вот, что Петя, - сказал он, - завтра мы будем изучать сероводород. Тебя я назначаю своим ассистентом. Собери прибор для получения сероводорода и проверь его действие. Вот инструкция, вот реактивы. Через двадцать минут я вернусь. Будь осторожен: не отравись сероводородом, поглощай его раствором щелочи!
-Ну что вы, корней Петрович! Имею опыт!...И Петя принялся за дело… Через двадцать минут он растерянно отчитывался:
-Корней Петрович! Здесь какая-то ошибка. Прибор я собрал по рисунку. Вот, поглядите сами. В колбу положил сернистое железо, добавил понемногу серную кислоту. Хоть бы что! Даже не запахло сероводородом. Я уж нагревать стал. Колба покрылась изнутри налетом, но не только белым, но и желтым. А сероводород так и не выделился.
-Прочти еще раз описание опыта.
-Да я его слово в слово помню: на сернистое железо нужно действовать серной кислотой…
-Значит слово в слово? - Корней Петрович оглядел замутневшуюся колбу, подержал в руках склянку с тяжелой маслянистой жидкостью, сомнений не было - серная кислота.
-И все же одно слово, ты Петр, пропустил.
Как же вы думаете?
Свойства серы
Для иллюстрации такого свойства серы, как горючесть, можно привести отрывок из романа С. Вилар «Замок на скале» - разговор старого война и мальчика из благородной семьи: «Этот серый порошок, малыш, - говорил он маленькому лорду, - самая сатанинская вещь на свете. Маленькой искры достаточно, чтобы все вокруг превратилось в ад и полыхнуло огнем. У основания башни есть каморка, где твой батюшка хранит запас пороха, и она всегда под замком, дабы какой-нибудь бедолага не вздумал зайти туда с факелом».
Сернистый газ, образуемый при горении серы:
«Собрав охапку сухой травы, Хуан Дарьен достал из кармана кремень, огниво, фитиль и серную палочку, высек огонь и сунул горящую серную палочку под собранную охапку. На миг взвилось и быстро погасло яркое пламя» .
Нахождение серы в природе:
Говоря о нахождении серы в природе, учитель отмечает, что она встречается в природе как в самородном виде, так и в виде соединений, о чем можно прочитать не только в учебнике, но и в художественной литературе. В фантастическом романе В.А. Обручева «Плутония», повествующем об экспедиции ученых в неведомый мир под земной поверхностью читаем: «За площадкой круто поднималась противоположная стена, густо покрытая белыми, желтыми и красными налетами и натеками. В желтых налетах нетрудно было узнать самородную. Серу в виде мелких и крупных кристаллов, сидевших в пустотах лавы или покрывавших ее поверхность нетолстым слоем»[14].
Среди природных соединений серы большое значение минерал пирит. Жюль Верн в «Таинственном острове» описал получение из пирита серной кислоты. Учитель обращает внимание на название материала: прослеживается связь с греческим «пирос» - огонь. Исходя из этого, пирит - огненный камень, и именно в этой роли он был известен еще на заре человечества. Затем он читает отрывок из книги Э.Штерха «Охотники на мамонтов» о жизни первобытного человека:
«Копчем увидел у нее на ладони блестящий камушек…вдруг несколько лучей снова упали на камень, и он весь заискрился…Насколько тверд этот блестящий камень? Кремень скользнул по камню…светящиеся искры разлетелись в стороны и исчезли в темноте…Появление светящихся искр в темной пещере тотчас заинтересовало охотников. Они повскакивали со своих мест, в восторге глядя на руки Копчема, которые так и мелькали, выбивая из огненного камня разлетающие искры.
-Огненный камень! У него есть огненный камень! У нас будет огонь! Будет все! [4].
Кусок пирита выполнял функцию огнива. Этот достаточно распространенный материал стал для наших далеких предков ступенькой к цивилизации.
Следующий отрывок из «Золотой розы» К. Паустовского: «Есть очень насыщенные минеральные источники. Стоит положить в такой источник ветку или гвоздь, что угодно, как через короткое время они обрастут множеством белых кристаллов и превратятся в подлинные произведения искусства» [39].
Тема: Фосфор и его соединения
«Крыша в хижине была худая, с потолка падали дождевые капли, но в очаге слабо мерцало голубое пламя…Концы хвороста тлели голубоватым огнем. О фосфоре, воспламеняющемся от воды, они не вспоминали, им было не до химии…» (Р.А. Штильмарк. «Наследники из Калькутты»).
Тема: Углерод и его соединения
А вот отрывок произведения В.Д.Одоевского «Мороз Иванович»: «…А я затем в окошки стучусь, чтобы не забывали печей топить, да трубы вовремя закрывать, а не то, ведь я знаю, есть такие неряхи, что… закроют… когда ещё не все угольки прогорели, а оттого в горнице угарно бывает, голова у людей болит, а в глазах зелено, даже и совсем от угара умереть можно».
Речь идет о сильном яде - оксиде углерода (II), угарном газе (CO).
При горении угля в печи происходит химическая реакция:
С + О2 = СО2 +402 кДж.
Но если трубу закрыть раньше того, как угли прогорят, то в печи скапливается избыток углекислого газа, который взаимодействует с еще раскаленными углями.
СО2 + С = 2СО - 160 кДж.
При закрытой трубе угарный газ проникает в помещение. При вдыхании он попадает в кровь человека и образует с гемоглобином стойкое соединение.
Огонь… Можно ли представить наше существование без огня? Он вошел в нашу жизнь, стал неотделим от неё. Но огонь может быть не только другом. Пожар - одно из страшнейших бедствий. Часто он является предметом описания в литературе, например, в романе «Унесенные ветром» М. Митчелл. Один из способов тушения пожаров - использование огнетушителя. Самодельный огнетушитель я изготовила в домашних условиях, основанный на взаимодействии пищевой соды и уксусной кислоты.
Тема: Алюминий и его свойства
Если порошок алюминия сильно нагреть, то он воспламеняется и сгорает ослепительным пламенем: 4Al + 3O2 = 2Al2O3. Эта реакция используется для изготовления бенгальских огней и фейерверков и легла в основу рассказа Н.Носова «Бенгальские огни»
Тема: Коррозия металлов
Интересно отображают поэты всем известное явление коррозии металлов:
…На рукомойнике моем
Позеленела медь.
Но так играет луч на нем,
Что весело глядеть…
(А. Ахматова. Из сб. «Вечер»)
Медь взаимодействует сначала с кислородом, а затем с углекислым газом и водой, постепенно превращаясь в основной карбонат меди - малахит:
2Сu + O2 = 2CuO
2CuO + CO2 + H2O= (CuOH)2CO3
…От медленных лобзаний влаги
Нежнеет грубый свод гробниц,
Где зеленеют саркофаги
Святых монахов и девиц…
(А. Блок. Итальянские стихи)
2.2 Химические ошибки в литературных произведениях
Как уже было сказано, авторы художественных произведений нередко допускают ошибки в описании химических веществ и процессов:
…Ржавеет золото и истлевает сталь,
Крошится мрамор. К смерти все готово.
Всего прочнее на земле печаль
И долговечней - царственное слово…
(А. Ахматова. Из.сб. «Бег времени»)
Ответ: конечно, золото не ржавеет, не коррозирует. Это ошибка, но как точно подмечена разница в динамике разрушения стали и мрамора!
А какую неточность можно заметить в стихотворении Л. Лавренева «Нобуж»?
…В озон превращается воздух…
Ответ: В озон превращается не воздух, а кислород.
Уравнение химической реакции:
3О2 = 2О3 (при электрическом разряде).
Писатели-фантасты часто используют химическую терминологию, при этом нередко допуская неточности и ошибки. Например, в романе А. Беляева «Продавец воздуха» читаем:
«Мистер Бейли открыл шестую дверь, и я увидел изумительное зрелище. Перед нами был огромный подземный грот. Десятки ламп освещали большое озеро, его вода отличалась необычайно красивым голубым цветом…
-Жидкий воздух, - сказал Бейли
Я был поражен. До сих пор мне приходилось видеть жидкий воздух только в небольших сосудах нашей лаборатории» [1].
Ответ: Хочется заметить, что температура, при которой воздух становится жидким, должна быть ниже минус 196 градусов. Человеку при этой температуре невозможно находиться вблизи этого «озера», он погибнет от переохлаждения.
Как вы думаете, имеет ли запах серная кислота? Обратимся к популярной повести А.Н. Рыбакова «Приключения Кроша»:
«…Стоящий в электроцехе запах серной кислоты напомнил мне о сожженных в Липках брюках…».
Что хотел сказать автор повести, и как следует видоизменить фразу, чтобы она звучала химически грамотно? Разумеется, в цехе дуговой электросварки не могло пахнуть серной кислотой - ей там просто неоткуда взяться. Тогда что имел ввиду автор? При дуговой электросварке материалы, чаще всего металлы, сплавляются теплом электрической дуги, температура которой достигает 5000 градусов. При столь высокой температуре могут образовываться: озон, оксид азота(II).
Поэтому фразу в тексте следовало бы изменить так:
«…Стоящий в электроцехе запах озона, оксидов азота и азотной кислоты напомнил мне о сожженных в Липках брюках…»
Крылатая фраза «без фосфора нет мысли» появилась после установления Генсингом наличия ионов фосфора в мозговой ткани. Особенно любили применять ее механистические материалисты прошлого века.
Хотя все важнейшие физиологические процессы в организме человека, начиная с сокращения мышц и кончая мышлением, связаны с химическими превращениями фосфора, но это не дает повода считать, что присутствие только фосфора обеспечивает свойство мозга - мыслить.
Называя фосфор «белым», следует иметь ввиду, что мы допускаем ошибку. В чистом виде белый фосфор бесцветное прозрачное вещество.
Кристаллы белого фосфора очень сходны с алмазами, они совершенно бесцветны, идеально прозрачны и настолько сильно преломляют свет, что на солнце играют всеми цветами радуги.
Нередко высказывания требуют соответствующих пояснений. К примеру, у И. Сильвинского мы читаем:
…Видишь - мрамор:
Это просто кальций…
Мрамор - это не кальций, а соль, карбонат кальция. Это ошибка.
И конечно, нельзя не вспомнить отрывок из знаменитой «Собаки Баскервилей» А.К.Дойла, в котором допущена существенная химическая ошибка: "…Да! Это была собака, огромная, чёрная, как смоль. Но такой собаки ещё никто из нас, смертных, не видывал. Из её отверстой пасти вырывалось пламя, глаза метали искры, по морде и загривку мерцал переливающийся огонь. Ни в чьём воспалённом мозгу не могло возникнуть видение более страшное, более омерзительное, чем это адское существо, выскочившее на нас из тумана… Страшный пёс, величиной с молодую львицу. Его огромная пасть всё ещё светилась голубоватым пламенем, глубоко сидящие дикие глаза были обведены огненными кругами. Я дотронулся до этой светящейся головы и, отняв руку, увидел, что мои пальцы тоже засветились в темноте.
- Фосфор, - сказал я".
Светится в темноте белый фосфор, а он, во-первых, ядовит, а во-вторых, самовоспламеняется на воздухе, поэтому его нельзя использовать для нанесения на тело животного.
Из произведения Александра Богданова «Красная звезда» :
«Это была «кислородная комната». В ней хранились запасы кислорода в виде 25 тонн бертолетовой соли, из которой можно было выделить по мере надобности 10 тысяч кубических метров кислорода».
По уравнению реакции разложения бертолетовой соли (хлората калия) проверяем вычислением правильность утверждения автора.
Получаем ответ: из 25т бертолетовой соли можно получить около 6,8 тыс. м3 кислорода, что на 32% меньше указанного объема.
2.3 Химия в произведениях Артура Конан Дойля
Благодаря своим химическим знаниям герой романов Артура Конан Дойля Шерлок Хомс, с легкостью раскрывал преступные дела, часто помогал полиции в этих делах. Химия здесь играла основную роль, но она выбрана не случайно, так как сам Артур Конан Дойл предпочел карьеру медика и поступил в Эдинбурский университет, то есть он сам хорошо владел химическими знаниями и свои знания отразил в своем персонаже.
«Проблема Вултонской тюрьмы»
О чем повествуется?
В один вечер из Скотланд-Ярда Шерлоку Х. и доктору В. сообщили о странных событиях в Вултонской тюрьме. Вожак преступной банды, на счету которой множество преступлений, был заключен в Вултонскую тюрьму, но другие члены банды остались на свободе. Поскольку он крепко держал всех в своем кулаке, бандиты привыкли ни шагу не делать без его приказа, и в Лондоне на несколько месяцев стало тихо. Но две недели назад банда снова начала действовать. Шерлок Х. выдвинул предположение, что вожак руководит шайкой, даже находясь в тюрьме. После посещения Вултонской тюрьмы сыщики узнали, что заключенный каждый день получает газету, которая тщательно проверяется до и после прочтения им, также он получает сырой картофель каждую пятницу, потому что у него болит локоть, и он растирает картофель и делает примочки из кашицы. Но доктор В., воскликнул, что медицина ничего не знает о картофельных примочках. Как стало известно, вожак передает приказы своей банде каждое воскресенье.
Для разгадки необходимо прежде всего ответить на три вопроса:
1. Как передаются послания из тюрьмы?
2. Какая химическая реакция поможет Холмсу разоблачить Стампа?
3. Кто передает банде приказы Стампа?
Разгадка
1. Послания передаются с помощью тех самых газет, заключенный растирал картофель, отжимал сок через бинт и с помощью проволоки, спички или бумажной трубочки писал свои приказы картофельным соком, т. е. крахмалом, на газете. Проще всего ему было бы метить буквы и слова газетных статей, передавая свой текст. Проверяющий не мог видеть пометок заключенного, поскольку крахмал бесцветен.
2. Холмс вынул свой перочинный нож и разрезал клубень пополам. Затем из саквояжа достал склянку с раствором йода и капнул раствором на свежий срез. Поверхность среза сразу же окрасилась в синий цвет.
Крахмал + йод = клатрат (соединение темно-синего цвета)
С6Н10О5 + J2=J2*( С6Н10О5)
3. Глухонемой охранник Эдмунд, которого вожак, беззвучно шевеля губами, мог попросить о небольшом одолжении, забирал проверенную Уильямсом газету и передавал ее посланнику бандитов - какому-нибудь безобидному старичку, - тоже не подозревая о послании. А уж в банде хорошо знали, как прочитать послание.
«Смертоносный гость на Бейкер- стрит, 221»
О чем повествуется?
Однажды доктор В. подарил Шерлоку Х. фарфоровый чайный набор из Индии. Через 6 недель после отъезда доктора В. ему пришлось вернуться назад, так как он узнал от миссис Хадсон, что Ш.Х. при смерти. От нее доктор В. узнал, что Ш. ел все меньше и меньше, пока не перестал совсем принимать пищу. У него сначала болел живот. Потом боли перешли на ноги, на руки и на плечи. При осмотре ШХ, доктор В. увидел темную линию вокруг рта у края десен, а вытянув его правую руку прямо: кисть руки безвольно упала. Юный мальчишка помогал ШХ провести некоторые опыты.
Он примерно полчаса кипятил уксус в красно-белом чайнике. Потом вылил варево в эту стеклянную штуку. Затем по указанию ШХ смешал сульфид железа с соляной кислотой - получился вонючий газ. Он нацепил на горлышко бутыли резинку, и конец сунул в стеклянную банку с уксусом. Из того конца резинки пошли пузыри, и все в банке стало черным, как ночь.
Для разгадки необходимо прежде всего ответить на три вопроса:
1. Что стало причиной болезни Холмса?
2. Кто виновен в болезни Холмса?
3. В чем смысл химической пробы, проведенной мальчиком?
Разгадка:
1. Причиной его болезни стало отравление свинцом. Нарушение работы желудка. Боли в животе, мышцах и суставах. Классический симптом-появление «свинцовой полосы»- темного окрашивания десен возле зубов, а также опускание кистей рук из-за ослабления мышц.
2. Виновен только Ватсон, так как это он подарил ШХ керамический набор.
3. PbO+2CH3СООН=Рb(CH3COO)2+H2O
FeS+2HCl=H2S+FeCl2
H2S+Pb(CH3OO)2=PbS+2 CH3СООН
Мальчишка должен был смешать сульфид двухвалентного железа и соляную кислоту. При этом образуется сероводород, который пахнет тухлыми яйцами. Через шланг газообразный сероводород поступал в склянку Эрленмейера. В склянке была уксусная кислота, которую до того мальчик кипятил в керамическом чайнике. Кислота при нагревании извлекла свинец из керамики чайника в виде свинцового сахара.
3. Исследование влияния художественных произведений на развитие познавательных интересов учащихся к химии
3.1 Организация экспериментального исследования
Экспериментальное исследование включало два этапа. Все виды эксперимента образовывали органическое единство.
Основой исходного этапа исследования стал констатирующий эксперимент, целью которого была диагностика состояния исследуемого вопроса в практике школ обучаемых. Констатирующий эксперимент включал в себя:
1) исследование развития познавательных интересов учащихся в процессе изучения химии;
2) выявление уровня познавательных интересов учащихся к изучению химии.
Во время констатирующего эксперимента велось систематическое наблюдение на уроках; фиксировались приемы, применяемые учителем для возбуждения познавательного интереса к изучению химии, оценивалась эффективность приемов, отмечались наиболее яркие проявления интереса к учению.
Результаты констатирующего эксперимента, дальнейший поиск и анализ литературных источников позволили выдвинуть гипотезу исследования, сформулировать задачи и в соответствии с ними продолжить проведение педагогического эксперимента.
Поисковый (корректирующий) эксперимент проводился с введением нового фактора, например, использование фрагментов литературных произведений при изучении различных тем школьной программы по химии с целью корректирования оптимального содержания, а также с применением методов, приемов, форм и средств обучения, стимуляции мотивов ориентированных на развитие познавательных интересов учащихся к изучению химического материала. Проведению формирующего эксперимента предшествовала разработка целостной методики использования и алгоритма обсуждения фрагментов художественных произведений на уроках химии и развитие в этом процессе познавательного интереса. При его проведении мы использовали сравнительный метод. Сравнительный эксперимент проводился с целью сравнения результатов определения в контрольных и экспериментальных группах. Для проведения сравнительного эксперимента были выделены контрольные- 8 и экспериментальные-9 классы: в МБОУ Садковской СОШ. Обучение в контрольных классах проводилось обычными методами, в экспериментальных - по разработанным нами методическим рекомендациям, ориентированных на развитие познавательного интереса к изучению химического материала в средней школе. Контролирующий эксперимент позволил оценить влияние художественных произведений на развитие познавательного интереса к изучению химии.
Эксперимент, в отличие от наблюдения, позволяет учителю активно влиять на интересующее явление, изменять условия его протекания, ориентировать их изменение в желаемом направлении.
С целью изучения осознанности познавательного интереса можно провести следующий эксперимент. Учащимся предлагается на выбор несколько заданий различной степени сложности:
1-е задание требует механического повторения уже выполнявшихся неоднократно упражнений;
2-е задание - усложненный вариант, требующий применения полученных знаний в несколько изменившихся условиях;
3-е задание творческого характера.
По тому, какое задание выбрал ученик, можно сделать вывод о том, является его интерес осознанным (такой ученик выбирает задание творческого характера) или нет. Эксперимент следует повторить несколько раз, факты зафиксировать с целью подтверждения выводов от степени осознанности интереса.
Выявляя наличие у учащихся интереса к познанию, определяется индекс их уверенности в таком наличии.
Учащимся предлагается 5 уровней самооценки, для каждого из которых определен "описательный ориентир" (критерий):
1 уровень "обладаю" - испытываю интерес к учебной деятельности, моральное удовлетворение от самого процесса получения знаний;
2 уровень "скорее обладаю, чем не обладаю" - испытываю интерес к учебной деятельности, но зачастую не испытываю эмоционального удовлетворения от процесса получения знаний;
3уровень "скорее не обладаю, чем обладаю" - не всегда испытываю интерес к процессу получения знаний, чаще привлекает конечный результат - получение хорошей отметки;
4уровень "не обладаю" - плохо представляю, есть ли у меня интерес к познанию, т.к. редко выполняю умственную работу с удовольствием;
5 уровень "затрудняюсь ответить" - у меня нет интереса к познанию, я учусь, потому что заставляют родители (боюсь отрицательного отношения к себе учителей и родителей, нет другого выхода и т.п.).
Формула вычисления общего индекса уверенности в наличии познавательного интереса:
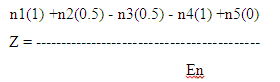
n1 - количество ответов "обладаю", n2- количество ответов "скорее обладаю, чем не обладаю", n3 - количество ответов "скорее не обладаю, чем обладаю", n4 - количество ответов "не обладаю", n5 - количество ответов "затрудняюсь ответить", Еn - общее количество ответов
Различной степени уверенности придаются условные числовые значения: +1(n1) - максимум уверенности, +0.5(n2) - уверенность, 0(n5) - неопределенное и безразличное отношение, -0.5(n3) - неуверенность, -1(n4) - максимум неуверенности. Такая методика выявляет индекс уверенности учащихся в наличии у них познавательного интереса, но не несет информации относительно его уровня. Оценку уровня ПИ можно проводить по методикам, перечисленным выше.
3.2 Сравнительный анализ результатов эксперимента
Результаты исследования обработаны и представлены в таблице 1:
Таблица 1. Результаты самооценки познавательных интересов (ПИ) учащимися
-
Группы/ число учащихся
Начало эксперимента
Конец эксперимента
Уровень самооценки(n)
Индекс уверенности в наличии П.И.
Уровень самооценки(n)
Индекс уверенности в наличии П.И.
К (13)
n1=1 n2=2 n3=3 n4=3 n5=4
-0,192
n1=2 n2=4 n3=2 n4=2 n5=3
0, 076
Э (19)
n1=2 n2=3 n3=4 n4=3 n5=7
-0,078
n1= 5 n2=9 n3=3 n4=2 n5=0
0,315
Результаты самооценки познавательных интересов учащихся до и после проведения педагогического эксперимента, отражены в диаграммах (рис.1)
Рис.1 Диаграммы самооценки познавательных интересов учащихся в контрольном классе до и после эксперимента
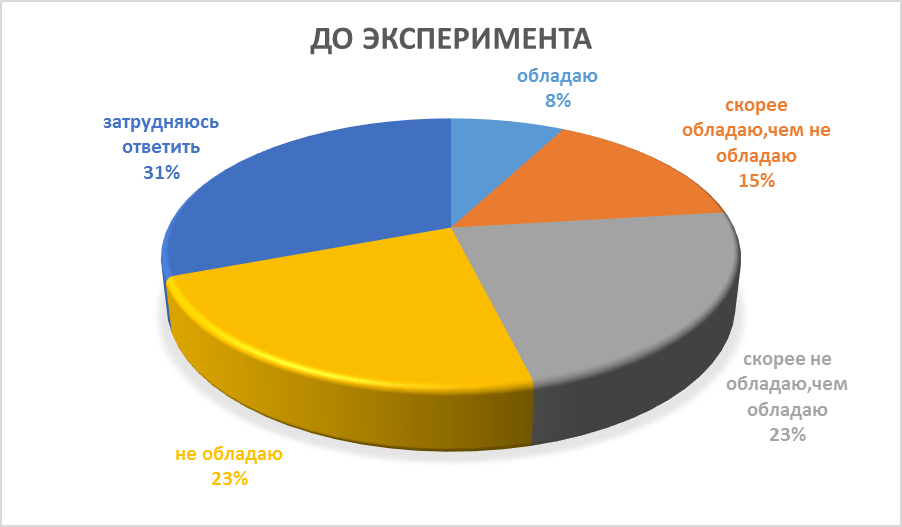
Рис 2. Диаграмма самооценки познавательных интересов учащихся в экспериментальном классе до и после эксперимента
Таким образом, можно сделать вывод, что в контрольном классе 15% учащихся плохо представляют, есть ли у них интерес к познанию, 23% учащихся не всегда испытывают интерес к процессу получения знаний, их чаще привлекает конечный результат - получение хорошей отметки, 23% учащихся испытывают интерес к учебной деятельности, но зачастую не испытывают эмоционального удовлетворения от процесса получения знаний, лишь 7% испытывают интерес к учебной деятельности, 30,7% - затрудняются ответить, у них нет интереса к познанию. В экспериментальном классе 15,7% - не обладают интересом, 30,7% - не всегда испытывают интерес к учению, 15,7% - скорее обладают, чем не обладают,10,5%- обладают и 53% не испытывают интереса к учению.По окончании эксперимента видно, что в контрольных классах 15,3% испытывают интерес к учению, 30,7% испытывают интерес к учебной деятельности, 15,3% не всегда испытывают интерес, 15.3% не обладают познавательным интересом, 23% затрудняются ответить.
В экспериментальных классах после эксперимента стали испытывать интерес к учению 38,4% учащихся, 47,3% испытывают интерес к учебной деятельности,10,52% не всегда испытывают интерес к учебе, 0% не обладают познавательным интересом.
Таблица 2. Выявление и оценка познавательных интересов (ПИ) учащихся к химии
-
группы
Уровни интересов
Х-качественный показатель интереса
Y-относительный прирост интереса
Высокий В
Средний С
Высокий+ средний
Э
До эксперимента
2/11%
3/16%
5/27%
0,27
3,4
После эксперимента
5/38%
9/47%
14/85%
0,85
К
До эксперимента
1/8%
2/15%
3/23%
0,23
2
После эксперимента
2/15%
4/31%
6/46%
0,46
Результаты педагогического эксперимента показали, что в экспериментальных классах относительный прирост познавательного интереса учащихся составил 3,4, что значительно выше, чем в контрольных классах - 2.
Результаты выявления и оценки познавательных интересов учащихся к химии, представлены на сравнительной гистограмме (рис.3)
Рис.3 Сравнительная гистограмма выявления качественного показателя интереса у учащихся.
4. Выводы
Проведенное теоретическое и экспериментальное исследование позволяет сделать следующие выводы:
-
Осуществлен анализ состояния учебно-познавательной деятельности учащихся в общеобразовательной школе на уроках химии.
-
Разработан дидактический комплект, который дает возможность использования фрагментов художественных произведений на уроках и во внеклассных мероприятиях по химии.
-
Определены наиболее целесообразные методические подходы обсуждения фрагментов художественных произведений на уроках химии.
-
Результаты экспериментально-методического исследования подтверждают эффективность использования художественных произведений на уроках химии и положительную их роль в развитии познавательных интересов учащихся к химии.
-
Благодаря тесной связи с другими науками, наука химия может стать увлекательным источником теоретических и практических знаний.
-
Фрагменты литературных произведений тренируют внимание, аналитическое мышление и формируют навыки исследовательской деятельности.
5. Список литературы
1.Беляев А. «Продавец воздуха». М.: «Эксмо», 2008. 25-26 с.
2. Верн Ж. Собрание сочинений. М.: Азбука - классика, 2004. 321 с.
3. Верн Ж. Опыт Доктора Окса/Пер. с фр. Алма - Ата: МГП, 1993. С. 238
4.Высоцкий В.С. Песня Кэррола//Соч.: В 2-х т.Т.2. Екатеринбург: Посулторг, 1994.
5. Занимательно об азоте и фосфоре: Методическая разработка для студентов-практикантов. / Под. Ред. В.И. Толкунова, Л.К. Гиренковой. Куйбышев, 1978. 19 с.
6. Казанцев А.П. «Пылающий остров». М.: Молодая гвардия, 1983.С. 45-48
7. Карпова А.А. Химия и литература// Химия в школе. 2003. №1. С.23-26.
8. Корнева Н.В. Интегрированные уроки химии и литературы. 2006. festival. 1 september.ru/articles/211159.
9. Леднев О.Б. Как химический язык попал в литературу// Химия в школе.2001. №6. 63.с
10. Лермонтов М.Ю. Сочинения. Т.1, М.: Правда, 1989.
11. Пушкин А.С. Сказка о мертвой царевне и о семи богатырях // Собр. Соч.: в 10 - и т. Т.3. М.: Художественная литература, 1960. 57 с.
12. Пушкин А.С. Собр. Соч.: в 10 - и т. Т.6. М.: Художественная литература, 1962. 34 с.
13. Пушкин А.С. Евгений Онегин // Собр.соч.: В 10-и т. Т.1. М.: Художественная литература, 1960. 78 с.
14. Роллинг Дж.К. Гарри Поттер и философский камень. М.: ООО «Росмэн - Издат», 2000. С. 258-268.
15. Ученик чародея // Сказки народов мира. Английские сказки. К.: Синопсис», 1992. 156 с.
16. Фадеев А. «Молодая гвардия», М.: Художественная литература, 1962. С.
17. Хачатрян И.Н. Неисчерпаемое море солей // Химия в школе. 2001. №1. С.20-25.
18. Химические приключения Шерлока Холмса (Ваддель Томас Г., Риболт Томас Р.)


