- Преподавателю
- Химия
- Урок 8 класс Закон сохранения массы веществ
Урок 8 класс Закон сохранения массы веществ
| Раздел | Химия |
| Класс | 8 класс |
| Тип | Конспекты |
| Автор | Чернявский Д.П. |
| Дата | 26.12.2015 |
| Формат | docx |
| Изображения | Есть |
Күні
Дата------------------------
Сабақ:
Урок: № 14.
Пән:
Предмет: Химия 8 класс.
Тақырып:
Тема: Закон сохранения массы веществ.
Мақсат:
Цель: Экспериментально доказать закон сохранения массы веществ. На основе этого закона сформировать понятие о материальном балансе химической реакции. Сформировать понятие об уравнении химической реакции как об условной записи, отображающей превращения веществ. Научить расставлять коэффициенты в уравнениях реакций.
Әдіс-тәсілдер:
Методы: словесные, наглядные.
Сабақ түрі:
Тип урока: комбинированный
Сабақ барысы: Ход урока:
После проверки умения составлять химические формулы веществ по валентности элементов учитель переходит к рассказу об опытах, проводимых М. В. Ломоносовым и А. Лавуазье, которые независимо друг от друга открыли закон сохранения массы веществ при химических реакциях. Затем учитель переходит к формулировке закона.
Внимание учащихся следует обратить на то, что сохранение массы веществ наблюдается только при таких явлениях, когда атомы не разрушаются - происходит их перегруппировка. Так как число атомов до реакции и после реакции остается неизменным, то их общая масса также не изменяется.
Далее учитель переходит к демонстрации опытов, иллюстрирующих закон сохранения массы веществ (горение красного фосфора и взаимодействие сульфата натрия с хлоридом бария в закрытых сосудах).
Рассматривается значение закона сохранения массы веществ. Затем учитель сообщает, что этот закон является основой для составления уравнений химических реакций, и переходит к условной записи химических реакций. При этом используются ранее приобретенные знания: понятие «валентность», правила составления формул веществ по валентности; формируется понятие «коэффициент» и умение расставлять коэффициенты в уравнении химической реакции. Учитель дает учащимся алгоритм расстановки коэффициентов в уравнениях химических реакций на примере реакции горения красного фосфора.
Порядок выполнения операций
Пример
1. В левой части уравнения записать исходные вещества, в правой - продукты реакции (молекулы газов водорода, хлора, кислорода, азота состоят из двух атомов)
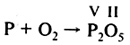
2. Определить число атомов каждого элемента в левой и правой частях схемы реакции
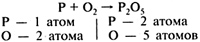
3. Среди элементов с разным числом атомов до и после реакции выбрать тот, число атомов которого больше
O - 2 атома слева
O - 5 атомов справа
4. Найти наименьшее общее кратное (НОК) числа атомов этого элемента в левой части уравнения и числа атомов этого элемента в правой части уравнения
НОК - 10
5. Разделить НОК на число атомов этого элемента в левой части уравнения, получив коэффициент для левой части уравнения
10 : 2 = 5
P + 5O2  P2O5
P2O5
6. Разделить НОК на число атомов этого элемента в правой части уравнения, получив коэффициент для правой части уравнения
10 : 2 = 5
P + 5O2  2P2O5
2P2O5
7. Необходимо подсчитать число атомов других элементов в левой и правой частях уравнения и с помощью коэффициентов уравнять их, т. е. число атомов каждого элемента в левой и правой частях уравнения должно быть одинаковым
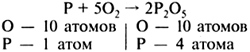
В левую часть уравнения перед фосфором необходимо поставить коэффициент 4.
4P + 5O2  2P2O5
2P2O5
Для закрепления умения записывать химические уравнения можно вызывать учащихся к доске и упражняться в расстановке коэффициентов в уравнениях химических реакций.
Этот урок можно провести, руководствуясь уроком 25 в электронном пособии «Электронная библиотека "Просвещение". Химия. 8 класс».
Домашнее задание. § 12, упр. 1-4 (с. 47).


