- Преподавателю
- Химия
- Задачи с экологическим содержанием
Задачи с экологическим содержанием
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Загравская Е.В. |
| Дата | 27.04.2014 |
| Формат | docx |
| Изображения | Есть |
Решение задач с экологическим содержанием
Карточка 1
1Задача. Накопление углекислого газа в атмосфере становится опасным загрязнением - приводит к парниковому эффекту. Какой объем CO2 попадает в атмосферу при сжигании 100 г полиэтилена (100 шт. использованных пакетов)?
2Задача. В солнечный день листья растений общей площадью 1м3 за 3,3 часа поглощают 5г оксида углерода (IV) Рассчитайте, площадь листьев, необходимых для поглощения оксида углерода (IV), который выделится при сжигании 1м3 природного газа, содержащего 95% метана, 4% этана и бутан.
Решение задач с экологическим содержанием
Карточка 2
3. Задача. На нефтеперерабатывающем заводе из-за поломки произошел аварийный сброс нефтепродуктов в ближайшее озеро. Масса сброшенных нефтепродуктов составила 500 кг. Выживут ли рыбы, обитающие в озере, если известно, что примерная масса воды в озере 10000т. Токсическая концентрация нефтепродуктов для рыб составляет 0,05 мг/л.
4.Задача. В промышленности винилхлорид получают пиролизом дихлорэтана (1-я стадия):
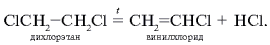
В настоящее время осуществлен сбалансированный (безотходный) синтез винилхлорида. Для этого выделяющийся при пиролизе HCl смешивают с этиленом и кислородом, а затем эту смесь подвергают окислительному хлорированию в присутствии катализатора хлорида меди(II) CuCl2 на носителе (2-я стадия):
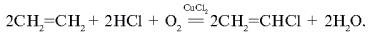
Рассчитайте объем НСl (н. у.), выделившегося при пиролизе 19,8 кг дихлорэтана, и массу винилхлорида, полученного при сбалансированном синтезе. Какой объем займет этилен (н. у.), необходимый для второй стадии процесса? Оцените новую технологию получения винилхлорида с позиции защиты окружающей среды от загрязнения.
Решение задач с экологическим содержанием
Карточка 3
5Задача. Рассчитайте объем СО2, возвращенного в круговорот углерода в результате деятельности метанокисляющих бактерий, если ими было утилизировано из воздуха 4,8 т СН4. Процесс биологического окисления метана идет ступенчато: СН4 -СН3ОН -НСНО - НСООН - СО2.
6Задача. Котельная сжигает 2т каменного угля в сутки. Состав угля: С -84%,Н - 5%, Н2О - 5%, S -3,5%, негорючие примеси - 2,5% по массе. Учитывая, что 1 га леса дает в сутки 10кг кислорода, вычислите, с какой площади будет восполняться расходуемый на сжигание кислород
Ответы.
1.1 Решение:
С2 Н4 +3О2 = 2С О2 + 2Н2О
М( С2 Н4 ) =28 г/моль;
Составляем пропорцию: из 100г ---------- х л
28г ------------ 44,8 л;
Ответ: х = 160 л
2.2Решение. Уравнения реакций сгорания смеси газов:
СН4 +2О2 = CO2 +2Н2О
2С2 Н6 +7О2 = 4С О2 + 6Н2О
2С4Н10 +13О2 = 8С О2 + 10Н2О
1м3 составляет 100%, значит, в смеси содержится 0,95 м3 метана, 0,04 м3 этана и 0,01 м3 бутана.
По уравнениям реакций рассчитываем объем углекислого газа.
0,95 м3 ------ х м3
1 м3 -------- 2 м3 х =1,9 м3
0,04 м3 ---------- yм3
2 м3 --------- 4 м3 y =0,08м3
100% -99% =1%
0,01 м3 ---------- zм3
2 м3 --------- 8 м3 z= 0,04 м3
Объем углекислого газа : 1,9 +0,08+0,04=2,02 м3
1 м3 -1000л х=2020
2,02м3 - х л
Находим количество вещества углекислого газа: 2020/22,4=90,17 моль
Массу углекислого газа находим по формуле: m=90,17 х 44 =3367,5г
Если листья растений общей площадью 1м3 за 3,3 часа поглощают 5г оксида углерода (IV) , то 3367,5/5 =733,5 м3
Ответ: площадь листьев, необходимых для
3.3 Решение
1 тонна - 1000кг
10 000 тонн - 10 000 000 кг (10 000 000л)
В 1кг -1000г, в 1г -1000мг,
500кг - 500 000 000мг,
500 000 000/10 000 000 =50мг/л
Ответ: Токсическая концентрация нефтепродуктов для рыб в 1000 раз превышает допустимые нормы.
4.4 Решение: Найдем молярную массу винилхлорида и дихлорэтана.
М (С2 Н4Cl2 ) =99г/моль; М (С2 Н3Cl ) =62,5г/моль
Количество вещества дихлорэтана 19800/99=200 моль
Количество вещества НCl также равно 200моль, объем: 200х 22,4 =4480л.
При сбалансированном синтезе количество вещества винилхлорида и этилена равно количеству вещества хлорводорода и составляет 200моль каждый из них. Этилен займет объем 200х 22,4 =4480л. Масса винилхлорида 62,5х 200=12500г, 12,5кг. Получения винилхлорида сбалансированным (безотходным) синтезом винилхлорида выгодно с позиции защиты окружающей среды от загрязнения, потому что происходит его утилизация.
5.5 Решение : 4,8т =48х105 г
М(СН4) =16г/моль;
Составим пропорцию: 48х105 --------- хл х=6,72х105 л
16 ----------- 22,4л
Ответ: объем СО2, возвращенного в круговорот углерода равен 6,72х105 л
6.6 Решение:
2т = 2000кг, 2000кг- 100%
х кг С - 84% х=4480кг С в составе угля.
Таким же образом рассчитываем массу Н, S
2000кг- 100%
х кг Н - 5% х= 100кг Н
2000кг- 100%
х кг S - 3,5% х =70кг
запишем уравнения реакции горения: С + О2 =СО2
найдем количество вещества углерода: 4480/12 =373,3 моль, тогда масса кислорода, идущего на взаимодействие с углеродом равна: 373,3 х 32=11946,6 кг;
также высчитываем массы кислорода, идущие на взаимодействие с водородом и с серой.
2Н2 +О2 = 2Н2О 100/2=50моль, кислорода необходимо в два раза меньше, -25 моль, 25х32=800кг.
S + О2 = SО2 Молярные массы серы и кислорода равны, следовательно, кислорода для реакции необходимо 70кг. Найдем общую массу кислорода: 11946,6 +800 + 70=1281,6кг.
Составим пропорцию: 1га леса дает в сутки 10кг
х га - 1281,6 кг; х =128.16га
Ответ: будет восполняться расходуемый на сжигание кислород с 128.16га леса.
поглощения оксида углерода (IV), равна733,5 м3


