- Преподавателю
- Химия
- Методическаяч разработка для самостоятельной работы по теме Типы гибридизации
Методическаяч разработка для самостоятельной работы по теме Типы гибридизации
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Веде И.В. |
| Дата | 14.08.2015 |
| Формат | doc |
| Изображения | Есть |
ГОСУДАРСТВЕННОЕ АВТОНОМНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
СРЕДНЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ НОВОСИБИРСКОЙ ОБЛАСТИ
«КУПИНСКИЙ МЕДИЦИНСКИЙ ТЕХНИКУМ»
МЕТОДИЧЕСКОЕ ПОСОБИЕ
«Типы гибридизации атома углерода»
для самостоятельной работы студентов
по дисциплине Химия
Раздел: Органическая химия
Тема: Предмет органической химии.
Теория строения органических соединений
Специальность: 34.02.01 «Сестринское дело» 1 курс
Купино
2015 учебный год
Рассмотрена на заседании
предметно - цикловой методической комиссии по
общеобразовательным дисциплинам, общему гуманитарному и
социально - экономическому, математическому
и естественнонаучному циклу
Протокол от 2015 г.
Председатель ______________ /__________________/
Автор - составитель: преподаватель химии высшей категории
Веде Ирина Викторовна
Пояснительная записка к методическому пособию
Методическое пособие предназначено для углубленного изучения темы «Типы гибридизации атома углерода».
Практика показывает, что многие обучающиеся затрудняются при определении типов гибридизации атомов углерода и видов химической связи при изучении органических соединений.
Цель пособия - помочь обучающимся научиться определять типы гибридизации атомов углерода и виды химической связи в органических соединениях.
Данное пособие рекомендовано для студентов 1 курса специальности 34.02.01 Сестринское дело. Пособие содержит теоретический материал по теме, таблицы для систематизации знаний, упражнения для самостоятельной работы и развернутые ответы по каждому из заданий.
Пособие направлено на формирование навыков самостоятельной работы с учебным материалом, осуществления поиска и использования информации, формирование и развитие творческого потенциала, повышение интереса к дисциплине.
Я всегда готов учиться,
но мне не всегда нравится,
когда меня учат
У. Черчилль
Типы гибридизации атома углерода
Электронное строение атома углерода в основном состоянии 1s22s22р2, на р-орбиталях 2-го уровня находятся два неспаренных элекетрона. Это позволяет атому углерода образовать по обменному механизму только две ковалентные связи. Однако во всех органических соединениях углерод образует четыре ковалентные связи, что становится возможным в результате гибридизации атомных орбиталей.
Гибридизация - это взаимодействие атомных орбиталей с близкими значениями энергии, сопровождающееся образованием новых 'гибридных' орбиталей.
Гибридизация - процесс, требующий затрат энергии, но эти затраты с избытком компенсируются за счет энергии, выделяющейся при образовании большего числа ковалентных связей. образующиеся 'гибридные' орбитали имеют форму ассимметричной гантели и резко отличаются от исходных орбиталей атома углерода.
Для атома углерода возможно три типа гибридизации: sр3-гибридизация - взаимодействующие орбитали показаны синими стрелками:
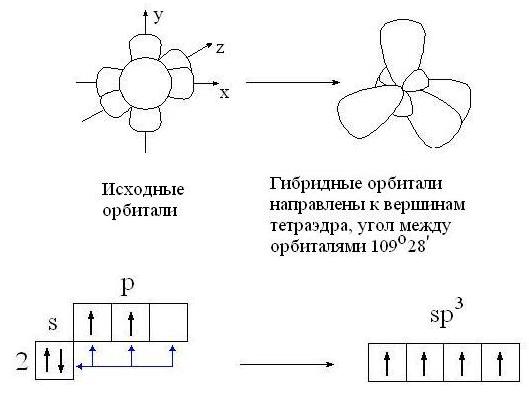
sр2-гибридизация:
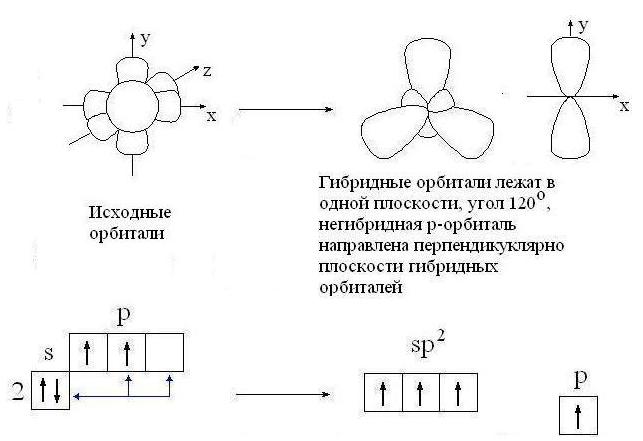
sр-гибридизация:
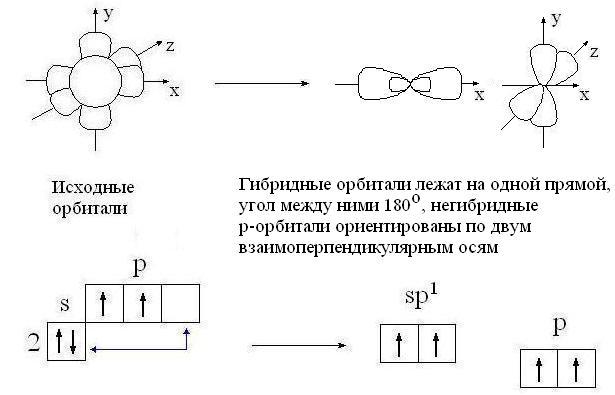
Гибридные орбитали атома углерода способны участвовать в образовании только 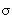 -связей, незатронутые гибридизацией р-орбитали образуют только
-связей, незатронутые гибридизацией р-орбитали образуют только 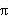 -связи. Именно этой особенностью определяется пространственное строение молекул органических веществ.
-связи. Именно этой особенностью определяется пространственное строение молекул органических веществ.
Гибридизация
атомных орбиталей углерода
Ковалентная химическая связь образуется при помощи общих связывающих электронных пар по типу:
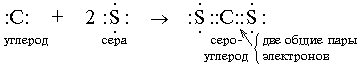
Образовывать химическую связь, т.е. создавать общую электронную пару с «чужим» электроном от другого атома, могут только неспаренные электроны. Неспаренные электроны при записи электронных формул находятся по одному в клетке-орбитали.
Атомная орбиталь - это функция, которая описывает плотность электронного облака в каждой точке пространства вокруг ядра атома. Электронное облако - это область пространства, в которой с высокой вероятностью может быть обнаружен электрон.
Для согласования электронного строения атома углерода и валентности этого элемента пользуются представлениями о возбуждении атома углерода. В нормальном (невозбужденном) состоянии атом углерода имеет два неспаренных 2р2-электрона. В возбужденном состоянии (при поглощении энергии) один из 2s2-электронов может переходить на свободную р-орбиталь. Тогда в атоме углерода появляется четыре неспаренных электрона:

Напомним, что в электронной формуле атома (например, для углерода 6С - 1s22s22p2) большие цифры перед буквами - 1, 2 - обозначают номер энергетического уровня. Буквы s и р указывают форму электронного облака (орбитали), а цифры справа над буквами говорят о числе электронов на данной орбитали. Все s-орбитали сферические:
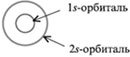
На втором энергетическом уровне кроме 2s-орбитали имеются три 2р-орбитали. Эти 2р-орбитали имеют эллипсоидную форму, похожую на гантели, и ориентированы в пространстве под углом 90° друг к другу. 2р-Орбитали обозначают 2рх, 2рy и 2рz в соответствии с осями, вдоль которых эти орбитали расположены.
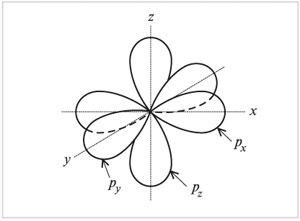
Форма и ориентация
р-электронных орбиталей
При образовании химических связей электронные орбитали приобретают одинаковую форму. Так, в предельных углеводородах смешиваются одна s-орбиталь и три р-орбитали атома углерода с образованием четырех одинаковых (гибридных) sр3-орбиталей:
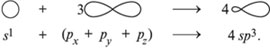
Это - sр3-гибридизация.
Гибридизация - выравнивание (смешивание) атомных орбиталей (s и р) с образованием новых атомных орбиталей, называемых гибридными орбиталями.
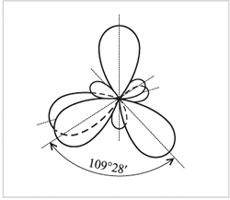
Четыре sp3-гибридные орбитали
атома углерода
Гибридные орбитали имеют асимметричную форму, вытянутую в сторону присоединяемого атома. Электронные облака взаимно отталкиваются и располагаются в пространстве максимально далеко друг от друга. При этом оси четырех sр3-гибридных орбиталей оказываются направленными к вершинам тетраэдра (правильной треугольной пирамиды).
Соответственно углы между этими орбиталями - тетраэдрические, равные 109°28'.
Вершины электронных орбиталей могут перекрываться с орбиталями других атомов. Если электронные облака перекрываются по линии, соединяющий центры атомов, то такую ковалентную связь называют сигма(![]() )-связью. Например, в молекуле этана С2Н6 химическая связь образуется между двумя атомами углерода перекрыванием двух гибридных орбиталей. Это
)-связью. Например, в молекуле этана С2Н6 химическая связь образуется между двумя атомами углерода перекрыванием двух гибридных орбиталей. Это 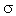 -связь. Кроме того, каждый из атомов углерода своими тремя sр3-орбиталями перекрывается с s-орбиталями трех атомов водорода, образуя три
-связь. Кроме того, каждый из атомов углерода своими тремя sр3-орбиталями перекрывается с s-орбиталями трех атомов водорода, образуя три 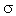 -связи.
-связи.
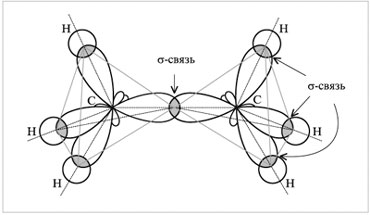
Схема перекрывания электронных облаков
в молекуле этана
Всего для атома углерода возможны три валентных состояния с различным типом гибридизации. Кроме sр3-гибридизации существует sр2- и sр-гибридизация.
sр2-Гибридизация - смешивание одной s- и двух р-орбиталей. В результате образуются три гибридные sр2-орбитали. Эти sр2-орбитали расположены в одной плоскости (с осями х, у) и направлены к вершинам треугольника с углом между орбиталями 120°. Негибридизованная
р-орбиталь перпендикулярна к плоскости трех гибридных sр2-орбиталей (ориентирована вдоль оси z). Верхняя половина р-орбитали находится над плоскостью, нижняя половина - под плоскостью.
Тип sр2-гибридизации углерода бывает у соединений с двойной связью: С=С, С=О, С=N. Причем только одна из связей между двумя атомами (например, С=С) может быть 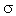 -связью. (Другие связывающие орбитали атома направлены в противоположные стороны.) Вторая связь образуется в результате перекрывания негибридных р-орбиталей по обе стороны от линии, соединяющей ядра атомов.
-связью. (Другие связывающие орбитали атома направлены в противоположные стороны.) Вторая связь образуется в результате перекрывания негибридных р-орбиталей по обе стороны от линии, соединяющей ядра атомов.
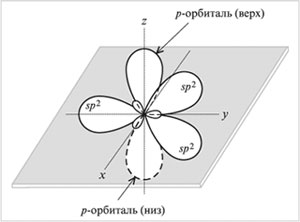
Орбитали (три sp2 и одна р)
атома углерода в sp2-гибридизации
Ковалентная связь, образующаяся путем бокового перекрывания р-орбиталей соседних углеродных атомов, называется пи( )-связью.
)-связью.
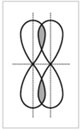
Образование
![]() -связи
-связи
Из-за меньшего перекрывании орбиталей  -связь менее прочная, чем
-связь менее прочная, чем 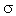 -связь.
-связь.
sр-Гибридизация - это смешивание (выравнивание по форме и энергии) одной s- и одной
р-орбиталей с образованием двух гибридных sр-орбиталей. sр-Орбитали расположены на одной линии (под углом 180°) и направлены в противоположные стороны от ядра атома углерода. Две
р-орбитали остаются негибридизованными. Они размещены взаимно перпендикулярно
направлениям ![]() -связей. На рисунке sр-орбитали показаны вдоль оси y, а негибридизованные две
-связей. На рисунке sр-орбитали показаны вдоль оси y, а негибридизованные две
р-орбитали- вдоль осей х и z.
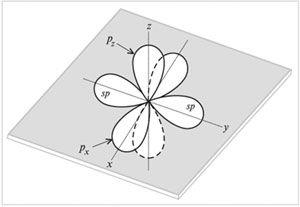
Атомные орбитали (две sp и две р)
углерода в состоянии sp-гибридизации
Тройная углерод-углеродная связь С С состоит из
С состоит из 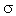 -связи, возникающей при перекрывании
-связи, возникающей при перекрывании
sp-гибридных орбиталей, и двух  -связей.
-связей.
Взаимосвязь таких параметров атома углерода, как число присоединенных групп, тип гибридизации и типы образуемых химических связей, показана в таблице 4.
Ковалентные связи углерода
Число групп,
связанных
с углеродом
Тип
гибридизации
Типы
участвующих
химических связей
Примеры формул соединений
4
sp3
Четыре  - связи
- связи
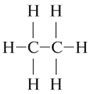
3
sp2
Три  - связи и
- связи и
одна  - связь
- связь
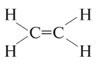
2
sp
Две 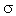 - связи
- связи
и две  -связи
-связи
H-C C-H
C-H
Упражнения.
1. Какие электроны атомов (например, углерода или азота) называют неспаренными?


2. Что означает понятие «общие электронные пары» в соединениях с ковалентной связью (например, СН4 или Н2S)?



3. Какие электронные состояния атомов (например, С или N) называют основными, а какие возбужденными?



4. Что означают цифры и буквы в электронной формуле атома (например, С или N)?



5. Что такое атомная орбиталь? Сколько орбиталей на втором энергетическом уровне атома Си чем они различаются?



6. В чем отличие гибридных орбиталей от исходных орбиталей, из которых они образовались?



7. Какие типы гибридизации известны для атома углерода и в чем они заключаются?


8. Нарисуйте картинку пространственного расположения орбиталей для одного из электронных состояний атома углерода.
9. Какие химические связи называют 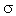 и какие
и какие ![]() ? Укажите
? Укажите ![]() - и
- и  -связи в соединениях:
-связи в соединениях:




10. Для атомов углерода приведенных ниже соединений укажите: а) тип гибридизации; б) типы его химических связей; в) валентные углы.
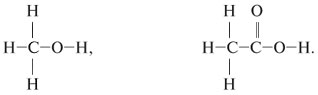



Ответы на упражнения
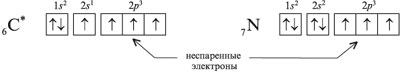
1. Электроны, которые находятся по одному на орбитали, называют неспаренными электронами. Например, в электронографической формуле возбужденного атома углерода - четыре неспаренных электрона, а у атома азота - три:
2. Два электрона, участвующие в образовании одной химической связи, называют общей электронной парой. Обычно до образования химической связи один из электронов этой пары принадлежал одному атому, а другой электрон - другому атому:
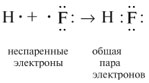
3. Электронное состояние атома, в котором соблюдается порядок заполнения электронных орбиталей: 1s2, 2s2, 2p2, 3s2, 3p2, 4s2, 3d2, 4p2 и т.д., называют основным состоянием. Ввозбужденном состоянии один из валентных электронов атома занимает свободную орбиталь с более высокой энергией, такой переход сопровождается разъединением спаренных электронов. Схематически это записывают так:
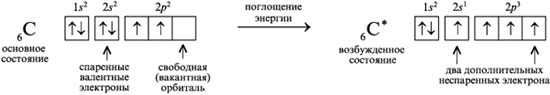
Тогда как в основном состоянии было только два валентных неспаренных электрона, то в возбужденном состоянии таких электронов становится четыре.
5. Атомная орбиталь - это функция, которая описывает плотность электронного облака в каждой точке пространства вокруг ядра данного атома. На втором энергетическом уровне атома углерода четыре орбитали - 2s, 2рx, 2рy, 2рz. Эти орбитали различаются:
а) формой электронного облака (s - шар, р - гантель);
б) р-орбитали имеют разную ориентацию в пространстве - вдоль взаимно перпендикулярных осей x, y и z, их обозначают рx, рy, рz.
6. Гибридные орбитали отличаются от исходных (негибридных) орбиталей формой и энергией. Например, s-орбиталь - форма сферы, р - симметричная восьмерка, sp-гибридная орбиталь - асимметричная восьмерка.
Различия по энергии: E(s) < E(sр) < E(р). Таким образом, sp-орбиталь - усредненная по форме и энергии орбиталь, полученная смешиванием исходных s- и p-орбиталей.
7. Для атома углерода известны три типа гибридизации: sp3, sp2 и sp (см. текст урока 5).
9. 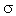 -связь - ковалентная связь, образующаяся путем лобового перекрывания орбиталей по линии, соединяющей центры атомов.
-связь - ковалентная связь, образующаяся путем лобового перекрывания орбиталей по линии, соединяющей центры атомов.
![]() -связь - ковалентная связь, образующаяся путем бокового перекрывания р-орбиталей по обе стороны от линии, соединяющей центры атомов.
-связь - ковалентная связь, образующаяся путем бокового перекрывания р-орбиталей по обе стороны от линии, соединяющей центры атомов.
![]() -Связи показывают второй и третьей черточкой между соединенными атомами.
-Связи показывают второй и третьей черточкой между соединенными атомами.
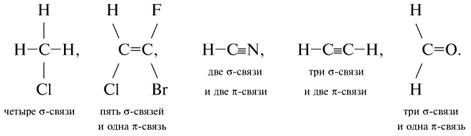
10.