- Преподавателю
- Химия
- Конспект урока на тему Соли
Конспект урока на тему Соли
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Хасанова С.С. |
| Дата | 09.01.2016 |
| Формат | docx |
| Изображения | Есть |
Хасанова Светлана Сайхановна
Учитель химии
Областная специальная школа-интернат №3
Г. Атырау
Тема урока: «Соли»
Цель урока: сформировать понятие «Соли», научить детей определять валентность кислотного остатка и составлять формулы солей.
Коррекционная задача урока: развивать логическое мышление, память, закреплять правильное произношение.
Воспитательная цель урока: воспитывать усидчивость, терпение, аккуратность.
Наглядность урока: таблица «Номенклатура солей», картинки, слайды, видеоматериал «Действие кислоты на металл»
Ход урока:
-
Организационный момент.
-
Повторение. Фронтальная беседа.
-
Что такое кислота?
-
Как кислота классифицируется?
-
Физическое свойство?
-
Химическое свойство?
А) Взаимодействие кислоты с металлом.
Б) Взаимодействие кислоты с основными оксидами.
В) Взаимодействие кислоты с основаниями.
III. Работа над новым материалом.
-
Соли.
-
Классификация солей.
-
Физическое свойство.
-
Химическое свойство.
-
Получение.
-
Применение.
1. Соли - это сложные вещества образованные атомами металлов и кислотными остатками.
-
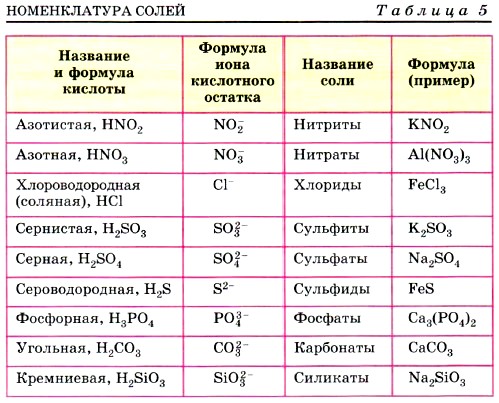
Ознакомление таблицей:
Соли соленой кислоты HCI
Соли азотной кислоты HNO3
Соли серной кислоты H2SO4
Соли угольной кислоты H2CO3
-
Игровая таблица (с помощью карточек вложить в карманчик нужные соли)
-
Металлы
Соли
Кислот
Хлоровод
Серной
Азотной
Фосфорной
Na
NaCI
Na2SO4
NaNO3
Na3PO3
2. Классификация солей.
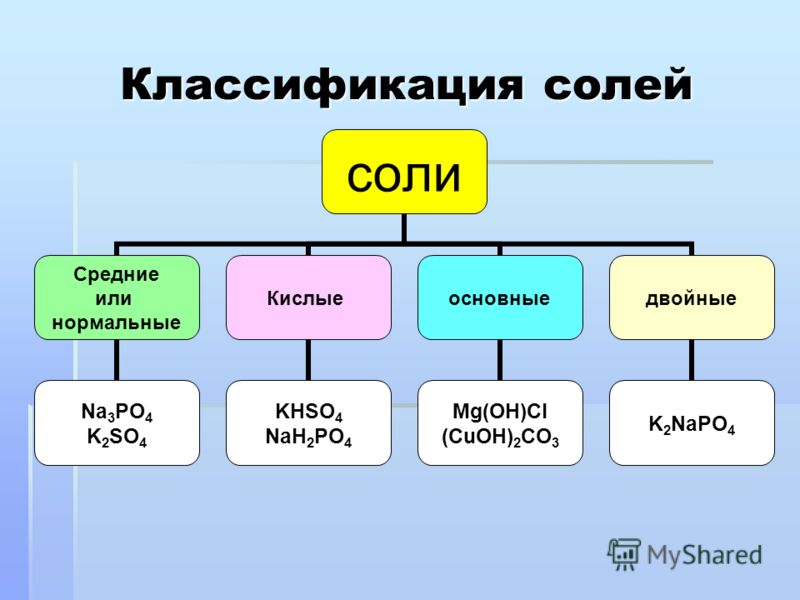
Средние соли, которые образуется при замещении атомами металлов всех атомов Na2 в молекулах кислот.
H3PO4+ 3NaOH = Na3PO4+ 3H2O ортофосфат натрия
Кислые соли, которые образуется в результате неполного замещения атомами металлов, атомов водорода в молекулах кислот.
H3PO4+ NaOH = NaH2PO4+ H2O ортогидрофосфат натрия
Основные соли, в молекулах которых, кроме кислотных остатков имеются гидросогруппы
Mg(OH)2 + HCI = MgOHCI + H2O Основной хлорид магия
Двойные соли, которые образуется при замещении атомов H2 в молекулах кислот двумя различными металлами.
H2PO4 + KOH + NaOH - >KNaPO4+ H2O
3.Физическое свойство: твердое, кристаллическое вещество растворимость различия.
4. Химическое свойство:
1. Соли реагирует с металлами
2. Соли реагирует с кислотами
3. Соли реагирует с щелочами
5. Получение: действие кислоты на металл. Видеоматериал
2H2PO4+6Na=2 Na2PO4 +3H2 ортофосфат калия
Кислотные оксиды со щелочами
N2O5 + Ca (NO3)2+ H2O
6. Применение: применяют в быту поваренную соль NaCI, ортофосфат калий натрия применяют в виде минеральных удобрении.


III. Закрепление. Используя таблицы, составьте формулы солей и назовите их.
IV. Тест
1. Из приведенных формул выпишите кислотных оксидов.
2. Закончи уравнение реакции.
3. Из приведенных формул выпишите отдельно соли.
4. Написать название солей.
5. Напишите формулы кислот;
Хлорная кислота, фосфорная кислота, азотное кислота, бромное кислота.
6. Из этих элементов напишите формул оксидов
Ae, Fe, Ce, S, Na, P, Mg, I
V. Домашнее задание. Создать презентацию на тему «Классификация солей»


