- Преподавателю
- Химия
- Инструкция к практической работе «Получение аммиака, изучение свойств водного раствора аммиака и солей аммония»
Инструкция к практической работе «Получение аммиака, изучение свойств водного раствора аммиака и солей аммония»
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Обичкина А.М. |
| Дата | 13.02.2015 |
| Формат | doc |
| Изображения | Есть |
Инструкция к практической работе № 2 «Получение аммиака, изучение свойств водного раствора аммиака и солей аммония».
Цель
Реактивы и оборудование
Ход работы
Наблюдения
Выводы, уравнения
-
Получить аммиак
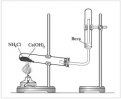
Рис.1 Установка для получения аммиака
Лист бумаги, ложечка, пробирка с газоотводной трубкой, штатив, горелка, спички, 2 пробирки, чашка с водой, фенолфталеин, хлорид аммония, шпатель.
На листе бумаги смешать 1 ложечку гидроксида кальция, 2ложечки хлорида аммония. Поместить полученную смесь в пробирку, закрепленную в штативе, закрыв пробирку газоотводной трубкой, как показано на рис.1 Смесь 1агревать осторожно, соблюдая ТБ.
При нагревании смеси (гидроксида кальция и хлорида аммония) выделяется газ - аммиак, с резким запахом.
-
Напишите уравнение получения аммиака, укажите условия проведения реакции.
-
Как нужно расположить пробирку для собрания NН3? (сравните относительную молекулярную массу NН3 и Мr воздуха )
-
Как 2 способами можно обнаружить аммиак?
2) Растворение аммиака в воде
1)Пробирку с собранным NН3 снять с газоотводной трубки, держа вверх дном. Закрыть отверстие пробирки большим пальцем и опустить отверстием вниз в чашку с водой.
2) Закрыв пробирку под водой пальцем , вынуть ее из чашки вместе с вошедшей в нее водой и сделайте пробу фенолфталеином.
Вода быстро поднимается вверх. При добавлении фенолфталеина раствор окрасился в малиновый цвет.
-
Напишите уравнения реакции взаимодействия NН3 с водой.
-
Почему поднялся уровень воды в пробирки?
-
Какую окраску приобрел фенолфталеин?
-
Какую среду имеет полученный раствор?
3) Термическое разложение хлорида аммония
В пробирку шпателем поместить хлорид аммония и пробирку нагреть, до исчезновения соли из пробирки.
Выделяется газ с резким запахом - аммиак.
-
Почему исчезла соль?
-
Напишите уравнение прошедшей реакции, укажите условия ее проведения.
Мысленный эксперимент
? Выберите из предложенных веществ те, из которых можно получить аммиак реакцией разложения: NH4Cl, NO2, NH4OH, NaNO3, K3N.
? Запишите уравнения этих реакций. Какие условия необходимы для их осуществления?
? Как можно получить гидроксид аммония? Допишите уравнения реакции.
? + NaOH = NH4OH + ?
? + Н2О = NH4OH
Проверь себя!
-
Отметьте правильный ответ
1. Для аммиака характерны свойства: 3. Цвет лакмуса в растворе аммиака:


кислот
солей
оксидов
оснований

красный
синий




фиолетовый
бесцветный
2. Аммиак взаимодействует с 4. Аммиак-восстановитель в реакции с




щелочами
неметаллами
металлами
кислотами



металлами
неметаллами
кислотами
Оксидами металлов


