- Преподавателю
- Химия
- Урок по химии на тему
Урок по химии на тему
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Кривоносова И.П. |
| Дата | 12.01.2015 |
| Формат | doc |
| Изображения | Есть |
Муниципальное казенное общеобразовательное учреждение Кривоносовская СОШ
Урок по химии в 10 классе
«Сложные эфиры»
Учитель химии IКК
Кривоносова Ирина Павловна
2013г
Это урок изучения нового материала (10 класс) с элементами исследования. На нем использованы методы беседы, практического исследования, приемы сравнения и анализа. Урок сопровождается презентацией.
Цели урока: рассмотреть строение и виды изомерии сложных эфиров. Познакомить учащихся с номенклатурой этого класса соединений. Изучить особенности реакций этерификации и гидролиза сложных эфиров. Рассказать о распространённости сложных эфиров в природе. Развивать умения анализировать, исследовать, формировать аналитическое мышление, воспитывать внимательность, аккуратность.
Оборудование и реактивы: шаростержневые модели молекул сложных эфиров, безводный ацетат натрия, этиловый спирт, концентрированная серная кислота, спиртовка, пробиркодержатель, мультимедийный проектор, компьютер.
Девиз урока: «Может тот, кто думает, что может».
Ход урока.
-
Вступительное слово учителя. На экране появляется слайд №1 с девизом и темой урока, учащиеся записывают тему урока в тетрадь.
Учитель предлагает учащимся сформулировать определение сложных эфиров по формуле: (слайд №2). Учащиеся записывают общую формулу сложных эфиров и предлагают определение, исходя из практической работы «Карбоновые кислоты», где был получен сложный эфир.

 O
O
R - C - O - R1
Учитель предлагает учащимся демонстрационный эксперимент по получению сложного эфира. (В практической работе был получен изоамиловый эфир уксусной кислоты - запах грушевой эссенции). В данном эксперименте помещаем в пробирку немного ацетата натрия, добавляем несколько капель этилового спирта и 2 капли концентрированной серной кислоты. Пробирку осторожно нагреваем над пламенем горелки. Через несколько секунд появляется освежающий запах. Данный запах применяют как отдушку в производстве мыла.
Учитель предлагает учащимся ответить на вопросы:
- Назовите формулу сложного эфира, который был получен при взаимодействии уксусной кислоты и этилового спирта?
(Этиловый эфир уксусной кислоты.)
- Откуда в смеси появилась уксусная кислота?
(При взаимодействии ацетата натрия и серной кислоты.) (Слайд №3)
-
Номенклатура сложных эфиров.
Учитель объясняет учащимся принцип построения названий сложных эфиров.
- По систематической номенклатуре названия сложных эфиров образуются путем прибавления к названию аниона кислоты и приставки, с названием углеводородного радикала спирта. Название аниона кислоты оканчивается на -ат или -оат. Например: метилацетат, этилформиат.
Названия сложным эфирам дают по названию кислот и спиртов, из которых они образованы. Часто названия соединений данного класса
составляют из названий углеводородных радикалов, образующих спирт и названий кислотных остатков. Метиловый эфир уксусной кислоты, этиловый эфир муравьиной кислоты. (Слайд №4)
-
Изомерия сложных эфиров. (Слайд №5)
-
Общая формула сложных эфиров СnH2nO2
-
Такая же формула у предельных одноосновных карбоновых кислот, значит есть межклассовая изомерия
-
Изомерия сложных эфиров связана с изомерией УВ радикалов кислот и спиртов, входящих в состав эфиров - изомерия углеродного скелета
Учитель предлагает учащимся составить структурные формулы изомерных соединений состава С3Н6О2, дать названия изомерам и указать вид изомерии. (Слайд №6)
Учащиеся составляют структурные формулы сложных эфиров: этилформиат и метилацетат - изомерия углеродного скелета; пропионовая кислота - межклассовая изомерия.

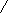

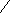
 О О О
О О О
Н
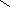
 - С СН3 - С СН3 - СН2 - С
- С СН3 - С СН3 - СН2 - С
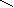 О - СН2 - СН3 О - СН3 О - ОН
О - СН2 - СН3 О - СН3 О - ОН
Этиловый эфир муравьиной Метиловый эфир уксусной Пропионовая кислота
кислоты (этилформиат) кислоты (метилацетат)
-
Особенности реакций этерификации и гидролиза сложных эфиров.
Учитель напоминает учащимся по какой реакции могут быть получены сложные эфиры. (Слайд №7)
Реакции взаимодействия кислот и спиртов, при которых образуется сложный эфир и вода, называются реакцией этерификации ,от лат. «этер»,что в переводе означает «эфир».


 О Н+ О
О Н+ О
C
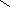
 H3-C + HO-C2H5 CH3-C + H2O
H3-C + HO-C2H5 CH3-C + H2O
ОН O-C2H5
Особенности реакции этерификации:
1.Обратима
2.Протекает в присутствии ионов Н+(ускоряет оба противоположно направленных процесса: как прямой, так и обратный)
3.От кислоты отщепляется группа ОН-
Долгое время ученые предполагали, что при взаимодействии кислот со спиртами водород должен отщепляться от молекулы кислоты, а гидроксильная группа - от молекулы спирта.
Однако при помощи изотопа кислорода с атомной массой 18 ученым удалось установить, что гидроксильная группа отщепляется от молекулы карбоновой кислоты. (Слайд №8)
Противоположный процесс реакции этерификации называется гидролиз сложного эфира. (Слайд №9)
Особенности данного типа реакций: гидролиз сложных эфиров протекает как в кислой, так и в щелочной среде.
Кислотный гидролиз
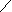


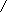 O H+ O
O H+ O
R

 1- C + H2O R1- C + HO - R2
1- C + H2O R1- C + HO - R2
 R2OH
R2OH
Щелочной гидролиз
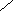

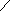
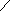 O Н2О O
O Н2О O
R

 1- C + NaOH R1- C + HO - R2
1- C + NaOH R1- C + HO - R2
О - R2 ONa
*Учитель ставит перед учащимися задачу: используя знания по смещению химического равновесия выбрать условия выполнения реакции этерификации.
Задача первая: Смещение химического равновесия реакции этерификации в сторону образования сложного эфира.
Ответы учащихся: повысить концентрацию реагентов - кислоты и спирта, тем самым увеличить скорость прямой реакции, удалить полученные в результате реакции продукты - воду и эфир (уменьшаем концентрации этих веществ, соответственно снижаем скорость реакции с их участием).
Учащиеся делают краткую запись в тетради.
Задача вторая: Смещение химического равновесия реакции гидролиза сложного эфира в сторону образования спирта и кислоты.
Учитель объясняет учащимся, что при кислотном гидролизе для смещения химического равновесия в сторону образования спирта и кислоты добавляется избыток воды. На каком принципе основан этот метод смещения равновесия?
Ответы учащихся: Скорость реакции зависит от концентрации реагирующих веществ. Чем больше концентрация воды, тем быстрее протекает гидролиз сложного эфира.
Учитель обращает внимание учащихся, что при щелочном гидролизе происходит «связывание» кислоты, которая переходит в соль. Соли и спирты не взаимодействуют между собой, поэтому реакция необратима. Щелочь в реакции не катализатор, а расходный материал. В результате получаются соль карбоновой кислоты и спирт:
 R1COOR2 + NaOH R1COONa + R2OH
R1COOR2 + NaOH R1COONa + R2OH
Таким образом, количество добавленной кислоты в ходе реакции не изменяется, в случае кислотного гидролиза расходуется вода, а в случае щелочного гидролиза расходуется щелочь, но не вода.
-
Распространение сложных эфиров в природе.
Сложные эфиры входят в состав эфирных масел растений, придавая им цветочный или фруктовый аромат. (Слайд №10)
Важнейшими представителями сложных эфиров являются жиры.
Сложные эфиры высших карболовых кислот и высших спиртов называют восками. (Слайд №11)
-
Свойства сложных эфиров. (Слайд №12)
Физические свойства: бесцветные жидкости, нерастворимые в воде и обладающие невысокими температурами кипения.
Многие эфиры имеют приятный запах и являются хорошими растворителями органических веществ. В воде растворимы только сложные эфиры с небольшой относительной молекулярной массой.
Химические свойства: гидролиз сложных эфиров.
-
Применение сложных эфиров. Самостоятельная работа учащихся с учебником. (Итоги на слайде №13).
-
Подведение итогов урока. Организация процесса рефлексии. Учитель предлагает учащимся ответить на вопросы и выполнить задания в тетради.
Задания: (Слайды №14,15)
-
Назовите сложные эфиры по предложенной формуле.
-
Какие вещества называют сложными эфирами? Составьте 3 примера реакций их образования.
-
Какой вид изомерии характерен для сложных эфиров? Напишите формулы 2-3 изомеров для вещества С5Н10 О2 и дайте названия.
-
Приведите уравнения реакций получения этилформиата, пентилацетата, метилакрилата.
-
Установите соответствие между реагентами и типом реакции.
Реагенты Тип реакции
А) C2Н2 + Н2О 1) Гидролиз
Б) CaC2 + Н2О 2)Гидратация
В) CH3COOH + CH3OH 3) Гидрирование
Г) CH3CHO + Н2 4) Галогенирование
5) Этерификация
Домашнее задание:§21, д/з может быть направлено как на индивидуальные задания для учащихся, так и для класса. Можно предложить задание такого типа: Напишите уравнения реакций, с помощью которых можно осуществить превращения, укажите условия протекания реакций, определите вещество Х.
C
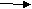
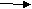
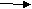 aC2 X CH3CHO C2H5OH CH3CHO
aC2 X CH3CHO C2H5OH CH3CHO
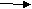
 CH3COOH CH3COOCH3CH3OH.
CH3COOH CH3COOCH3CH3OH.


