- Преподавателю
- Химия
- Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Белоусова Ю.А. |
| Дата | 08.10.2015 |
| Формат | docx |
| Изображения | Есть |
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области
Государственное автономное профессиональное образовательное учреждение Саратовской области
«САРАТОВСКИЙ ОБЛАСТНОЙ ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ТЕХНИКУМ»
Структурное подразделение «Отделение нефтегазохимической отрасли»
«Согласовано»
Рябухова Татьяна Олеговна,
доцент кандидат химических наук Энгельсского технологического института СГТУ ____________________________
«23» апреля 2015 г.
«Утверждено»
Верина Людмила Васильевна,
Руководитель Структурного подразделения
«Отделение нефтегазохимической отрасли» ГАПОУ СО «СОХТТ»
_______________________
«23» апреля 2015 г.
Вопросы, задания и критерии оценок
теоретического и практического туров Олимпиады
для студентов 1 и 2 курсов разработаны
Белоусовой Юлией Александровной, преподавателем химических дисциплин высшей категории Государственного автономного профессионального образовательного учреждения Саратовской области «Саратовский областной химико-технологический техникум» Структурное подразделение «Отделение нефтегазохимической отрасли»
Саратов, 2015
-
Общие положения
Настоящее Положение разработано в соответствии с:
-
Федеральным законом Российской Федерации от 29 декабря 2012 г. N 273-ФЗ "Об образовании в Российской Федерации"
-
Приказом Министерства образования и науки Российской Федерации (Минобрнауки России) от 14 июня 2013 г. N 464 г. Москва "Об утверждении Порядка организации и осуществления образовательной деятельности по образовательным программам среднего профессионального образования"
-
Областная олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области (в дальнейшем - Олимпиада) проводится в ГАПОУ СО «Саратовский областной химико-технологический техникум» Структурное подразделение «Отделение нефтегазохимической отрасли».
-
Цели и задачи Олимпиады
-
Олимпиада представляет собой очные соревнования, проводимые в течение определенного периода, предусматривающие выполнение конкретных заданий с последующей оценкой качества, времени и других критериев и завершающиеся церемонией чествования победителей.
-
Олимпиада призвана способствовать повышению качества химического образования в интересах развития личности и ее творческих способностей. Проводится в целях определения уровня подготовки специалистов в области химических наук, закрепления и углубления знаний и умений, полученных в процессе теоретического, практического обучения, стимулирования творческого роста, выявления наиболее одаренных и талантливых студентов по химическим дисциплинам.
-
Основными задачами Олимпиады являются:
-
- повышение творческой активности студентов;
- популяризация знаний по химии;
- творческий обмен опытом в области химического образования;
- создание условий для творческой самореализации личности специалистов;
- совершенствование навыков самостоятельной работы студентов и повышение ответственности за выполненную работу;
- повышение престижа образовательных учреждений.
-
Организация и проведение Олимпиады
-
Олимпиада проводится среди студентов 1 и 2-х курсов.
-
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
Критерии оценок для теоретических туров
-
Теоретический тур (тест)
-
Максимальное количество баллов - 20 баллов
1.2 Оценка результатов осуществляется с помощью компьютерной программы автоматически.
-
Теоретический тур (решение задач)
2.1 Максимальное количество баллов: 1 курс - 24, 2 курс - 34.
2.2 При равенстве баллов дополнительный балл присуждается работе, в которой написаны уравнения реакций веществ с применением развернутых структурных формул.
-
Практический тур (выполнение эксперимента)
3.1 Максимальное количество баллов - 30 баллов
3.2 Оценка этапов задания:
-
Соблюдение правил техники безопасности - 3 балла
-
Выбор оптимального пути решения - 5 баллов
-
Определение вещества - по одному баллу за каждое вещество - 4 балла
-
Пояснения к опыту и составление уравнений реакций - по баллу за каждое пояснение и уравнение - максимально 8 баллов.
-
Баллы снижаются за:
4.1 нарушение техники выполнения эксперимента - 1 балл за одну ошибку
4.2 небрежность выполнения записей - 1 балл.
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
(бланк ответа теоретического тура)
Шифр участника
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
1 тур - тестирование на компьютере 1 курс (максимально - 20 баллов)
№ п/п
Вопрос
Варианты ответов
Периодический закон открыл:
1. Д.И. Менделеев
2. С. Аррениус
3. С.В. Лебедев
4. А.М. Бутлеров
Галогены - это:
1. Металлы
2. Соли
3. Неметаллы
4. Оксиды
Не более восьми электронов:
1. На первом энергетическом уровне
2. На втором энергетическом уровне
3. На четвертом энергетическом уровне
4. На третьем энергетическом уровне
р-подуровень состоит:
1. из пяти р-орбиталей
2. из трех р-орбиталей
3. из десяти р-орбиталей
4. из одной р-орбиталей
В какой из пар у обоих атомов на четвертом энергетическом уровне расположено по 18 электронов?
-
Kr - Ar
-
Ag - Cd
-
Sr - Cd
-
Mg - Kr
К какому типу элементов относится резерфордий?
-
s
-
p
-
d
-
f
Соли кислот H2SO4 , HNO3 , H3PO4 соответственно называются:
-
нитраты, сульфаты, ортофосфаты
-
сульфаты, нитраты, фосфаты
3 сульфаты, нитраты, ортофосфаты
4 сульфиты, нитриты, фосфиты
Укажите среди вариантов ответа катион
-
NO
-
CH3+
-
OH-
-
CO
Реактивом для выявления карбонат-ионов является:
-
гидроксид натрия
-
хлорид калия
-
cоляная кислота
-
нитрат серебра
В реакции
K2S + K2SO3 + H2SO4 →
→ S + K2SO4 + H2O окислителем является вещество:
-
K2SO3
-
H2SO4
-
S
-
H2O
Какие из растворов проводят электрический ток?
-
Раствор глюкозы
-
Раствор этилового спирта
-
Раствор карбоната натрия
-
Уксусный альдегид
Углеводород состава
С2Н5
│
СН3 -С- СH2-C≡СН
│
СН3
имеет название по систематической номенклатуре:
-
2-этил-2-метилпентин-4
-
4-метил-4-этилпентин-1
-
3,3-диметилгексин-5
-
4,4- диметилгексин-1
Сколько изомеров имеет пентан?
-
1
-
3
-
5
-
7
Укажите соединение, в котором степень окисления углерода равна нулю:
-
СН4
-
С6Н12О6
-
С2Н6
-
CO2
Химическая реакция гидратации характеризуется:
-
отщеплением водорода
-
выделением воды
-
присоединением воды
-
присоединением водорода
CnH 2n+1OH - гомологическая формула:
-
аренов
-
алкинов
-
спиртов
-
алканов
Объем метана количеством вещества 0,5 моль равен:
-
112 л
-
11,2 л
-
1,12 л
-
0,11 л
C3H8- это химическая формула:
-
пропана
-
этана
-
бутана
-
пентана
В химическом уравнении горения 1 моль этана (C2H6) перед формулой углекислого газа стоит
коэффициент:
-
2
-
4
-
6
-
0
К какому классу относятся вещества с формулой CnH2n?
-
алканы
-
алкины
-
арены
-
циклоалканы
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
1 тур - тестирование на компьютере 2 курс (максимально - 20 баллов)
№ п/п
Вопрос
Варианты ответов
Изомерия - явление, при котором могут существовать несколько веществ, которые имеют:
-
одинаковый состав, но разное строение молекул
-
разный состав и разное строение молекул
-
разный состав, но одинаковое строение молекул
-
порядок соединения атомов в молекуле
Соединение (я) какого класса отвечает молекулярной формуле С6Н12?
-
Алканы
-
Алкены
-
Алканы и циклоалканы
-
Циклоалканы и алкены
Химическая реакция гидратации характеризуется:
-
отщеплением водорода
-
выделением воды
-
присоединением воды
-
присоединением водорода
Какие виды химической связи в молекуле этилового спирта?
-
σ-связь
-
π-связь
-
σ-связи и π-связь
-
Другие виды связи
В химическом уравнении горения 1 моль этана (C2H6) перед формулой углекислого газа стоит
коэффициент:
-
2
-
4
-
6
-
0
Какое соединение - главный продукт реакции гидратации пропина?
-
Кетон
-
Предельная одноосновная кислота
-
Альдегид
-
Предельный одноатомный спирт
Диэтиловый эфир получается при:
-
взаимодействии этанола с уксусной кислотой
-
отщеплении одной молекулы воды от одной молекулы этанола
-
взаимодействии этанола с хлороводородом
-
отщеплении одной молекулы воды от двух молекул этанола
К какому классу соединений относится вещество, если известно, что при каталитическом гидрировании оно присоединяет водород, а при нагревании его с гидроксидом меди (II) образуется осадок оранжевого цвета?
-
Одноатомные предельные спирты
-
Предельные карбоновые кислоты
-
Альдегиды
-
Сложные эфиры
Выберете ответ, в котором перечислены только углеводороды:
-
CH4, C2H6, C2H5OH
-
CH4, C2H6, C3H8
-
CH4, C2H6, NН2СН(СН3)СООН
-
CH4, C2H6, C6H5Сl
Предельные углеводороды или алканы - это вещества, обладающие общей формулой:
-
CnH2n+1
-
CnH2n
-
CnH2n+2
-
CnH2n-2
Синтетический каучук получают из 2-метилбутадиена-1,3 путем:
-
крекинга
-
поликонденсации
-
изомеризации
-
полимеризации
При щелочной гидратации жиров получают:
-
глицерин и воду
-
глицерин и карбоновые кислоты
-
глицерин и мыло
-
карбоновую кислоту и воду
При полном окислении 1 Моль пропана кислородом воздуха образуется:
-
3 Моль СО2 и 4 Моль Н2О
-
2 Моль СО2 и 4 Моль Н2О
-
2 Моль СО2 и 3 Моль Н2О
-
6 Моль СО2 и 4 Моль Н2О
Вид гибридизации электронных облаков атомов углерода в алканах:
-
sp
-
sp2
-
sp3
-
электронные облака не гибридизуются
Какой объем кислорода (н. у.) нужно для полного сгорания 96 г этилового спирта?
-
13,4 л
-
44,8 л
-
134,4 л
-
4,48 л
Сколько изомеров имеет гептан?
-
5
-
7
-
9
-
11
Плотность паров циклоалкана по водороду равна 42. Молекула циклоалкана не имеет боковых ответвлений от главной углеродной цепи.
-
С6H12 циклогексан
-
С5H10 циклопентан
-
С7H14 циклогептан
-
С4H8 циклобутан
Конечным веществом в цепочке превращений 1-хлорбутан →
бутен-1→ 1,2-дибромбутан → .. является:
-
бутен-1
-
бутин-1
-
н-бутан
-
н-гексан
Углеводород состава
С3Н7
│
СН3 -С=С- СН3
│
СН3
имеет название по систематической номенклатуре:
-
2-пропил-3-метилбутен-2
-
3-пропил-2-метилбутен-2
-
4,5-диметилгексин-4
-
2,3-диметилгексен-2
Альдегиды можно получить в результате следующих химических реакций:
-
гидролизом сложных эфиров, каталитическим окислением предельных углеводородов
-
окислением спиртов, из солей карбоновых кислот
-
присоединением воды к предельным углеводородам
-
дегидрированием гомологов метана
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
Задания 2 тура - решение задач
1 курс (максимально - 24 балла)
-
Электронные формулы двух элементов - 1s22s22p4 и 1s22s22p63s23p4. Составьте уравнение реакции взаимодействия друг с другом двух простых веществ, образованных атомами этих элементов, и назовите образующийся продукт. (3 балла.)
-
При взаимодействии 7,2 г некоего двухвалентного металла с раствором серной кислоты выделилось 6,72 л (н.у.) легкого горючего газа. Определите исходный металл. Составьте уравнение реакции водного раствора соли этого металла, образующейся при действии на него серной кислоты, с водным раствором хлорида бария. Запишите полное и сокращенное ионные уравнения этой реакции и объясните, почему она протекает в водном растворе до конца. (9 баллов.)
-
Самый эффективный способ обезвреживания загрязненных сточных вод химических предприятий - обработка их веществами, осаждающими вредные примеси в виде труднорастворимых соединений. Предприятие подает на участок водоочистки 1000 м3 воды, содержащей 3,31 мг/л нитрата свинца (II). Осаждение катионов свинца ведут, добавляя в стоки 1,27 кг карбоната натрия. Рассчитайте массу выпадающего осадка. Почему очень важно, чтобы добавляемый к стокам реагент - осадитель был в избытке? (8 баллов.)
-
Известно, что молярная масса непредельного углеводорода каротина равна 536 г/моль, а при сжигании 1 моль его образуется 40 моль углекислого газа и 28 моль воды. Определите молекулярную формулу каротина. (4 баллов.)
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
Задания 2 тура - решение задач
2 курс (максимально - 34 балла)
-
При действии на некоторый алкен избытком раствора хлора в четыреххлористом углероде образовалось 3.66 г дихлорпроизводного. При действии на такое же количество исходного углеводорода избытком бромной воды было получено 5.44 г дибромпроизводного. Определите молекулярную формулу алкена, напишите структурные формулы четырех его изомеров, отвечающих условию задачи, назовите их. (10 баллов.)
-
Соединение А - газ, горящий сильно коптящим пламенем. При его нагревании до 6500С в присутствии активированного березового угля образуется бесцветная жидкость В, относительная плотность паров которой по метану равна 4,875. При действии на В смеси концентрированных азотной и серной кислот образуется тяжелая жидкость С с запахом горького миндаля, при каталитическом восстановлении которой водородом получают жидкость Д, имеющую большое практическое значение в органическом синтезе. Приведите формулы веществ А, В, С, Д, назовите их и напишите уравнения всех химических реакций, о которых идет речь.
(9 баллов.)
-
Сколько граммов этилацетата можно получить из 180 г уксусной кислоты и 184 г этанола, если выход сложного эфира составляет в массовых долях 0,9, или 90%, по сравнению с теоретическим? Почему практический выход продукта реакции обычно меньше, чем рассчитанный теоретически по уравнению реакции? Приведите как можно больше причин. (10 баллов.)
-
Определите строение вещества состава С4Н8О, если известно, что при восстановлении оно образует 2-метилпропанол-1, а при окислении 2-метилпропановую кислоту. (5 баллов.)
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
Ответы
1 курс 2 тур (решение задач)
-
Задание 1.
Элемент с электронной формулой 1s22s22p4 имеет порядковый номер и заряд ядра сZ = 2+2+4=8 - кислород (О).
1 б
Элемент с электронной формулой 1s22s22p63s23p4 имеет порядковый номер и заряд ядра сZ = 2+2+6+2+4=18 - сера (S)
1 б
Уравнение реакции: S+ О2 → SО2
0,5 б
SО2- оксид серы (IV), сернистый ангидрид, сернистый газ
0,5 б
Итого
3 б
Задание 2.
Уравнение реакции взаимодействия двухвалентного Металла и разбавленной серной кислоты: Ме+H2SO4→ МеSO4 + H2↑
1 б
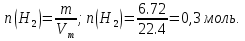
1 б
n(H2)=n(Me)=0,3 моль.
1 б
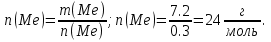 Значит Ме - магний (Mg).
Значит Ме - магний (Mg). 1 б
Уравнения реакций:
Мg+H2SO4→ МgSO4 + H2↑
МgSO4 +BaCl2→МgCl2+BaSO4↓
Мg2++ SO42- +Ba2++2Cl-→Мg2++ 2Cl-+BaSO4↓
Ba2++ SO42- → BaSO4↓
1 б
1 б
1 б
1 б
Данная реакция протекает в водном растворе до конца, т.к. образующийся сульфат бария - нерастворимое соединение.
1 б
Итого
9 б
Задание 3.
Масса нитрата свинца(II) в стоках:
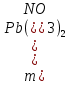
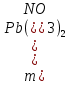
1 б
Количество вещества нитрата свинца в стоках:
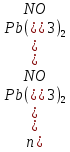
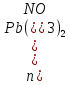
1 б
Количество вещества реагента-осадителя карбоната натрия:
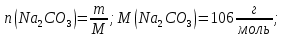
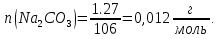
1 б
Уравнение реакции осаждения:
Pb(NO3)2 + Na2CO3 → 2 NaNO3 + PbCO3 ↓
1 б
По уравнению реакции:
 - 1 моль
- 1 моль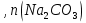 - 1 моль;
- 1 моль; По данным задачи:
 - 10 моль
- 10 моль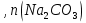 - 12 моль;
- 12 моль; 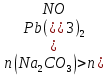 , карбонат натрия в избытке. Расчет массы осадка следует рассчитывать по нитрату свинца (II).
, карбонат натрия в избытке. Расчет массы осадка следует рассчитывать по нитрату свинца (II). 1 б
По уравнению реакции:
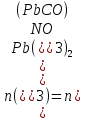
1 б
Масса выпавшего осадка:
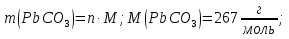
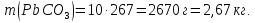
1 б
Реагент-осадитель всегда должен быть в избытке, чтобы загрязнитель прореагировал с ним полностью и весь перешел в осадок, иначе не будет достигнута требуемая степень очистки стоков.
1 б
Итого
8 б
Задание 4.
Так как каротин - углеводород, то пусть формула каротина - СxHy.
Реакцию горения каротина можно схематично записать так:
t0
СxHy+О2 → СО2 + Н2О.
1 б
Количество вещества и индекс углерода в молекуле каротина определим по количеству образовавшегося углекислого газа:
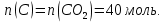
1 б
Количество вещества и индекс водорода в молекуле каротина определим по количеству образовавшейся воды:
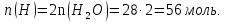
1 б
Простейшая формула каротина С40H56.
Проверка: М(С40H56) = 536 г/моль, что соответствует условию задачи, следовательно молекулярная формула С40H56 - истинная формула каротина.
1 б
Итого
4 б
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015
Ответы
2 курс 2 тур (решение задач)
-
Задание 1.
Общая формула алкенов - СnH2n.
1 б
-
Реакция алкена с хлором:
CCl4
СnH2n + Сl2 → СnH2nСl2;
1 б
-
Реакция алкена с бромом:
H2O
СnH2n + Br2 → СnH2nBr2.
1 б
Молярная масса алкена: М(СnH2n) = 12n + 2n = 14n.
Молярная масса дихлоралкена: М(СnH2nСl2) = 14n + 71.
Молярная масса дибромалкена: М(СnH2nBr2) = 14n + 160.
1 б
Количество вещества дихлоралкена:
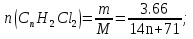
1 б
Количество вещества дибромалкена:
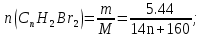
1 б
По уравнению 1: n(СnH2n) = n(СnH2nСl2)
По уравнению 2: n(СnH2n) = n(СnH2nBr2), следовательно
n(СnH2nСl2) = n(СnH2nBr2).
1 б
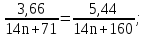
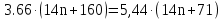
51,24 n + 585,6 = 76,16 n + 386,24
24,92 n = 199,36
n = 8. С8H16 - октен
1 б
Структурные формулы и названия изомеров октена по положению кратной связи:
1 2 3 4 5 6 7 8
-
СН2=СН-СН2-СН2- СН2- СН2- СН2- СН3 октен-1
1 2 3 4 5 6 7 8
-
СН3-СН=СН-С Н2- СН2- СН2- СН2- СН3 октен-2
1 2 3 4 5 6 7 8
-
СН3-СН2-СН=С Н- СН2- СН2- СН2- СН3 октен-3
1 2 3 4 5 6 7 8
-
СН3-СН2-СН2-СН=СН- СН2- СН2- СН3 октен-4
0,5 б
0,5 б
0,5 б
0,5 б
Итого
10 б
Задание 2.
Вещество А - ацетилен С2H2.
1 б
Уравнение реакции горения ацетилена:
t0
2С2H2+5О2 → 4СО2 +2 Н2О.
1 б
Вещество В - бензол С6H6.
1 б
Относительная плотность паров бензола по метану:
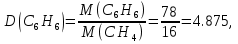 что соответствует условию задачи
что соответствует условию задачи 1 б
Уравнение реакции тримеризации ацетилена:
6500С, акт.уголь
3С2H2 - С6H6.
1 б
Вещество С - нитробензол С6H5NO2.
1 б
Уравнение реакции нитрования бензола:
t0, Н2SO4(конц.)
С6H6 + HNO3 С6H5NO2 + Н2O.
1 б
Вещество D - анилин С6H5NН2.
1 б
Уравнение реакции восстановления нитробензола:
t0, Ni(Pt)
С6H5NO2 + 3Н2 С6H5NН2 + 2Н2O
1 б
Итого
9 б
Задание 3.
Количество вещества уксусной кислоты:
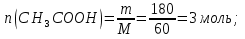
Количество вещества этилового спирта:
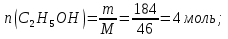
1 б
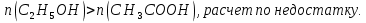
1 б
Уравнение реакции этерификации:
Н+
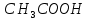 +
+ 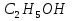
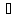
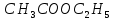 +
+ 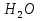 .
. Уксусная этанол уксусноэтиловый
Кислота эфир (этилацетат)
1 б
1 б
По уравнению реакции: n эфира (
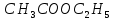 ) = n уксусной кислоты (
) = n уксусной кислоты (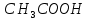 ) =
) = 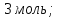
1 б
M(
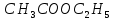 ) = 88 г/моль; m(
) = 88 г/моль; m(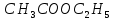 ) = n
) = n  M = 3
M = 3  88 = 264 г.
88 = 264 г. 1 б
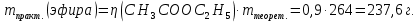
1 б
Практический выход продукта реакции обычно меньше, чем рассчитанный теоретически по уравнению реакции:
-
реакции не идут на 100% в одну сторону. Есть понятие химического равновесия.
-
при очистке полученного продукта от остатков исходных реагентов или растворителей тоже могут происходить потери.
-
в некоторых реакциях потери неизбежны просто по условиям протекания таких реакций (например, испарение исходных веществ)
-
некоторые химические реакции идут весьма медленно. Поэтому используют катализаторы.
-
Как правило не всё вещество вступает в реакцию (не преодолена энергия активации)
-
Исходные реагенты могут содержать примеси.
0,5 б
0,5 б
0,5 б
0,5 б
0,5 б
0,5 б
Итого
10 б
Задание 4.
Вещество C4H8O соответствует общей формуле CnH2nO, которая является общей формулой предельных альдегидов.
1 б
По условию задачи альдегид должен иметь формулу:
O
//
CH3-CH-C; 2-метилпропаналь.
| \
CH3 H
1 б
Уравнение реакции восстановления альдегида:
Ni
CH3-CH-COH +H2 CH3-CH-CH2OH
| |
CH3 CH3
(2-метилпропанол-1)
1 б
0,5 б
CH3-CH-COH +Ag2O = CH3- CH- COOH+2Ag
| |
CH3 CH3
(2-метилпропановая кислота)
1 б
0,5 б
Итого
5 б
-
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015 г.
(практический тур - 2 курс)
Шифр участника
Задание
В четырех пробирках под номерами могут находиться растворы следующих веществ: глицерин, глюкоза, крахмал, белок, уксусная кислота, фенол.
Определите опытным путем, в какой пробирке содержится то или иное вещество.
Составьте наиболее рациональный и краткий план распознавания с применением минимального числа вспомогательных реактивов.
Оборудование и реактивы:
-
Штатив с пробирками
-
Спиртовка
-
Держатель для пробирок
-
Дистиллированная вода
-
Раствор гидроксида натрия
-
Раствор сульфата меди (II)
-
Раствор нитрата серебра
-
Раствор иода
-
Раствор хлорида железа (III)
-
Раствор карбоната натрия
-
Концентрированная азотная кислота
Вещество
Реактив
Условия реакции
Признаки реакции
Глицерин
Глюкоза
Крахмал
Белок
Уксусная кислота
Фенол
Порядок открытия органических веществ:
1.__________________________________________________
2.__________________________________________________
3.__________________________________________________
4.__________________________________________________
5.__________________________________________________
Работа с нарушением правил техники безопасности или небрежным выполнением эксперимента - не оценивается и не засчитывается!
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015 г.
(практический тур - 1 курс)
Шифр участника
Задание
В четырех пробирках под номерами могут находиться растворы следующих веществ: глицерин, глюкоза, крахмал, белок.
Определите опытным путем, в какой пробирке содержится то или иное вещество.
Составьте наиболее рациональный и краткий план распознавания с применением минимального числа вспомогательных реактивов.
Оборудование и реактивы:
-
Штатив с пробирками
-
Спиртовка
-
Держатель для пробирок
-
Дистиллированная вода
-
Раствор гидроксида натрия
-
Раствор сульфата меди (II)
-
Раствор нитрата серебра
-
Раствор иода
-
Раствор хлорида железа (III)
-
Раствор карбоната натрия
-
Концентрированная азотная кислота
Вещество
Реактив
Условия реакции
Признаки реакции
Глицерин
Глюкоза
Крахмал
Белок
Порядок открытия органических веществ:
1.__________________________________________________
2.__________________________________________________
3.__________________________________________________
4.__________________________________________________
Работа с нарушением правил техники безопасности или небрежным выполнением эксперимента - не оценивается и не засчитывается!
Ключ экспериментального тура, 1 курс
Вещество
Реактив
Условия реакции
Признаки реакции
Порядок открытия
Глицерин
Сu(OH)2
Образование ярко-синего раствора
1
Глюкоза
Сu(OH)2
t0
Ярко-синее окрашивание, при нагревании образование красного осадка
2
Крахмал
I2
Синее окрашивание
4
Белок
Сu(OH)2
Фиолетовое окрашивание
3
Ключ экспериментального тура, 2 курс
Вещество
Реактив
Условия реакции
Признаки реакции
Порядок открытия
Глицерин
Сu(OH)2
Образование ярко-синего раствора
1
Глюкоза
Сu(OH)2
t0
Ярко-синее окрашивание, при нагревании образование красного осадка
2
Крахмал
I2
Синее окрашивание
5
Белок
Сu(OH)2
Фиолетовое окрашивание
3
Уксусная кислота
Na2CO3
Выделение газа СО2
4
Фенол
FeCl3
Фиолетовое окрашивание
-
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015 г.
Ключ к практическому туру - 1 курс
Вариант
Вещества
Вариант
Вещества
Вариант
Вещества
1
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
10
-
Глюкоза
-
Глицерин
-
Крахмал
-
Белок
19
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
2
-
Глюкоза
-
Глицерин
-
Крахмал
-
Белок
11
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
20
-
Глюкоза
-
Глицерин
-
Крахмал
-
Белок
3
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
12
-
Глицерин
-
Белок
-
Крахмал
-
Глюкоза
21
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
4
-
Крахмал
-
Белок
-
Глюкоза
-
Глицерин
13
-
Глицерин
-
Белок
-
Глюкоза
-
Крахмал
22
-
Крахмал
-
Белок
-
Глюкоза
-
Глицерин
5
-
Белок
-
Глицерин
-
Крахмал
-
Глюкоза
14
-
Глюкоза
-
Крахмал
-
Глицерин
-
Белок
23
-
Белок
-
Глицерин
-
Крахмал
-
Глюкоза
6
-
Крахмал
-
Глицерин
-
Белок
-
Глюкоза
15
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
24
-
Крахмал
-
Глицерин
-
Белок
-
Глюкоза
7
-
Глицерин
-
Белок
-
Крахмал
-
Глюкоза
16
-
Крахмал
-
Белок
-
Глицерин
-
Глюкоза
25
-
Глицерин
-
Белок
-
Крахмал
-
Глюкоза
8
-
Крахмал
-
Глицерин
-
Глюкоза
-
Белок
17
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
26
-
Крахмал
-
Глицерин
-
Глюкоза
-
Белок
9
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
18
-
Глицерин
-
Белок
-
Крахмал
-
Глюкоза
27
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
Олимпиада по химии для студентов учреждений среднего профессионального образования Саратовской области, 2015 г.
Ключ к практическому туру - 2 курс
Вариант
Вещества
Вариант
Вещества
Вариант
Вещества
1
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
10
-
Глюкоза
-
Глицерин
-
Крахмал
-
Белок
19
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
2
-
Глюкоза
-
Уксус. кисл.
-
Крахмал
-
Белок
11
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
20
-
Глюкоза
-
Уксус. кисл.
-
Крахмал
-
Белок
3
-
Уксус. кисл.
-
Глюкоза
-
Глицерин
-
Крахмал
12
-
Глицерин
-
Белок
-
Уксус. кисл.
-
Глюкоза
21
-
Уксус. кисл.
-
Глюкоза
-
Глицерин
-
Крахмал
4
-
Уксус. кисл.
-
Белок
-
Глюкоза
-
Глицерин
13
-
Глицерин
-
Белок
-
Глюкоза
-
Крахмал
22
-
Уксус. кисл.
-
Белок
-
Глюкоза
-
Глицерин
5
-
Уксус. кисл.
-
Глицерин
-
Крахмал
-
Глюкоза
14
-
Глюкоза
-
Крахмал
-
Глицерин
-
Уксус. кисл.
23
-
Уксус. кисл.
-
Глицерин
-
Крахмал
-
Глюкоза
6
-
Уксус. кисл.
-
Глицерин
-
Белок
-
Глюкоза
15
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
24
-
Уксус. кисл.
-
Глицерин
-
Белок
-
Глюкоза
7
-
Уксус. кисл.
-
Белок
-
Крахмал
-
Глюкоза
16
-
Крахмал
-
Белок
-
Глицерин
-
Уксус. кисл.
25
-
Уксус. кисл.
-
Белок
-
Крахмал
-
Глюкоза
8
-
Крахмал
-
Глицерин
-
Уксус. кисл.
-
Белок
17
-
Глицерин
-
Крахмал
-
Белок
-
Глюкоза
26
-
Крахмал
-
Глицерин
-
Уксус. кисл.
-
Белок
9
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
18
-
Уксус. кисл.
-
Белок
-
Крахмал
-
Глюкоза
27
-
Белок
-
Глюкоза
-
Глицерин
-
Крахмал
Список использованных источников
-
Школьные олимпиады. Химия. 8 - 11 классы/А.В. Артемов, С.С. Дерябина. - 2-е изд. - М.: Айрис-пресс, 2009. - 240 с.
-
Всероссийская олимпиада школьников по химии Тюльков И.А., Емельянов В.А., Архангельская О.В., Лунин В.В. Методические рекомендации по проведению школьного и муниципального этапов всероссийской олимпиады школьников по химии в 2014/2015 учебном году. Москва, 2014 г.
-
Ерохин Ю.М. Химия: Учеб. для средних проф. учебных заведений. - М.: Мастерство, 2002. - 384 с.
-
Габриелян О.С. Химия: учеб. для студ. учреждений сред. проф. образования/ О.С. Габриелян, И.Г. Остроумов. - 8-е изд., стер. - М.: Издательский центр «Академия», 2011. - 336 с.
-
Егоров А.С., Аминова Г.Х. Эксперсс-курс неорганической и органической химии. Для поступающих в вузы. - Ростов н/Д: изд-во «Феникс», 2002. - 336 с.
-
Зоммер К. и др. Химия: Справочник школьника и студента/ К.Зоммер, К.Х. Вюнш, М. Цеттлер; Пер. с нем. под ред. проф Р.А. Лидина. - 2-е изд., стереотип. - М.: Дрофа, 2000. - 384 с.
-
Ерохин Ю.М., Фролов В.И. Сборник задач и упражнений по химии (С дидактическим материалом): Учеб. Пособие для средних спец. Учебных заведений. - 2-е изд., перераб. И доп. - М.: Высш. шк., 1998. - 304 с.


