- Преподавателю
- Химия
- Ковалентная связь и геометрия молекул
Ковалентная связь и геометрия молекул
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Норина Т.Ю. |
| Дата | 16.12.2014 |
| Формат | doc |
| Изображения | Есть |
Ковалентная связь и геометрия молекул
Цели урока:
-
Раскрыть универсальный характер понятия "гибридизация орбиталей".
-
Показать зависимость пространственного строения молекул веществ от типа гибридизации электронных орбиталей.
-
Показать зависимость физических свойств от геометрии молекул.
Форма урока: Комбинированный урок.
Особенности урока: Проведён по технологии "развитие критического мышления" с применением мультимедийного комплекса.
Оборудование:
-
Модели гибридных облаков для магнитной доски.
-
Тексты для работы учащихся.
-
Вопросы для 1-го этапа урока "Знаю" (Приложение I).
-
Текст для "критического чтения" (Приложение II).
-
Мультимедийный комплекс для демонстрации фрагментов темы "Химическая связь" (1, 2, 3 фрагменты).
-
-
Компакт-диск "Химия общая и неорганическая 10-11 класс" Лаборатория систем мультимедиа, МарГТУ. Предназначен для изучения химии в 10-11 классах.
Задачи:
-
Научить учащихся критически мыслить.
-
Научить учащихся добывать знания.
Ожидаемые результаты:
-
Учащиеся должны предсказывать геометрию молекул, применяя теорию гибридизации электронных орбиталей.
Этапы урока:
I. Стадия "Вызова"
-
Записать тему урока.
-
Разделить развёрнутый двойной лист на 3 колонки: "Знаю", "Хочу знать", "Узнал".
-
Учащиеся читают вопросы (Приложение I) и выписывают те понятия, которые знают в 1-ую колонку - "Знаю".
Приложение 1
-
Во вторую колонку - "Хочу знать" выписываю т проблемы, возникающие в ходе ответов на вопросы.
Предполагаемые проблемы:
-
Почему возникает направленность связи?
-
Каким образом определяется направленность связи?
-
Почему геометрия молекул влияет на физические свойства?
II. Стадия "Осмысления"
-
Демонстрация фрагмента №1 "Направленность электронных облаков". Во фрагменте в динамике показываются электронные облака и их перекрывания. Диктор делает вывод, что направленность связи возникает из-за направленности перекрывающихся облаков.
-
Фрагмент №2. В отрывке рассказывается о том, что перед образованием связи облака гибридизируются.
-
Чтение текста с маркировкой: "Знаю" V, "Узнал" +, "Удивило" ?
Приложение II
III. Этап "Рефлексия".
-
Учащиеся отвечают на вопросы по второй колонке - "Хочу знать".
-
Демонстрируют шаростержневые молекулы.
-
Делается вывод, что молекула состава AB2 могут быть линейные или угловые. Демонстрируется фрагмент №3. Фрагмент показывает тип гибридизации электронных орбиталей в молекулах NH3 и CH4 и геометрию этих молекул.
Домашнее задание:
Учебник Габриелян О.С. 11 кл. Зарисовать перекрывание облаков в молекуле CO2, BCl3. Ответить на вопрос №11: "Почему растворимость SO2 лучше, чем CO2?"
Приложение Вид доски.
Тема: Глюкоза. Строение глюкозы.
Знаю
Хочу узнать
Узнал
Синквейн
Гипотезы:
1. Глюкоза - кислородосодержащее вещество
2. Глюкоза - углевод
3. С6Н12О6
1 .К какому классу
веществ можно
отнести глюкозу?
а)к альдегидам
б)к многоатомным спиртам
в)к карбоновым кислотам
2.Какая углеродная цепь - линейная или разветвленная?
3.Сколько
гидроксильных групп
содержит глюкоза?
Лабораторная работа
"Изучение свойств глюкозы"
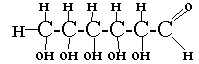
существительное
три прилагательных
два глагола
крылатая фраза
существительное
По данной технологии записей больше у учащихся, поэтому представляю вид
записей у учащихся (см. следующую стр.) записи в тетради у у чащихся
На доске я только напоминаю форму и распределение записей в колонках у
учащихся (ступенчатый)
Вид записи в тетради у учащихся.
Тема: Глюкоза. Строение глюкозы.
Знаю
Хочу узнать
Узнал
Гипотезы:
1. Глюкоза - кислородосодержащее вещество
2. Глюкоза - углевод
3. С6Н12О6
1 .К какому классу
веществ можно
отнести глюкозу?
а)к альдегидам
б)к многоатомным спиртам
в)к карбоновым кислотам
2.Какая углеродная цепь - линейная или разветвленная?
3.Сколько
гидроксильных групп
содержит глюкоза?
Лабораторная работа:"Изучение свойств глюкозы"
1.гидроксидмеди (II) от раствора
глюкозы синеет -> глюкоза многоатомный спирт
2. раствор глюкозы с гидроксидом
меди (II) при нагревании
краснеет -> глюкоза содержит
альдегидную группу
3. присоединяет до 5 молекул
уксусной кислоты-> 5
гидроксильных групп
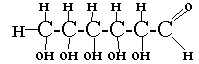
Синквейн:
Глюкоза
Сладкая, растворимая, энергетическая
Краснеет и синеет от Cu(OH)2
Хочешь лучше думать - съешь глюкозу
Альдегидоспирт.
Домашнее задание:
-
Учебник Габриелян О.С. 10 кл. §22, моносахариды
-
Записать уравнения реакций по третьей колонке «Узнал»:
1. Глюкоза - альдегид 2. Глюкоза - многоатомный спирт (На основе лабораторной работы).
Приложение I
Ковалентная связь. Её характеристики.
-
Что такое ковалентная связь?
-
Какова классификация ковалентной связи по способу перекрывания электронных орбиталей?
-
Какова классификация ковалентной связи по кратности?
-
Что такое длина связи?
-
Какая связь бывает по степени смещённости?
-
Почему следует отличать полярность связи от полярности молекулы?
-
Что такое направленность связи?
-
Каким образом определяется направленность связи?
-
По каким связям определяют угол (σ или π)?
-
Молекулы CO2 и SO2 отвечают общей формуле AB2. Почему молекула CO2 - линейная, а SO2 - угловая?
-
Почему растворимость SO2 лучше, чем у CO2?
Приложение II
Гибридизация электронных орбиталей и геометрия молекул
В основе модели максимального перекрывания облаков (МП) форма молекул сопоставляется с типом гибридизации орбиталей центрального атома (ЦА).
При образовании химической связи орбитали ЦА гибридизируются (гибридизация осуществляется при возбуждении атома). Гибридизация - это выравнивание орбиталей по форме и по энергии. Возможно шесть сочетаний гибридизирующихся орбиталей: sp, sd, sf, pd, pf, df. Рассмотрим простейшие способы гибридизации орбиталей sp:
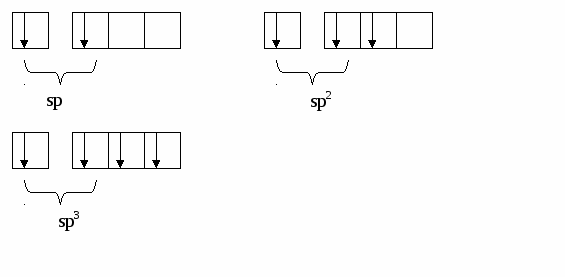
Мы встречались со всеми этими способами гибридизации в курсе органической химии. У атома углерода в молекуле метана наблюдается sp3, в молекуле этилена sp2, в молекуле ацетилена sp-гибридизация.
SP3-гибридизация обуславливает тетраэдрическое строение молекулы метана, sp2-плоскостное в молекуле этилена, а sp-линейное строение молекулы ацетилена.
Гибридизация орбиталей - понятие универсальное, т.е. применяется для молекул неорганических веществ. У элементов, имеющих два, три и четыре валентных электрона (в ЦА), можно рассматривать указанные виды гибридизации орбиталей sp.
Попробуйте определить геометрию (углы) молекул AB2: ВеCl2 и H2O на основе теории гибридизации электронных орбиталей, рассмотрев электронно-графические формулы этих элементов и зарисовать перекрывание всех облаков в этих молекулах.


