- Преподавателю
- Химия
- Тесты по органической химии
Тесты по органической химии
| Раздел | Химия |
| Класс | - |
| Тип | Тесты |
| Автор | Хамзина А.Т. |
| Дата | 28.11.2014 |
| Формат | doc |
| Изображения | Есть |
Тест по органической химии 10 класс
1. Общая формула альдегидов:
а) СnH2n+1OH б) R - COH в) R - COOH г) R1 - COOR2
2. Углеводород С9Н12 относится к классу:
а) алканы б) алкены в) арены г) алкины.
3. Тип гибридизации атомов С в ацетилене:
а) sp3 б) sp2 в) sp г) sp3d2
4. Длина связи С - С в молекуле этана, нм:
а) 0,154 б) 0,140 в) 0,120 г) 0,134
5. Углеводород 2,2-диметилпентан имеет молярную массу, г/моль: а) 98 б) 100 в)102 г) 104
6. Плотность паров одноосновной карбоновой кислоты по водороду равна 30. Формула кислоты:
а) НСООН б) СН3СООН в) СН3СН2СООН г) СlСН2СООН
7. Формула метанола:
а) НСООН б) НСОН в) СН3ОН г) С2Н5ОН
8. Для алканов наиболее характерны реакции:
а) присоединения б) замещения
в) полимеризации г) окисления.
9. Вещества бутанол-1 и бутанол-2:
а) изомеры б) гомологи.
10. Углеводород содержит 93,3% углерода и 7,7% водорода, плотность при н.у. 1,161 г/л. Химическая формула углеводорода _________
11. Фенол не вступает в реакцию с веществом:
а) NaOH б) Br2 (aq) в) Na г) NaHCO3
12. Реакция гидратации:
а) С2Н4 + Н2 б) С2Н4 + Н2О
в) СН3СООС2Н5 + НОН г) СН4
13. Этилен в лаборатории получают:
а) СаС2 + Н2О б) Al4C3 + H2O
в) С2Н2 + Н2О г) С2Н5ОН
14. Метан получают в промышленности:
а) Al4C3 + H2Oб) СН3СООNa + NaOH в) из природного газа г) из нефти
15. Реакция не возможна в случае:
а) С2Н5ОН + Ag2O б) С2Н5ОН + СН3СООН
в) С6Н5СООН + NаОН г) С6Н6 + НОNO2
16.Сила кислот в ряду CH3COOH - CH2ClCOOH - CHCl2COOH - CCl3COOH
а) возрастает б) уменьшается
17. Для распознавания глицерина и этанола можно воспользоваться реактивом:
а) Cu(OH)2 б) Br2 (aq) в) KMnO4 г) Ag2O (ам.)
18. При сгорании органического вещества массой 4,6 г получили 8,8 г СО2 и 5,4 г Н2О. Относительная плотность вещества по водороду равна 23. Формула органического вещества _________.
19. Наибольшая массовая доля углерода в соединении:
а) С2Н2 б) С2Н6 в) С2Н4 г) С2Н5ОН
20. Объём воздуха, необходимый для сжигания 2 литров пропана, л: а) 10 б) 20 в) 50 г) 100
21. Дана схема превращений:
22. Объём углекислого газа (н. у.), полученный при спиртовом брожении 5 моль 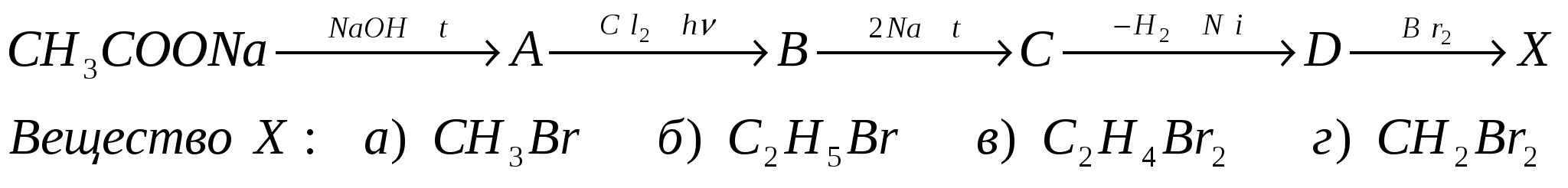
глюкозы, л:
а) 2,24 б) 22,4 в) 224 г) 2240
23. Для получения этилового эфира муравьиной кислоты необходимо взять:
а) СН3СООН и С2Н5ОН б) НСООН и СН3ОН
в) СН3СООН и СН3ОН г) НСООН и С2Н5ОН
24. Углеводород, содержащий тройную связь:
а) С4Н6 б) С4Н8 в) С4Н10 г) СН4
25. Вещество, которое можно обнаружить по запаху:
а) СН2 - ОН б) СН2 - ОН в) СН3СООН г) С6Н12О6
СН2 - ОН СН - ОН
СН2 - ОН
Т
ест по органической химии, 10 класс
1. Общая формула алкенов:
а) СnH2n+2 б) СnH2n-6 в) СnН2n г) CnH2n-2
2. Вещество СН3 -СН2 - СН = О принадлежит к классу:
а) спирты б) альдегиды
в) карбоновые кислоты г) сложные эфиры
3. Тип гибридизации атомов С в бензоле:
а) sp б) sp2 в) sp3 г) sp3d2
4. Валентный угол НСН в молекуле метана:
а) 10928 б) 120 в) 180 г) 90
5. Углеводород 3-метилбутин-1 имеет молярную массу, г/моль:
а) 68 б) 70 в) 72 г) 74
6. Плотность паров предельного одноатомного спирта по водороду равна 37. Формула спирта:
а) С2Н5ОН б) С3Н7ОН в) С4Н9ОН г) С5Н11ОН
7. Химическая формула муравьиного альдегида:
а) СН3СООН б) НСОН в) НСООН г) СН3ОН
8. Для ароматических углеводородов наиболее характерны реакции:
а) замещения б) присоединения
в) этерификации г) гидролиза
9. Вещества бутен-2 и гексен-2:
а) гомологи б) изомеры.
10. Углеводород содержит 85,7% углерода и 14,3% водорода. Плотность при
н.у. 1,875 г/л. Формула углеводорода __________.
11. Фенол вступает в реакцию с веществом:
а) Н2О б) Br2 (aq) в) НСl г) Na2CO3
12. Реакция этерификации:
а) C2H5Cl + NaOH б) С2Н5ОН + СН3СООН
в) С2Н2 + НОН г) С2Н2 + Н2
13. Этилен в лаборатории получают:
а) С2Н2 + Н2 б) СН3Cl + Na в) С2Н5ОН г) Al4C3 + HCl
14. Изомером глюкозы является:
а) фруктоза б) рибоза в) крахмал г) целлюлоза
15. При окислении этилена водным раствором перманганата калия образуется:
а)уксусная кислота б) этиловый спирт в)этиленгликоль г) уксусный альдегид
16. При взаимодействии метанола с муравьиной кислотой образуется:
а) СН3СООСН3 б) СН3СООС2Н5 в) НСООС2Н5 г) НСООСН3
17. Для распознавания метана и ацетилена следует воспользоваться:
а) КMnO4 (р-р) б) NaOH в) НСl г) Сu(OH)2
18.При сжигании 3 г органического вещества получили 4,4 г СО2 и 1,8 г Н2О. Относительная плотность паров вещества по водороду 30. Химическая формула вещества ________
19. Наибольшая массовая доля углерода в соединении:
а) С6Н6 б) С6Н5Сl в) С6Н5ОН г) С6Н5СООН
20. Из 1 кг технического карбида кальция получили 260 л ацетилена (н.у.).
Массовая доля примесей в исходном образце карбида, %.
а) 2,57 б) 25,7 в) 74,3 г) 81,2
21. Дана схема превращений:
В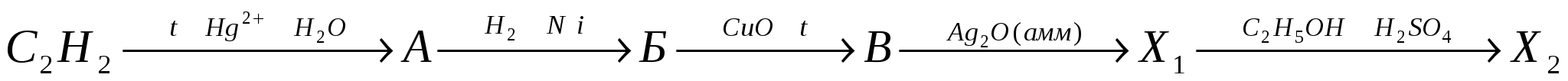
ещество Х2:
а) муравьиный альдегид б) уксусный альдегид
в) муравьиная кислота г) этилацетат
22. Масса этилового спирта, образовавшаяся при брожении 200 г 80%-ного
раствора глюкозы, г:
а) 46 б) 81,9 в) 92 г) 41,1
23. Природным полимером является:
а) полиэтилен б) сахароза в) глюкоза г) крахмал
24. Муравьиный спирт - 1,25%-ный раствор вещества:
а) этанол б) уксусная кислота
в ) муравьиная кислота г) метанол
25. При сварке и резке металлов используют:
а) бутадиен-1,3 б) ацетилен в) этилен г) метан
Тест по органической химии 10 класс
1. Общая формула карбоновых кислот:
а) R - OH б) R - COH в) R - COOH г) R1 - CO - R2
2.Углеводород С4Н8 относится к классу:
а) алканы б) циклоалканы в) алкины г) алкадиены
3. Тип гибридизации атомов С в пропане:
а) sp3 б) sp2 в) sp г) sp3d2
4. Геометрическая форма молекул метана:
а) линейная б) плоская в) тетраэдрическая г) тор
5. Этиловый эфир пропановой кислоты имеет молярную массу: г/моль:
а) 60 б) 74 в) 88 г) 102
6. Плотность по водороду алкена равна 42. Формула алкена _______
7. Химическая формула уксусного альдегида:
а) СН3СОН б) СН3ОН в) СН3СООН г) НСОН
8. Для ацетиленовых углеводородов наиболее характерны реакции:
а) замещения б) присоединения в) этерификации г) дегидратации
9. Вещества глюкоза и фруктоза:
а) гомологи б) изомеры
10. Углеводород содержит 84,21% углерода и 15,79% водорода. Относительная плотность углеводорода по водороду 3,93. Молекулярная формула углеводорода _______.
11. Этанол не вступает в реакцию с химическим соединением:
а) Na б) СН3СООН в) НBr г) Na2CO3
12. Реакция гидрирования:
а) С2Н4 + Н2О б) СН4
в) С2Н2 + Н2 г) С2Н5ОН + НСООН
13. Уксусный альдегид можно получить:
а) С2Н2 + Н2О б) СН3СООNa + NaOH
в) С2Н5ОН г) СН3Cl + NaOH
14. Гомологом этилена является:
а) этан б) ацетилен в) бутен-1 г) дивинил
15. Сила кислот в ряду CFH2COOH - CClH2COOH - CBrH2COOH
а) возрастает б) уменьшается.
16. При взаимодействии карбоновых кислот со спиртами образуются:
а) соли карбоновых кислот б) простые эфиры
в) сложные эфиры г) альдегиды
17. Для распознавания муравьиной и уксусной кислот следует использовать:
а) Ag2O (амм.) б) лакмус в) Na г) Br2 (aq)
18. При сжигании органического вещества массой 9,2 г получили 8,96 л СО2 (н.у.) и 10,8 г воды. Относительная плотность вещества по воздуху 1,587. Молекулярная формула вещества _______
19. Наибольшая массовая доля углерода в соединении:
а) С2Н5ОН б) С2Н4Сl2 в) СН3СООН г) СН3СОН
20. Из 10 г 96%-ного этилового спирта получили 4 л этилена (н.у.). Выход этилена, %:
а) 74 б)86 в) 92 г) 95
21. Дана схема превращений:
В
ещество Х:
а) бензол б) толуол в) бромбензол г) 4- бромтолуол
22.Обьём углекислого газа, полученный при сжигании 8 л метана (н.у.), л:
а) 4 б) 6 в) 8 г) 16
23. Для определения крахмала в продуктах используют:
а) Br2 (aq) б) Ag2O (амм.) в) I2 (спирт. р-р) г) KMnO4
24. Для приготовления антифризов применяют:
а) этанол б) уксусный альдегид
в) этилацетат г) этиленгликоль.
25. Формалин -40% раствор вещества:
а) глюкоза б) муравьиный альдегид
в) муравьиная кислота г) фенол.
Тест по органической химии 10 класс
1. Общая формула спиртов:
а) R -COH б) R - COOH в) R - OH г) R1 - CO - R2
2. Углеводород С3Н6 относится к классу:
а) алканы б) алкены в) арены г) алкины.
3. Тип гибридизации атомов С в этилене:
а) sp3 б) sp2 в) sp г) sp3d2
4. Валентный угол НСН в ацетилене:
а) 10928 б) 120 в) 180 г) 90
5. Углеводород 3,4 диметилпентен-1 имеет молярную массу, г/моль:
а) 96 б) 98 в)100 г) 102
6. Плотность паров альдегида по воздуху равна 2. Формула альдегида:
а) НСОН б) СН3СОН в) СН3СН2СОН г) С2Н5СН3СОН
7. Формула муравьиной кислоты:
а) СН3ОН б) СН3СОН в) СН3СООН г) НСООН
8. Для алкенов наиболее характерны реакции:
а) присоединения б) замещения
в) этерификации г) дегидрирования.
9. Вещества 2-метилбутан и 2-метилпропан:
а) изомеры б) гомологи.
10. Углеводород содержит 82,8% углерода и 17,2% водорода, плотность при н.у. 2,59 г/л. Формула углеводорода ___________________
11. Бензол может взаимодействовать с веществом:
а) вода б) бромная вода
в) бром г) гидроксид натрия
12. В реакцию гидрирования вступает:
а) СН3СОН б) СН3СООН в) СН3СН2ОН г) С2Н6
13. Ацетилен в лаборатории получают:
а) СН3СООNa+NaOH б) СаС2+Н2О
в) Аl4C3+H2O г) СН3СН2ОН+СuO
14. Гомологом бензола является углеводород:
а) С7Н8 б) С6Н14
в) С6Н12 г) С6Н5 - СН = СН2
15. Гидроксид меди (II) взаимодействует со спиртом:
а) СН3ОН б) С2Н5ОН в) СН2 - ОН г) СН3 (СН2)2 ОН
СН2 - ОН
16. В результате гидролиза сахарозы получают:
а) глюкозу б) глюкозу и фруктозу в) крахмал г) рибозу
17. Для распознавания этана и этилена необходим реактив:
а) NaOH б) Сu(OH)2 в) Br2 (aq) г) Ag2O (амм.)
18. При сжигании органического вещества массой 2,4 г получены 3,3 г СО2 и 2,7 г Н2О. Относительная плотность вещества по водороду 16. Формула вещества _____________
19. Наибольшая массовая доля углерода в соединении:
а) СН4 б) СН3Сl в) НСОН г) СCl4
20. В реакцию вступает 23 г этанола и 45 г уксусной кислоты. Масса полученного сложного эфира при 90% выходе, г:
а) 39,6 б) 44 в) 66 г) 59,4
21. Дана схема превращений:
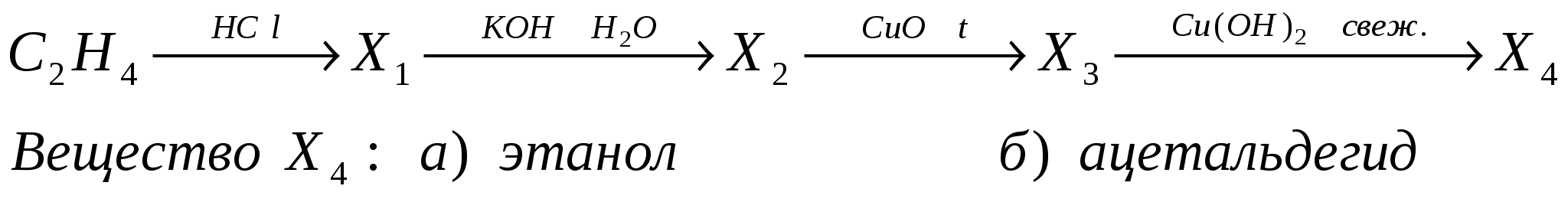
в) этановая кислота г) метановая кислота
22. При брожении глюкозы выделился углекислый газ объёмом 112 л (н.у.). Масса глюкозы, подвергшейся брожению, г:
а) 900 б) 450 в) 4,5 г) 90
23. При нагревании спиртов с концентрированной серной кислотой (температура 140) образуются:
а) алкоголяты б) альдегиды
в) простые эфиры г) сложные эфиры
24. Углеводород, содержащий две двойные связи:
а) С3Н8 б) С3Н6 в) С3Н4 г) С4Н10
25. Вещество, которое можно обнаружить по внешнему виду среди других органических веществ:
а) этанол б) уксусная кислота в) глицерин г) этилацетат


