- Преподавателю
- Химия
- Подготовка к ЕГЭ по химии. ЦИКЛОАЛКАНЫ
Подготовка к ЕГЭ по химии. ЦИКЛОАЛКАНЫ
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Кисакова О.А. |
| Дата | 26.11.2014 |
| Формат | docx |
| Изображения | Есть |
Циклоалканы - предельные циклические углеводороды.
Общая формула гомологического ряда CnH2n.
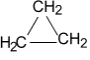

Циклопропан
Циклобутан
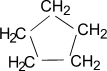
Циклопентан
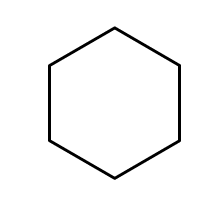
Циклогексан
Малые циклы
Большие циклы
Строение циклоалканов.
Каждый атом углерода в циклоалканах находится в состоянии sp3-гибридизации и образует четыре σ-связи С-С и С-Н.
Углы между связями зависят от размера цикла. В малых циклах С3 и С4 углы между связями С-С сильно отличаются от тетраэдрического угла 109,5°, что создает в молекулах напряжение и обеспечивает их высокую реакционную способность.
σ-связи в циклопропане называют "банановыми". По свойствам они напоминают ПИ-связи. Поэтому молекулу циклопропана очень легко разорвать и поэтому он способен вступать в реакции присоединения (с разрывом цикла).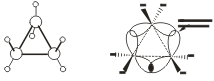
Циклобутан в пространстве имеет перегиб по линии, соединяющей 1 и 3 атом С в кольце:
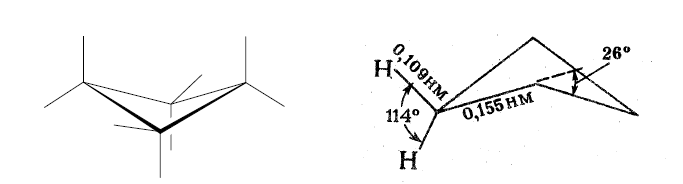
Циклопентан имеет форму, которую называют «конверт»:
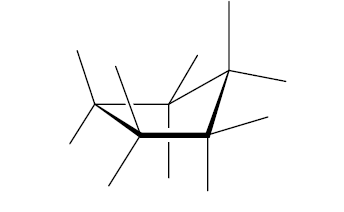
Большие циклы очень устойчивы и не склонны к разрыву. Так, молекула циклогексана не является плоским многоугольником и принимает различные конформации, имеющие названия «кресло» и «ванна»:
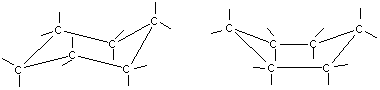
а - кресло б - ванна.
И в конформации кресла, и в конформации ванны связи вокруг каждого атома углерода имеют тетраэдрическое расположение. Отсюда - несравнимо большая устойчивость обычных циклов по сравнению с малыми циклами, отсюда - их возможность вступать в реакции замещения, но не присоединения.
Изомерия:
1. Структурная изомерия, связанная:
a) с числом углеродных атомов в кольце:
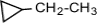 (этилциклопропан),
(этилциклопропан), 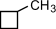 (метилциклобутан);
(метилциклобутан);
b) с числом углеродных атомов в заместителях:
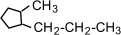 (1-метил-2-пропилциклопентан),
(1-метил-2-пропилциклопентан), 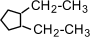 (1,2-диэтилциклопентан)
(1,2-диэтилциклопентан)
c) с положением заместителя в кольце:
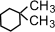 (1,1-диметилциклогексан),
(1,1-диметилциклогексан), 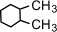 (1,2-диметилциклогексан)
(1,2-диметилциклогексан)
2. Межклассовая изомерия: циклоалканы изомерны алкенам.
3. Геометрическая цис-транс-изомерия:
Например, в молекуле 1,2-диметилциклопропана две группы СН3 могут находиться по одну сторону от плоскости цикла (цис-изомер) или по разные стороны (транс-изомер):
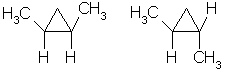
цис-изомер транс-изомер
Получение.
1. Отщепление двух атомов галогена от дигалогеналканов:
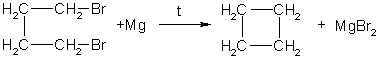
2. При каталитическом гидрировании ароматических углеводородов образуются циклогексан или его производные: C6H6 + 3H2 -t°,р,Ni→ C6H12.
Химические свойства.
1. Малые циклы (циклопропан и циклобутан) из-за большой напряженности кольца (малые углы) легко разрываются, вступая в реакции присоединения.
1) Гидрирование. При каталитическом гидрировании трех-, четырех- и даже пятичленные циклы разрываются с образованием алканов.
 (циклопропан) + H2 -120ºC,Ni CH3-CH2-CH3
(циклопропан) + H2 -120ºC,Ni CH3-CH2-CH3
 (циклопентан)+ H2-300ºC,PdCH3-CH2-CH2-CH2-CH3
(циклопентан)+ H2-300ºC,PdCH3-CH2-CH2-CH2-CH3
Пятичленный цикл разрывается только при высоких температурах.
2) Галогенирование. Циклопропан и циклобутан разрываются, присоединяя атомы галогена.
 + Br2 BrCH2-CH2-CH2Br (1,3- дибромпропан)
+ Br2 BrCH2-CH2-CH2Br (1,3- дибромпропан)
3)Гидрогалогенирование. Циклопропан и замещенные циклопропаны взаимодействуют с галогеноводородами с разрывом цикла.
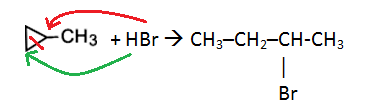
В случае замещенных циклопропанов реакция идёт в соответствии с правилом Марковникова.
Другие циклоалканы с галогеноводородами не реагируют.
2. Большие циклы - циклопентан и циклогексан - гораздо более устойчивы, цикл в них не разрывается. Они ведут себя подобно алканам, вступая в реакции замещения: галогенирование на свету, нитрование.
1) Галогенирование: циклопентан и циклопентан реагируют с галогенами на свету, вступая в реакцию замещения.
 + Cl2-(свет)
+ Cl2-(свет)  (хлорциклопентан) + HCl
(хлорциклопентан) + HCl
2) Нитрование.
Циклопентан + HNO3 -(t,p) нитроциклопентан + вода.
3. Дегидрирование. Производные циклогексана дегидрируются в производные бензола:
![]()
--300°C,Pd
![]()
+ 3H2
4. Горение. Как и любые органические вещества, циклоалканы горят с образованием углекислого газа и воды.


