- Преподавателю
- Химия
- Урок по теме Карбоновые кислоты
Урок по теме Карбоновые кислоты
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Султанова Е.А. |
| Дата | 16.04.2015 |
| Формат | doc |
| Изображения | Есть |
Министерство Образования Республики Казахстан


Учитель химии сш № 17
Г. Балхаш
Султанова Е.А.
Балхаш
Урок по теме: « Карбоновые кислоты» Учитель: Султанова Е.А.
Класс: 11 класс естественно- математического профиля. Сш № 17 г. Балхаш
Цель урока: В сравнительной характеристике с неорганическими кислотами познакомить с особенностью органических карбоновых кислот, показав их строение, зависимость свойств от строения, отработать умение применять методы сравнения, объяснять, делать выводы, наблюдать. Развивать логическое мышление, воспитывать интерес к науке.
План урока:
1. Организационный момент (1 мин)
2 Опрос: пары учитель - ученик, индивидуальный при помощи тестов на компьютере (4 варианта), фронтальный при помощи слайд - фильма, решение задач.
3. Введение новых знаний с элементами работы на компьютере по электронным учебникам, с решением задач исследовательского характера, с применением всемирной паутины «Интернет».
4. обобщение.
5. Д/з разноуровневое и творческое.
Учащиеся сидят по группам, на столе у каждой группы стоит компьютер.
В начале урока проводится опрос:
4 ученика работают на компьютере, проходят тестирование (4 варианта), создается 4 пары учитель - ученик, которые работают по домашнему заданию с контрольным вопросом учителя, 2 работают у доски, 1решает задачу, другой - цепочку превращений, одна группа работает на компьютере, имеет опережающее задание по теме урока. Остальные работают фронтально с учителем по слайд - вопроснику.
Задание группе: Используя электронный учебник «Кирилла и Мефодия», изучить общую характеристику карбоновых кислот: общая формула, гомологи, названия, строение функциональной группы, диссоциация.
Задание для учащихся у доски: 1. С →СН4 → С2Н2 →СН3СОН→С2Н5ОН
 ↓ ↓
↓ ↓
СО2 СН3СООН
2. Задача: На гидрирование 20,4 грамм смеси этаналя и пропоналя потрачено 8,96литров водорода. Рассчитайте % состав смеси. (отв.этаналя 46%)
После опроса учитель называет тему урока, а цели формулируют учащиеся. Итак, сегодня мы знакомимся со следующим классом кислородсодержащих органических веществ: карбоновыми кислотами. Одна из групп работала по общей характеристике этих соединений, используя электронный учебник им слово. Пока отвечает группа, учитель на доске выкладывает элементы опорной схемы.
С nH2n+1COOH ├ одно, двух изомерия: 1. угл.ск, 2. межкл.
nH2n+1COOH ├ одно, двух изомерия: 1. угл.ск, 2. межкл.
( RCOOH) много основные
RCOOH) много основные


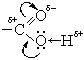
предельные СnH2n+1COOH↔ СnH2n+1COO- +
непредельные H+
ароматические Ф: Ж,з,Н2О х, М> в Н2О <,
С8Н17 СООН тв. з, …
НСООН - метановая
СН3СООН - этановая
С 9Н19СООН - декановая
Изомерию показывает через Flach фильм по Интернету.
Работа по электронному учебнику: Откройте электронные учебники, найдите в уроке «Карбоновые кислоты» тренажер по номенклатуре карбоновых кислот (фрагмент №3), у вас есть 1 минута, чтобы назвать вещество.
Гипотеза: Если карбоновые кислоты диссоциируют с образованием катиона водорода, то они должны иметь общие свойства с неорганическими кислотами.
Вы, используя электронные учебники, и эксперимент составьте мини- проблему и докажите её решение экспериментом.
1 группа: действие индикаторов на кислоты.
Дано: НCl, H2SO4, СН3СООН, индикаторы: лакмус, метиловый оранжевый.
Задание 1: Проверьте выданные кислоты на индикатор, сделайте выводы.
Гипотеза: Если карбоновые кислоты имеют общие свойства с неорганическими кислотами, значит …
Задание 2: Проверьте наличие кислот в яблоке и лимоне, капните на срезы фруктов индикаторами, сделайте выводы.
Гипотеза: Если срезы фруктов изменят цвет индикаторов, то в их составе …
Вывод: Карбоновые кислоты ….., значит их общие свойства обусловлены …, как у неорганических кислот.
2 группа: взаимодействие кислот с металлами и оксидами металлов.
Дано: НCl, H2SO4, СН3СООН, Fe,CuO.
Задание: Проведите реакции кислот с металлом и оксидом металла, сделайте выводы.
Гипотеза: Если карбоновые кислоты имеют общие свойства с неорганическими кислотами, значит …
Вывод: Карбоновые кислоты ….., значит их общие свойства обусловлены …, как у неорганических кислот.
3 группа: Взаимодействие кислот с основанием.
Дано: НCl, H2SO4, СН3СООН,NaOH, фенолфталеин.
Задание: Проведите реакцию кислот со щелочью, добавьте в щелочь индикатор, добавьте кислоту, сделайте вывод.
Гипотеза: Если карбоновые кислоты имеют общие свойства с неорганическими кислотами, значит …
Вывод: Карбоновые кислоты ….., значит их общие свойства обусловлены …, как у неорганических кислот.
4 группа: Взаимодействие кислот с солями более слабых кислот.
Дано: НCl, H2SO4, СН3СООН, мел ( CaCO3).
Задание: Проведите взаимодействие кислот с карбонатом кальция, сделайте вывод.
Гипотеза: Если карбоновые кислоты имеют общие свойства с неорганическими кислотами, значит …
Вывод: Карбоновые кислоты ….., значит их общие свойства обусловлены …, как у неорганических кислот.
5 Группа: Специфические свойства карбоновых кислот.
Задание: Используя электронный учебник, объясните специфические свойства карбоновых кислот (муравьиной и уксусной), при помощи компьютера продемонстрируйте реакцию серебряного зеркала для муравьиной кислоты.
Гипотеза: Если карбоновые кислоты имеют радикал, который отличает их от неорганических кислот, то …
Вывод: Карбоновые кислоты ….., значит их специфические свойства обусловлены ….
Каждая группа защищает свое мини - исследование.
Помимо названных свойств карбоновых кислот, у них есть свойство взаимодействовать со спиртами. Как называется данная реакция?
Демонстрация видеоролика о реакции этерификации.
Х: Индикатор → Меняет цвет
Ме→СnH2n+ 1COOМе +H2
МеО→ СnH2n+ 1COOМе + H2О
СnH2n+1COOH МеОН→ СnH2n+ 1COOМе + H2О
МеХ→ СnH2n+ 1COOМе + HХ
Н2→ СnH2n+ 1CН2OН
Сl2→ СlСnH2nCOOH + HCl Применение: мыла, …
NH4OH→ СnH2n+ 1CONH2
ROH→ СnH2n+ 1COOR + H2
 О
О

 Р2О5→ СnH2n+ 1C
Р2О5→ СnH2n+ 1C
 O + H2О
O + H2О

 СnH2n+ 1C
СnH2n+ 1C
Ангидриды O
Получение: Информация из Интернета.
Применение по электронным учебникам.
Обобщение: Мы с вами сегодня разобрали особенности карбоновых кислот, сравнили их с неорганическими, увидели их особенности, давайте вспомним все, о чем мы сегодня узнали. И так первый вопрос мой, кто на него отвечает, тот задает вопрос любому. (3 минуты)
Обобщение в группах.
На столах у вас лежат задания, вы можете получить дополнительную оценку за его выполнение, рядом указаны баллы, набрав 5, вы получите дополнительно «5».
Задания: 1. Составьте по общей формуле карбоновых кислот представителей этого класса, если:
1в. n = 3,5,7
2в. n = 2,4,6
3в. n = 4,6,8
4в. n = 3,4,9
Назовите их(1балл)
Задание: 2. Напишите по 2 изомера каждого вида для карбоновых кислот, если
1в. n = 5,7
2в.n = 4,6
3в. n = 5,8
4в. n = 7,8
Назовите их. (2 балла)
Задание: 3. Опишите при помощи уравнений реакций химические свойства карбоновых кислот, если
1в. n = 5,7
2в.n = 4,6
3в. n = 5,8
4в. n = 7,8
Назовите продукты. (3 балла)
Задание: 4. Дано: Na, S, SO2, Na2O, НCl, H2SO4, СН3СООН, Fe,CuO, NaOH, Cu(OH)2, C3H7OH, P2O5 (t0), O2, Ag2O(NH3), Cl2
C какими из перечисленных веществ будет реагировать карбоновая кислота, если :
1в. n = 5,7
2в.n = 4,6
3в. n = 5,8
4в. n = 7,8 (4 балла)
Задание: 5. Составьте генетическую цепочку превращений и решите её для карбоновой кислоты, если:
1в. n = 5,7
2в.n = 4,6
3в. n = 5,8
4в. n = 7,8
Итоги, оценки.
д/з.1 . по учебнику гл 10 § 10.1 - 10.6, стр. 210-211
«5» в.8-12, «4» в.4-8, «3» в.1-4
2. Домашняя практическая работа (мини- исследование), Купите в аптеке таблетки фенолфталеина, раздробите их, растворите полученное в воде, слейте прозрачный раствор, это ваш индикатор, проверьте раствор соды на него, проведите реакцию нейтрализации с уксусной и лимонной кислотами, проверьте другие свойства этих кислот.


