- Преподавателю
- Химия
- ПУТЕШЕСТВИЕ В НЕОРГАНИЧЕСКУЮ ХИМИЮ
ПУТЕШЕСТВИЕ В НЕОРГАНИЧЕСКУЮ ХИМИЮ
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Верещагина Н.В. |
| Дата | 09.02.2015 |
| Формат | doc |
| Изображения | Есть |
17
ПУТЕШЕСТВИЕ В НЕОРГАНИЧЕСКУЮ ХИМИЮ
Урок-игра
-
Цели: закрепить умения сравнивать, сопоставлять, анализировать;
-
продолжить развитие логического мышления, умения использовать теоретические знания в новых ситуациях;
-
воспитывать чувство коллективизма, взаимопомощи и взаимовыручки.
-
Задачи: Повторить и систематизировать знания учеников о классификации, номенклатуре, свойствах основных классов неорганических соединений;
-
закрепить умение решать расчетные задачи и записывать химические свойства классов уравнениями реакций;
Оборудование:
-
на столах учащихся конверты с заданиями, чистые листы; на столе ассистентов (2 старшеклассника) конверт с ответами, решениями упражнений.
-
на демонстрационном столе: наборы реактивов для лабораторного опыта (пронумерованные склянки с растворами, фенолфталеин, лакмус, пробирки);
-
на доске эпиграф:
"Человек рождается на свет,
Чтоб творить, дерзать, а не иначе,
Чтоб оставить в жизни добрый след
И решить все трудные задачи"
Учитель: Ребята, мы с вами закончили изучение важной темы "Классы неорганических соединений". Чтобы обобщить знания о составе, классификации и свойствах веществ, мы отправляемся в путешествие по удивительной стране Химляндии. Нам с вами предстоит пройти немало испытаний, побывать в городах этой удивительной страны. Прежде чем отправиться в путешествие, надо выяснить, какой багаж вы приготовили, что вам поможет в путешествии.
Класс разделим на две туристические группы.
I. Актуализация знаний (повторение изученного ранее учебного материала в обобщенном виде).
Учитель проводит фронтальный опрос с одновременным составлением схемы на доске и в тетрадях учащихся.
Схема
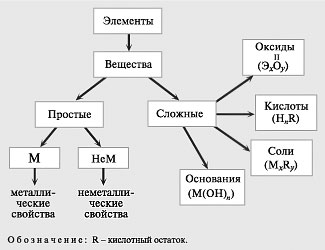
Вопросы:
![]() дать определение понятия «элемент»;
дать определение понятия «элемент»;
![]() какие вещества называются простыми, сложными;
какие вещества называются простыми, сложными;
![]() перечислить физические свойства, характерные для металлов, неметаллов;
перечислить физические свойства, характерные для металлов, неметаллов;
![]() дать определение оксидам, кислотам, солям, основаниям.
дать определение оксидам, кислотам, солям, основаниям.
Умницы!
Я вижу, что вы неплохо подготовились к путешествию.
А теперь вы отправляетесь в путь. Счастливого вам пути !
Первый город, который мы посетим, -это «Сложные вещества»,где вы примите участие в аукционе знаний.
Первая остановка
Аукцион знаний
1. Соли азотной кислоты (Нитраты).
2. Вещества, состоящие из двух элементов (Бинарные соединения).
3. Сложные вещества, состоящие из ионов металлов и кислотных остатков (Соли).
4. «Хлеб» Химической промышленности (Серная кислота).
5. Основность угольной кислоты (Два).
6. Растворимые основания (Щёлочи).
7. Соли соляной кислоты (Хлориды)
8. Оксид водорода (Вода)
9. Сложные вещества, состоящие из атомов водорода и кислотных остатков (Кислоты)
10. Вещества, с помощью которых можно определить кислоту и щёлочь (Индикаторы)
11. Сложные вещества, состоящие из катионов металлов и гидроксид-анионов (Основания)
12. Формула негашёной извести (CaO)
13. Формула гашёной извести (Са(ОН)2)
14. Соли серной кислоты (Сульфаты)
15. Формула азотной кислоты (HNO3)
16. Формула хлорида натрия (NaCl)
17. Формула фосфорной кислоты (H3PO4)
18. Формула углекислого газа (СО2)
19. Соли фосфорной кислоты (Фосфаты)
20. Формула угольной кислоты (Н2СО3)
А сейчас мы подъезжаем к удивительному городу «Эврика», где вам предстоит блеснуть эрудицией.
Вторая остановка
«Интеллектуальная».
Кроссворд
6
1
О
К
С
И
Д
Ы
2
Б
И
Н
А
Р
Н
Ы
Е
3
О
С
Н
О
В
А
Н
И
Я
4
С
О
Л
И
О
5
И
Н
Д
И
К
А
Т
О
Р
Ы
Ы
Вопросы к кроссворду:
-
1)Сложные вещества, состоящие из двух элементов, один из которых кислород со степенью окисления (-2). -
2)Вещества, состоящие из двух химических элементов.
-
3)Сложные вещества, состоящие из ионов металлов и связанных с ними одного или нескольких гидроксид ионов.
-
4)Сложные вещества, состоящие из ионов металлов и кислотных остатков.
-
5)Вещества-указатели. С их помощью определяют кислоты, щелочи и другие вещества.
-
6)Сложные вещества, молекулы которых состоят из атомов водорода и кислотных остатков.
Мы у города «Оксиды»,здесь необходимо показать практические умения по составлению формул оксидов.
Третья остановка
«Оксиды»
Составьте формулы оксидов
Учитель: Эти вещества очень распространены в природе, к ним относят такие хорошо известные соединения, как : песок, вода, углекислый газ, глина. Угадали, куда мы пришли? Правильно, это город, где живут ОКСИДЫ.
Задание: Составьте формулы названных в тексте оксидов. Прочитайте текст.
1 команда: В земной коре-литосфере находятся оксид алюминия
________________(глина), оксид кремния (4)
________________(песок), оксид железа (3)
________________(содержится в красном железняке)
2команда:
Водная оболочка Земли - гидросфера - это оксид водорода ________.
В воздухе есть оксид углерода (4) _________ (углекислый газ).
3 команда: В результате хозяйственной деятельности человека образуются вещества, загрязняющие атмосферу:
оксид углерода (2) _________(угарный газ),
оксид серы(4) _______(сернистый газ),
оксид азота (2) и оксид азота (4) ___________.
1 ученик зачитывает текст, другой ученик от команды пишет формулы на доске.
Подведение итогов. Спасибо за знания!
Едем дальше.
Перед нами достопримечательности города «Загадочный»
Четвертая остановка
«Капитанская»
Ребята! Нам путь преградил шлагбаум. Для того, чтобы проехать дальше, нам должны помочь наши капитаны.
Капитаны должны отгадать загадки, тогда мы продолжим свое путешествие.
Отгадай загадки:
1 команда:
Ах, что же я поделаю с собой -
Ведь в щелочи я сине-голубой.
А в кислоте быть синим я не смею: Я ...,
И в кислотах я краснею (фенолфталеин).
Их получают путем горения,
Или сложных веществ разложением.
В них два элемента, один - кислород.
Я отнесу к ним и известь и лед. (Оксиды).
Они имеют кислый вкус,
В них изменяет цвет лакмус,
А если активный металл попадет
Получим мы соль и еще водород.(Кислоты).
2 команда:
Как на прогулке от мороза,
От кислого я стану розов.
Но вид мой в щелочи смешон:
Я сразу желтый, как лимон.
В каких веществах у фенолфталеина
Бывает не жизнь, а сплошная малина?
Хлориды и нитраты,
Сульфаты, карбонаты. (Щелочи).
Я без труда и боли
Объединю кислоту и основание в класс . . . (Соли).
Молодцы! Справились с заданием. Шлагбаум поднять- и мы можем отправляться в путь.
Будьте осторожны! Впереди город «Непредсказуемый»
Пятая остановка
«Опасный поворот»
Расшифровав запись на асфальте дороги ,сможем безопасно тронуться в путь.
Расшифровать:
Начав движение с верхней левой клетки и передвигаясь по горизонтали (налево или направо) или вертикали (вверх или вниз), пройдите все клетки таким образом, чтобы из букв, приведённых в клетках, получилось правило по мерам предосторожности при обращении с химическими реактивами.
х
и
р
е
а
к
п
р
о
б
о
у
с
и
м
е
и
и
т
я
з
ь
а
в
к
в
ч
е
с
к
в
ы
н
е
л
т
ь
н
а
Ответ: Химические реактивы нельзя пробовать на вкус.
Физминутка.
А теперь послушайте, что может быть, если не соблюдать правила по технике безопасности:
-
При работе с веществами
Не берите их руками,
И не пробуйте на вкус,
Реактивы - не арбуз:
Слезет кожа с языка,
И отвалится рука.
-
Если на руку тебе кислота или щёлочь попала,
Руку быстро промой ты водой из-под крана.
И, чтоб осложнений себе не доставить.
Не забудь учителя в известность поставить.
-
В кислоту не лей ты воду,
-
А совсем наоборот:
Тонкой струйкой подливая, осторожненько мешая,
Лей в водичку кислоту -
Так отвадишь ты беду. -
А сейчас мы подъезжаем к городу «Эксперимент»,нам необходимо повторить правила безопасности жизнедеятельности.
Шестая станция
«Индикаторная»
Осторожно выдвигайте столик для выполнения опытов.
Найдём в ящике с реактивами сульфат меди (это № 34). Нальём в пробирку №1 1-2мл сульфата меди и опустим в пробирку железный гвоздь. Через несколько секунд вы увидите, что….
Так что же вы увидели? Гвоздик покрылся красным налётом. Что это? Это - медь.
Напишите уравнение реакции:
CuSO4 + Fe → ( CuSO4 + Fe = FeSO4 + Cu ), реакция замещения.
(обучающиеся пишут уравнение на доске, одновременно на экране -уравнение).
2)Возьмём реактив гидроксид натрия. Нальём в пробирку №2 1-2мл щёлочи и добавим 1-2 мл сульфата меди (это - CuSO4 ), видим …. (синий осадок).
Запишем уравнение реакции:
CuSO4 + 2NaOH = Na2SO4 + Cu(OH)2↓ , реакция обмена.
Определить.
В двух пробирках даны растворы веществ, среди них есть кислота и щелочь. Ваша задача в течение 1 минуты определить , в какой пробирке кислота, а в какой- щелочь, пользуясь индикаторами. Свой ответ поясните. В это время задание командам: Отгадать загадки (про индикаторы).Молодцы!
Перед вами город «Знаков». Не робейте!
Седьмая остановка.
«Химическая дорожка»
Впереди дорожка веществ. Здесь живут оксиды, кислоты, щелочи, соли. Я поздравляю Вас, вы успешно добрались до города. Если хотите быть другом этих веществ, вам придется выполнить еще одно задание, но уже каждый за себя (задание дифференцированное).
Задание на дорожке:
-
1. Составить формулы:
-
оксид фосфора (5)
-
гидроксида меди (2)
-
сульфата алюминия
Дайте названия веществам, формулы которых приведены ниже:
-
HCL
-
SO3
-
CaCO3
3. Укажите, какие кислоты и основания соответствуют приведенным ниже оксидам:
а) SiO2 - ... , P2O5 - ... , SO3 - ... ,
б) MgO - ... , Na2O - ... , Al2O3 - ... .
Все ли кислоты и основания можно получить растворением этих оксидов в воде?
-
Дать название веществам:
1-ая команда
NaCl; K2CO3; Ba(NO3)2; MgCl2; Li3PO4; CuCl2
2-ая команда
Na2CO3; KCl ; Mg(NO3)2 ; Na2SiO3 ; ZnS ; ZnSO4
Затем обмениваются карточками, проверяют друг друга, исправляют ошибки, оценку ставят карандашом.
Ответы написаны на доске:
-
Р2О5, Cu(OH)2, AL2(SO4)3
-
Соляная кислота, оксид серы (6), карбонат кальция
-
H2SiO3, H3PO4, H2SO4, Mg(OH)2, NaOH, Al(OH)3. Нет.
-
Натрия хлорид, калия карбонат, бария нитрат, магния хлорид, лития фосфат, хлорид меди, карбонат натрия, хлорид калия, нитрат магния, силикат натрия, сульфид цинка, сульфат цинка.
Благодарю за хорошую работу!Впереди очень интересный город-город Игр.
Восьмая остановка
«Крестики-нолики»
А сейчас я предлагаю вам игру «крестики-нолики».
Задание: Выделить соли.
Ba(OH)2
Mg3(PO4)2
K2O
H2O
HBr
FeBr3
Na2SO4
CuCl2
Ca(NO3)2
Задание: Выделить кислоты.
NaCl
Fe2O3
HNO3
CO2
HCl
BaSO4
H2SO4
H2O
Ca(NO3)2
Задание:
2. Впишите формулы оксидов указанных элементов в соответствующие клетки (по стрелкам).
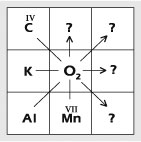
Ребята, вы порадовали меня своими знаниями, и мы можем продолжать путешествие. Мы в центре города Умельцев.
Девятая остановка
«Эстафетная»
Внимание! У нас закончилось топливо. Для того чтобы произвести заправку, нам необходимо собрать деньги и купить его. Вы должны проявить знания для достижения цели. Вам предлагают осуществить цепочку превращений.
Задание:
Осуществить превращения и указать тип реакции
1 Команда.
Cu ↔ CuO →СuС12 → Сu(NО3)2 →Cu
2 Команда.
Са → СаО → Са(ОН)2 → СаCO3 → CaO
Задание:
Написать всевозможные реакции.
-
1)HCl, CaO, H2O, Na2SO4, NaOH, Zn.
-
2)CuO, H2SO4, NaOH, SO3, H2O, Ca.
Задание:
Получить всевозможными способами MgCl2.
Умницы! Автобус заправлен, и мы можем отправляться в путь.
Мы завершаем путешествие.
Десятая остановка
«Расчетная»
На этой вынужденной остановке, нам необходимо произвести подсчет денежных средств для дальнейшего путешествия.
Задачи:
-
1)Найти относительную плотность метана по воздуху.
-
2)Вычислить количество вещества, содержащегося в 17 г. Сероводорода. Сколько молекул содержится в данном образце сероводорода? Сколько атомов водорода?
3) Сформулируйте условие задачи и решите ее:
Mgo2 моль + H2х л. →…
По вашим подсчетам мы определили, что для продолжения путешествия нам недостаточно средств. Пора возвратиться домой, но вы не расстраивайтесь, путешествие будет продолжено по теме: «Периодическая система Д.И Менделеева».
Рефлексия:
Потопайте ногами, если вы с этим утверждением согласны:
1. Мне было очень интересно на уроке.
2. Я узнал много нового и познавательного.
3. Я принимал активное участие во всех этапах урока.
4. Мне нравится такая форма урока.
Домашнее задание:
Во время путешествия вы купили сувениры своим родителям:
а) алюминий;
б) ортофосфорную кислоту;
в) оксид серы(IV);
г) водорода оксид;
д) оксид кальция;
е) щелочь.
Необходимо составить формулы сложных веществ и написать возможные уравнения реакций.


