- Преподавателю
- Химия
- ОСУД и тренажер по теме оксиды
ОСУД и тренажер по теме оксиды
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Леонтьева Е.А. |
| Дата | 21.04.2015 |
| Формат | docx |
| Изображения | Есть |

Кислотным оксидам соответствуют кислоты
P2O5→H3PO4
SO3→H2SO4
P2O5+3H2O→2H3PO4
CO2+H2O→H2CO3
SO3+H2O→H2SO4
Амфотерным оксидам соответствуют и основания и кислоты
Al2O3→Al(OH)3
Al2O3→H3AlO3→HAlO2
Al2O3+6HCl→2AlCl3+3H2O
Al2O3+2KOH→2KAlO2+H2O
Основным оксидам соответствуют основания
CaO→Ca(OH)2
Na2O→NaOH
CaO+H2O→Ca(OH)2
Na2O+H2O→2NaOH
Кислотные
P2O5,SO3,CO2,Mn2O7
(все неМе и Ме с валентностью V,VI,VII)






Несолеобразующие
CO,NO,N2O,SiO
солеобразующие
Амфотерные
Al2O3,ZnO,BeO,PbO
(Ме с валентностью II, III, IV)
Основные
CaO, CuO,Na2O
(Ме с валентностью I,II)
классификация
Взаимодействие простых веществ с кислородом
2Ba+O2→2BaO
C+O2→CO2
4Al+3O2→2Al2O3
Разложение солей при нагревании
CaCO3→CaO+CO2
MgCO3→MgO+CO2
Разложение нерастворимых оснований при нагревании
Cu(OH)2→CuO+H2O
2Fe(OH)3→Fe2O3+3H2O
Взаимодействие сложных веществ с кислородом
2CO+O2→2CO2
2NO+O2→2NO2
CH4+2O2→CO2+2H2O
получение
если






 ОСУД Х 8 ОКСИДЫ 1.
ОСУД Х 8 ОКСИДЫ 1.
Номенклатура
Слово оксид+название элемента в Р.п.(валентность)
Fe2O3 - оксид железа(III)
ОСУД Х 8 Оксиды 2. Химические свойства.
оксид+щелочь=соль+вода
Al2O3 + 2NaOH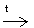 H2O + 2NaAlO2
H2O + 2NaAlO2
ZnO + 2NaOH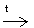 H2O + Na2ZnO2
H2O + Na2ZnO2
оксид+кислота=соль +вода
Al2O3 +3H2S04 = Al2(SO4)3 + 3H2O
оксид+вода≠
Al2O3 + H2O ≠
оксид+щелочь=соль+вода
SO2 + 2KOH = K2SO3 + H2O
(H2SO3)
SO2 + KOH = KHSO3
(H2SO3)
P2O5 + 6NaOH = 2Na3PO4 + 3H2O
(H3PO4)
оксид+основной оксид=соль
3CaO + P2O5 = Ca3(PO4)2
(H3PO4)
оксид+вода=кислота
SO2 + H2O = H2SO3
P2O5 + 3H2O = 2H3PO4
оксид +кислотный оксид=соль
CaO + СO2 = CaCO3
FeO + SO3 = FeSO4
оксид+вода=гидроксид
ВaO + H2O = Вa(OH)2
Na2O + H2O = 2NaOH
оксид + кислота = соль + вода
CaO + 2HCl = CaCl2 + H2O
CuO + 2HF = CuF2 + H2O
3Na2O + 2H3PO4 = 2Na3PO4 + 3H2O
амфотерный
кислотный
основной
если


