- Преподавателю
- Химия
- Конспект урока по теме Неметаллы
Конспект урока по теме Неметаллы
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Голощапова Н.М. |
| Дата | 01.02.2015 |
| Формат | doc |
| Изображения | Есть |
Эпиграф урока:
Найдется ль правило простое,
Что целый мир объединит?
Таблицу Менделеев строит,
Природы ищет Алфавит.
С. Щипачев «Читая Менделеева»
Тема урока НЕМЕТАЛЛЫ
Тип урока: повторительно - обобщающий.
Цели:
обобщающая: обобщить знания об особенностях строения атомов неметаллов; закрепить умения определять степени окисления элементов атомов; составлять уравнения химических реакций, характеризующих свойства неметаллов, научить составлять краткие сообщения, работая с дополнительной литературой, расширить кругозор учащихся.
развивающая: формирование умений сравнивать, обобщить свойства неметаллов и их соединений на основе положения химических элементов в ПСХЭ.
воспитательная: развитие познавательной активности, чувства ответственности, уважения друг к другу, взаимопонимания, уверенности в себе.
Оборудование: Таблица ПСХЭ, Д.И.Менделеева, справочный материал, карточки-задания, видеофильм - «Углерод», кристаллическая решетка графита и алмаза.
Ход урока
Ι. Организационный момент. Проверка готовности к уроку, выявление отсутствующих.
ΙΙ. Актуализация знаний.
«Мозговой штурм»
-
Наиболее активный металл? (Фтор)
-
В какой капусте много йода? (Ламинария)
-
Название, какого элемента неметалла состоит из названия двух млекопитающих? (Мышьяк)
-
В атмосфере какого неметалла вода горит ярким пламенем?(Фтор)
-
Оксид водорода? (Вода)
-
Назовите два самых распространенных неметалла во Вселенной? (Водород и гелий)
-
М.В.Ломоносов в статье, опубликованной в 1745 г., писал «При растворении какого - либо неблагородного металла, особенно железа, в кислотах из отверстия склянки вырывается горючий пар». Что это за вещество? (Водород)
-
Самое твердое из известных веществ? (Алмаз)
-
Какой элемент составляет основу органической жизни на Земле? (Углерод)
-
Графит и алмаз, что это? (Аллотропные видоизменения)
-
Сколько валентных электронов в атоме химического элемента имеющего порядковый номер 17? (семь)
-
Этот газ входит в состав воздуха, он поддерживает горение и дыхание? (Кислород)
-
Другое название хлороводородной кислоты? (Соляная)
-
Назовите галоген, у которого электроны расположены на трех энергетических уровнях? (Хлор)
-
В ней лакмус краснеет? (Кислота)
-
Как называют соли серной кислоты? (Сульфаты)
-
Этот оксид самое распространен6ное и необходимое вещество на нашей планете? (Вода)
-
Эта кислота в свободном виде не существует, так как разлагается на воду и углекислый газ? (Угольная кислота)
-
Оксид, какого неметалла образуется при спиртовом брожении? (Углерода)
-
Самый легкий неметалл? (Водород)
-
Эта кислота в воде почти не растворима? (Кремневая)
-
Как называется вещество, формула которого NH3? (Аммиак)
-
Назовите жидкий неметалл? (Бром)
-
Эти вещества получают реакцией окисления простых веществ? (Оксиды)
ΙΙΙ. Работа в малых группах
Студенты разделены на 4 группы, каждая группа имеет свое название.
Названия малых групп:
Группа №1. Элементы неметаллов
Группа №2. Окислители-восстановители
Группа №3. Оксиды и гидроксиды
Группа№4. Аллотропные модификации
Каждая группа получает задания, готовят выступления
Задание группе №1
-
Дать сравнительную характеристику элементов неметаллов в соответствии с положением в ПС
-
На основании строения атомов доказать закономерности в изменении неметаллических свойств
Задание группе №2
-
Электроотрицательность, степень окисления неметаллов
-
Окислительно-восстановительные свойства неметаллов
Задание группе №3
-
Каковы закономерности изменения кислотного характера оксидов и гидроксидов в периодах и группах в зависимости от положения неметаллов в ПС
Задание группе №4
-
Фосфор и его аллотропные видоизменения
-
Применение фосфора
ΙV. Показ видеофильма «Аллотропные модификации углерода»
V. Проверочная работа
Ι вариант
1. На примере соответствующих уравнений реакций:
а) 2P + 3H2 → 2PH3
б) P + 3Na → Na3P
Объяснить в каком случае фосфор проявляет:
а) окислительные свойства;
б) восстановительные свойства.
2. Сравнить неметалличность элементов: Cl, Br, J, F, O
Расположить элементы в порядке возрастания неметалличности.
3. Определить степень окисления каждого элемента:
O2, SO3, HClO4, H2SO4, NH3
4. Осуществить превращения, одно уравнение записать с электронным балансом:
а) S→SO2→ SO3→H2SO4→BaSO4
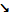
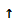
H2S
б) P→P2O5→H3PO4→Ca3(PO4)2
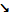
Ca3P2→PH3→P2O5
ΙΙвариант
1. На примере соответствующих уравнений реакций:
а) S + O2 → SO2
б) 3S + 2Al → Al2S3
Объяснить в каком случае сера проявляет:
а) окислительные свойства;
б) восстановительные свойства.
2. Сравнить неметалличность элементов: P, S, Si, Cl, H
Расположить элементы в порядке возрастания неметалличности.
3. Определить степень окисления каждого элемента:
Cl2, Na2O, H2CO3, H3PO4, PH3
4. Осуществить превращения, одно уравнение записать с электронным балансом:
а) Na3N→N2→ NO→NO2→HNO3→NaNO3
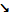
NH3
б) CH4→C→CO→CO2→Na2CO3→CaCO3
VΙ. Подведение итогов урока


