- Преподавателю
- Химия
- Конспект урока по химии _Химическая регата 8 класс
Конспект урока по химии _Химическая регата 8 класс
| Раздел | Химия |
| Класс | 8 класс |
| Тип | Конспекты |
| Автор | Бекирова А.Г. |
| Дата | 01.01.2016 |
| Формат | docx |
| Изображения | Есть |

 УРОК № ___
УРОК № ___
Дата «____» ___________ 20__ г.
Тема
Обобщающий урок-игра «Химическая регата»
Цель
повторить и обобщить знания об основных классах неорганических соединений, об их составе, названиях, классификации, физических свойствах; закрепить умение составлять формулы веществ по их названиям и давать названия веществам по их формулам. Активизировать умственную деятельность учеников, создать условия для взаимодействия и взаимопомощи учеников во время обучения.
Оборудование и материалы
карта-схема маршрута регаты, карточки с заданиями, карта оценивания «Судовой журнал», карта о. Неоргания
Базовые понятия и термины
оксиды, кислоты, основания, соли, индикаторы
Тип урока
урок обобщения и систематизация знаний.
ХОД УРОКА
-
мотивация учебной деятельности
Сообщение темы, определение цели и задания урока
-
Организационный этап
-
Распределение обязанностей
-
Ознакомление с маршрутом регаты вокруг о. Неоргания (Маршрутный лист)
-
Актуализация опорных знаний
Проверка готовности к плаванию.
-
Понятия необходимые для плавания (беседа)
-
Определение понятий «оксиды», «кислоты», «основания», «соли»
-
Обобщение и проверка знаний, умений и навыков
Игра-путешествие «Химическая регата»
-
«Штиль формул»
Выпишите отдельно формулы оксидов, кислот, оснований, солей
CuSO4, CaO, NaOH, Al(NO3)3, H2SiO3, CO2, HBr, Fe(OH)2, K2O, CaCO3, Al(OH)3, H2SO4, Cr2O3, K3PO4, Zn(OH)2, HPO3
-
Бухта «Оксиды»
-
Составьте формулы оксидов таких элементов:
Al, Na, S(VI), N(IV), Cl(VII), Ba, P(V), Fe(III)
-
Выбрать ряд соединений, который состоит только из оксидов
CrO3
FeO
HCl
Na2SO4
SiO2
SnO
H3PO4
N2O3
CO
-
Вычислите массовые доли элементов в оксиде углерода (IV)
-
«Кислотный риф»
-
Из приведенных формул выберите формулы серной, угольной, хлоридной, азотной, сульфидной, фосфорной кислот. Классифицируйте их по содержанию кислорода
Кислоты
H2SO4, H2CO3, H2SO3, HNO3, HCl, H2S, HBr, H3PO4, HI, HPO3
-
Задача. Вычислите массу 3 моль серной кислоты.
-
Дайте названия кислотам и классифицируйте их по основности
Кислоты
H2SO3, HBr, H3PO4, HNO3, H2SiO3
-
«Загадочный берег»
-
Их вкус нам привычен, приятен.
У них белый цвет, реже темный.
В природе всегда их так много.
Ну, как вы думаете: что это?
Ответ: _________________
-
Бинарными зовутся эти вещества.
В них, крепко взявшись за руки,
Два элемента соединились.
Какие вещества образовались?
Ответ: _________________
-
Их вкус узнаешь сразу ты.
Когда лимон иль яблоко возьмешь ты в рот,
От них все вещи нужно уберечь -
Такая у веществ работа.
Разрушат, разъедят, порвут…
Скажи: как вещества зовут?
Ответ: _________________
-
Двойное название имеют они,
Растворимы в воде бывают.
На кожу попадут - смейся и плачь.
Почувствуешь сразу ты -ОН.
Не про молочные реки и берега
Вели мы с вами речь, а об…
Ответ: _________________
-
«Щелочной залив»
-
Составьте формулы оснований:
-
гидроксид меди(II) __________________
гидроксид калия ____________________
гидроксид железа(III) _______________
гидроксид кальция __________________
гидроксид цинка ___________________
гидроксид алюминия ________________
гидроксид бария ____________________
гидроксид натрия ___________________
-
С помощью «Таблицы растворимости кислот, оснований и солей в воде» разделитеполученные основания на щелочи и нерастворимые основания.
Основания
Щелочи
Нерастворимые основания
-
Мыс «Индикатор»
Заполните таблицу известными вам индикаторами. Какую окраску имеют индикаторы в нейтральной, щелочной и кислой средах
Среда
Индикатор
Нейтральная
(вода)
Кислая
Щелочная
-
Полуостров «Соли»
Из предложенных ионов составьте формулы солей (не дописывая индексы) и назовите их.
Na+
Mg2+
Al3+
Ca2+
K+
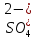
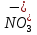
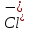
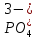
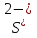
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
-
ПОДВЕДЕНИЕ ИТОГОВ УРОКА
По баллам в «Судовом журнале» учащиеся получают оценки
За каждый правильный ответ начисляется 1 балл.
Решенная задача - 1 балл.
Правильно выполненная классификация - 1 балл
Максимальное количество баллов за:
-
«Штиль формул» - 16 баллов
-
Бухта «Оксиды» - (8 + 1+ 1) = 10 баллов
-
«Кислотный риф» - (8 + 8 + 1) = 17 баллов
-
«Загадочный берег» - (1 + 1 + 1 + 1) = 4 балла
-
«Щелочной пролив» - (8 + 2) = 10 баллов
-
Мыс «Индикатор» - 16 баллов
-
Обогнуть полуостров «Соли» - (9 + 9) = 18 баллов
Итоговая таблица
-
Балл
Оценка
Балл
Оценка
1 - 7
1
48 - 55
7
8 - 15
2
56 - 63
8
16 - 23
3
64 - 71
9
24 - 31
4
72 - 79
10
32 - 39
5
80 - 87
11
40 - 47
6
88 - 91
12
-
ДОМАШНЕЕ ЗАДАНИЕ
-
Повторить § 7-8, 10 - 11,
-
Подготовиться к контрольной работе


