- Преподавателю
- Химия
- Контрольные работы к учебнику О. С. Габриеляна «Химия – 8»
Контрольные работы к учебнику О. С. Габриеляна «Химия – 8»
| Раздел | Химия |
| Класс | - |
| Тип | Тесты |
| Автор | Галиева О.В. |
| Дата | 07.05.2015 |
| Формат | doc |
| Изображения | Есть |

Контрольные работы
ХИМИЯ
К учебнику О. С. Габриеляна «Химия - 8»
8 класс
2014
Контрольные работы
ХИМИЯ
К учебнику О. С. Габриеляна «Химия - 8»
8 класс
2014
Галиева О.В.
Химия. 8* класс: Контрольные работы к учебнику О. С. Габриеляна «Химия - 8»
Пособие состоит из текстов контрольных работ в тестовой форме в параметрах ЕГЭ, соответствующих программе химии для 8 класса О. С. Габриеляна. Оно предназначено для проведения на уроках тематического и итогового контроля по основным темам курса.
Содержание
Контрольная работа № 1 Атомы химических элементов…………..........………………………. 5
Вариант 1…………………………………………………………………………………………………5
Вариант 2…………………………………………………………………………………………………7
Вариант 3 …………………………………………………….……………………..……………………9
Вариант 4………………………………………………………………………………..………………11
Контрольная работа № 2 Простые вещества. Количественные соотношения………………..13
Вариант 1……………………………………………………………..…………………………………13
Вариант 2………………………………………………………………………………………………..15
Вариант 3 ……………………………………………………………………………………………….17
Вариант 4………………………………………………………………………………………..………19
Контрольная работа № 3 Соединения химических элементов……………………..…………...21
Вариант 1………………………………………………………………………………………………..21
Вариант 2…………………………………………………………………………………..……………23
Вариант 3 ……………………………………………………………………………………………….25
Вариант 4………………………………………………………………………………………………..27
Контрольная работа № 4 Изменения, происходящие с веществами…………………….……..29
Вариант 1……………………………………………………….…………………………………….…29
Вариант 2………………………………………………………………………………………………..31
Вариант 3 ……………………………………………………………………………………………….33
Вариант 4………………………………………………………………………….…………………….35
Контрольная работа № 5 Классы неорганических соединений………………………………...37
Вариант 1…………………………………………………………………….……….…………………37
Вариант 2………………………………………………………………………………………………..39
Вариант 3 ……………………………………………………………………………………………….41
Вариант 4………………………………………………………………………………………………..43
Контрольная работа № 6 Итоговая контрольная работа за курс 8 класса……………………45
Вариант 1…………………………………………………………………………………………..……45
Вариант 2………………………………………………………………………………………………..47
Вариант 3 ……………………………………………………………………………………………….49
Вариант 4…………………………………………………………………………………………….….51
Приложения…………………………………………………………………………………………….53
Ответы…………………………………………………………………………………………………..55
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 1
Атомы химических элементов
ВАРИАНТ-1
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Элемент третьего периода главной подгруппы III группы ПСХЭ - это:
1) алюминий
3) магний
2) бериллий
4) бор
2. Обозначение изотопа, в ядре которого содержится 8 протонов и 10 нейтронов:
1) 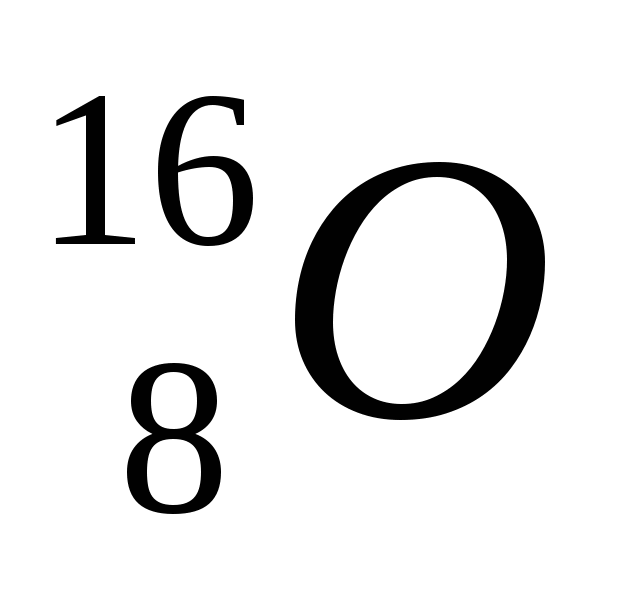
3) 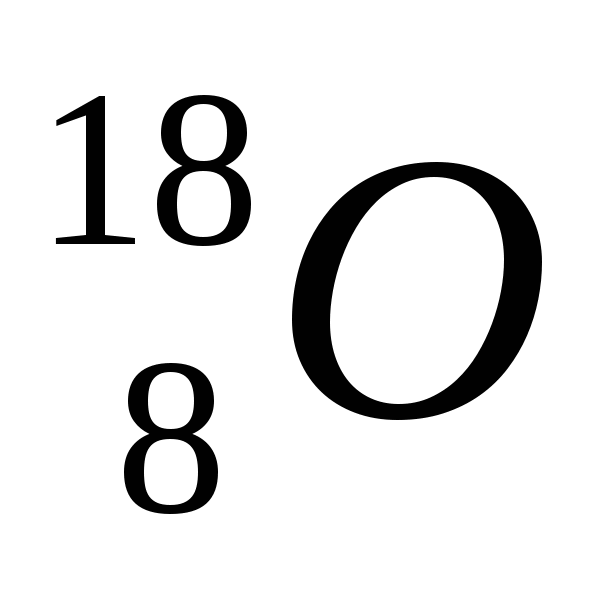
2) 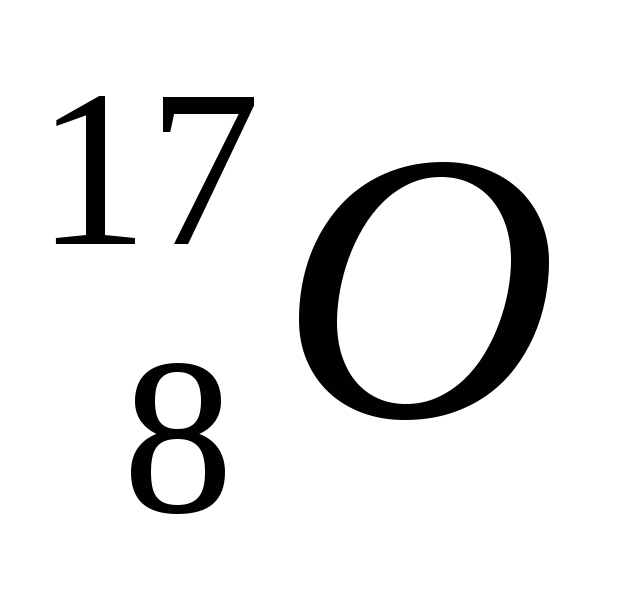
4) 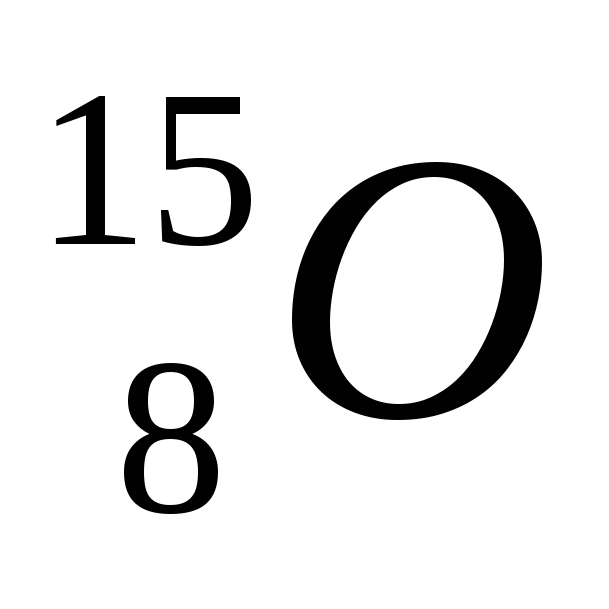
3. Атом химического элемента, электронная оболочка которого содержит 17 электронов:
1) кислород
3) хлор
2) сера
4) фтор
4. Два электронных слоя (энергетических уровня) имеет атом:
1) азота
3) калия
2) магния
4) гелия
5. Пара химических элементов, имеющих на внешнем электронном уровне по 5 электронов:
1) P и С
3) Si и Са
2) С и Si
4) N и P
6. Верны ли следующие высказывания?
А. В периоде металлические свойства атомов элементов с увеличением порядкового номера усиливаются.
Б. В периоде металлические свойства атомов элементов с увеличением порядкового номера ослабевают.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между частицей и распределением электронов по энергетическим уровням:
Частица:
Распределение электронов:
А) Ca
1) 2е, 8е, 8е, 2е
Б) Al3+
2) 2е, 8е, 2е
В) N3-
3) 2е, 5е
Г) N
4) 2е, 8е, 3е
5) 2е, 8е,18е,4е
6) 2е, 8е
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Соединениями с ионной связью являются:
1) NH3
3) BaCl2
5) ZnS
2) CO2
4) Al I3
6) O2
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до целых
9. Относительная молекулярная масса хлорида бария BaCl2 равна __________.
Часть 2
Запишите номер задания и полное решение
10. Дайте характеристику элемента c Z = 11 (Приложение 1, пункты I (1-5), II (1-3, 6, 7), V(1,2)). Запишите схему строения его иона Na+.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 1
Атомы химических элементов
ВАРИАНТ-2
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Элемент второго периода главной подгруппы III группы ПСХЭ - это:
1) литий
3) кальций
2) бор
4) магний
2. Обозначение изотопа, в ядре которого содержится 26 протонов и 30 нейтронов:
1) 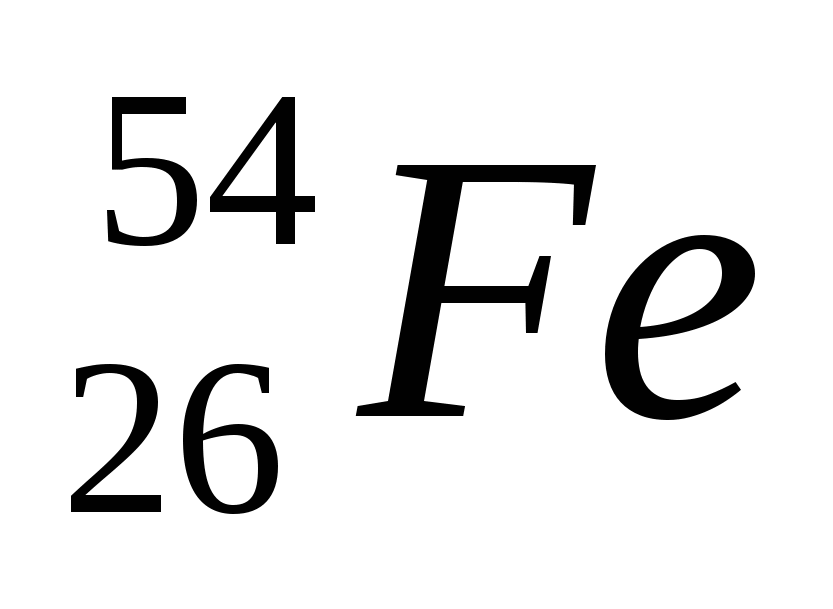
3)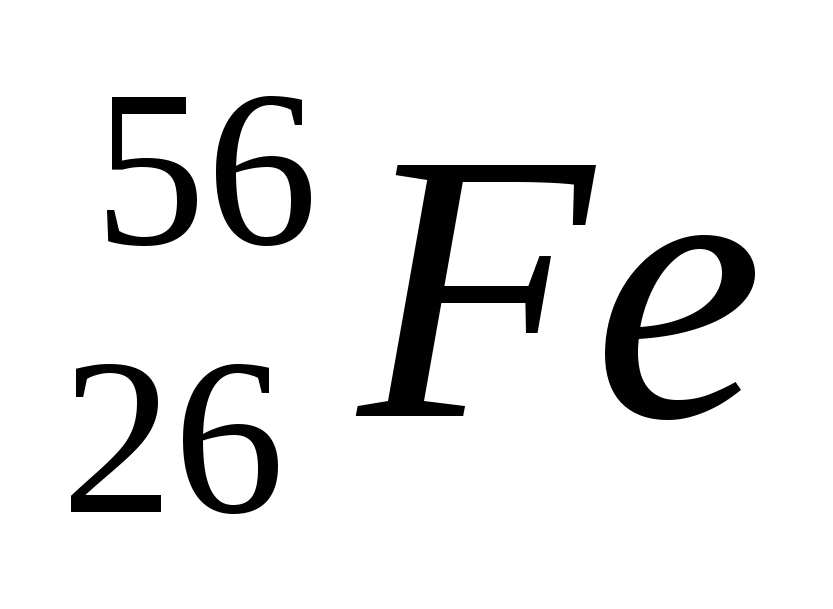
2)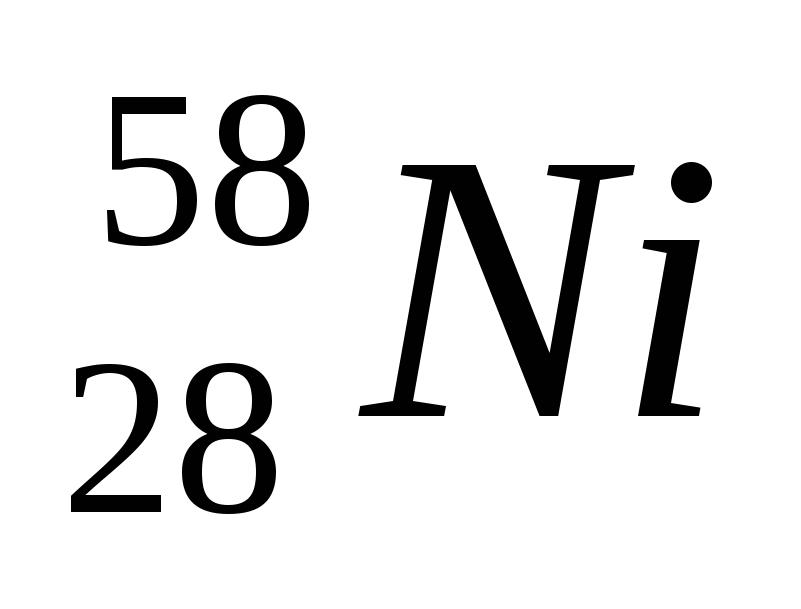
4)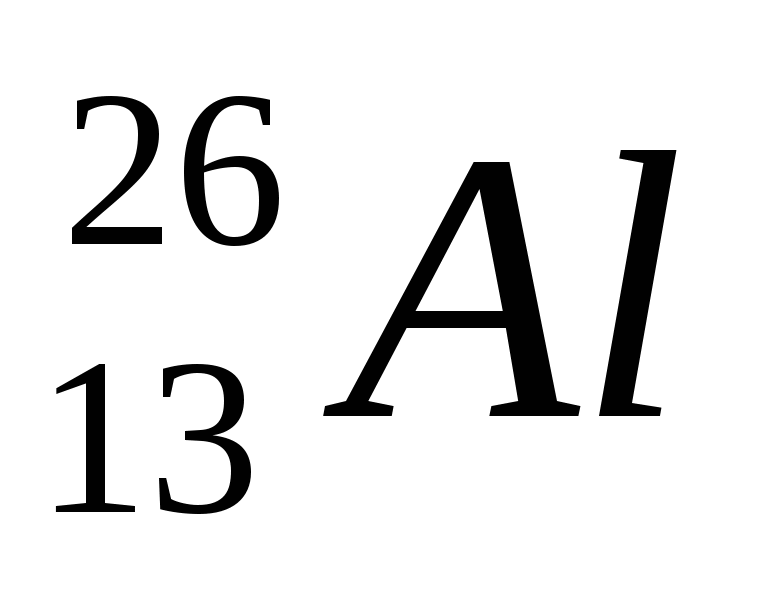
3. Атом химического элемента, ядро которого содержит 14 протонов - это:
1) азот
3) калий
2) кремний
4) цинк
4. Три электронных слоя (энергетических уровня) имеет атом:
1) бора
3) фтора
2) кальция
4) серы
5. Пара химических элементов, имеющих на внешнем электронном уровне по 3 электрона:
1) Mg и Al
3) N и S
2) O и S
4) B и Al
6. Верны ли следующие высказывания?
А. В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера усиливаются.
Б. В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера ослабевают.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между частицей и распределением электронов по энергетическим уровням:
Частица:
Распределение электронов:
А) Mg
1) 2е, 8е, 7е
Б) K
2) 2е, 8е, 2е
В) Na+
3) 2е, 7е
Г) Cl -
4) 2е, 8е, 8е
5) 2е, 8е
6) 2е, 8е, 8е,1е
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Соединениями с ковалентной полярной связью являются:
1) NH3
3) BaCl2
5) O2
2) CO2
4) H2S
6) ZnS
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до целых
9. Относительная молекулярная масса оксида алюминия Al2O3 равна _______.
Часть 2
Запишите номер задания и полное решение
10. Дайте характеристику элемента c Z = 16 (Приложение 1, пункты I (1-5), II (1-3, 6, 7), V(1,2)). Запишите схему строения его иона S2-.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 1
Атомы химических элементов
ВАРИАНТ-3
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Элемент третьего периода главной подгруппы V группы ПСХЭ - это:
1) азот
3) фосфор
2) алюминий
4) углерод
2. Атом химического элемента, имеющий в своем составе 9 протонов, 10 нейтронов, 9 электронов:
1) бор
3) фтор
2) бериллий
4) калий
3. Атом химического элемента, электронная оболочка которого содержит 10 электронов:
1) кальций
3) неон
2) фтор
4) бор
4. Четыре электронных слоя (энергетических уровня) имеет атом:
1) железа
3) углерода
2) бария
4) аргона
5. Пара химических элементов, имеющих на внешнем электронном уровне по 4 электрона:
1) углерод и кремний
3) азот и углерод
2) азот и фосфор
4) калий и кальций
6. Верны ли следующие высказывания?
А. В периоде неметаллические свойства атомов элементов с увеличением порядкового номера не изменяются.
Б. В периоде неметаллические свойства атомов элементов с увеличением порядкового номера ослабевают.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между частицей и распределением электронов по энергетическим уровням:
Частица:
Распределение электронов:
А) C4+
1) 2е, 6е
Б) Li
2) 2е, 1е
В) O
3) 2е, 8е, 3е
Г) S2-
4) 2е, 8е, 8е,1е
5) 2е, 8е, 8е
6) 2е
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Соединениями с ионной связью являются:
1) NaCl
3) K
5) CuO
2) H2
4) ZnI2
6) HCl
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Относительная молекулярная масса нитрата калия KNO3 равна __________.
Часть 2
Запишите номер задания и полное решение
10. Дайте характеристику элемента c Z = 14 (Приложение 1, пункты I (1-5), II (1-3, 6, 7), V(1,2)). Запишите схему строения его иона Si 4+.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 1
Атомы химических элементов
ВАРИАНТ-4
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Элемент четвертого периода главной подгруппы II группы ПСХЭ - это:
1) натрий
3) калий
2) кальций
4) углерод
2. Атом химического элемента, имеющий в своем составе 15 протонов, 16 нейтронов, 15 электронов:
1) кислород
3) фтор
2) цинк
4) фосфор
3. Атом химического элемента, ядро которого содержит 24 протона - это:
1) хром
3) медь
2) магний
4) криптон
4. Пять электронных слоев (энергетических уровней) имеет атом:
1) брома
3) мышьяка
2) йода
4) бора
5. Пара химических элементов, имеющих на внешнем электронном уровне по 7 электронов:
1) кремний и фосфор
3) хлор и йод
2) азот и фосфор
4) серебро и кадмий
6. Верны ли следующие высказывания?
А. В главной подгруппе радиус атомов элементов с увеличением порядкового номера увеличивается.
Б. В главной подгруппе радиус атомов элементов с увеличением порядкового номера уменьшается.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между частицей и распределением электронов по энергетическим уровням:
Частица:
Распределение электронов:
А) S
1) 2е, 8е, 7е
Б) Ca2+
2) 2е, 8е, 4е
В) О2-
3) 2е, 8е
Г) Si
4) 2е, 8е, 6е
5) 2е
6) 2е, 8е, 8е
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Соединениями с ковалентной неполярной связью являются:
1) H2
3) Cl2
5) KCl
2) SO2
4) Na
6) C
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Относительная молекулярная масса сульфата натрия Na2SO4 равна _________.
Часть 2
Запишите номер задания и полное решение
10. Дайте характеристику элемента c Z = 20 (Приложение 1, пункты I (1-5), II (1-3, 6, 7), V(1,2)). Запишите схему строения его иона Ca 2+.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 2
Простые вещества. Количественные соотношения
ВАРИАНТ-1
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Больше металлических свойств проявляет:
1) магний
3) алюминий
2) натрий
4) железо
2. Аллотропная модификация кислорода:
1) графит
3) озон
2) белый фосфор
4) алмаз
3. Атому элемента, образующему простое вещество - металл, соответствует электронная схема:
1) +18Э)2)8)8
3) +3Э)2)1
2) +15Э)2)8)5
4) +8Э)2)6
4. Запись 3О2 означает:
1) 2 молекулы кислорода
3) 5 атомов кислорода
2) 3 молекулы кислорода
4) 6 атомов кислорода
5. Химическая связь является ковалентной неполярной в веществе:
1) железо
3) вода
2) хлор
4) соляная кислота
6. Верны ли следующие высказывания?
А. При нормальных условиях ртуть жидкая.
Б. При нормальных условиях ртуть твердая.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
Ответом к заданиям 7- 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
7. Масса 3 моль сероводорода Н2S равна ________г.
8. Количество вещества углекислого газа СO2, в котором содержится 36•1023 молекул, равно_____ моль.
9. Объем, который занимает 2 моль газообразного вещества с формулой SO2 (н.у.) равен ____л.
Часть 2
Запишите номер задания и полное решение
10. Рассчитайте объем для 160 г кислорода O2.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 2
Простые вещества. Количественные соотношения
ВАРИАНТ-2
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Больше неметаллических свойств проявляет:
1) углерод
3) фтор
2) азот
4) кислород
2. Аллотропная модификация углерода:
1) озон
3) красный фосфор
2) сера кристаллическая
4) алмаз
3. Атому элемента, образующему простое вещество - неметалл, соответствует электронная схема:
1) +11Э)2)8)1
3) +12Э)2)8)2
2) +8Э)2)6
4) +4Э)2)2
4. Запись 5N2 означает:
1) 2 молекулы азота
3) 7 атомов азота
2) 5 молекул азота
4) 10 атомов азота
5. Химическая связь является металлической в веществе:
1) кислород
3) сульфид железа
2) алюминий
4) оксид калия
6. Верны ли следующие высказывания?
А. При нормальных условиях озон жидкий.
Б. При нормальных условиях озон твердый.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
Ответом к заданиям 7- 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
7. Масса 2 ммоль углекислого газа СО2 равна __________ мг:
8. Количество вещества воды, в котором содержится 12•1023 молекул, равно_____ моль.
9. 3 моль кислорода О2 (н.у.) занимают объем ____л.
Часть 2
Запишите номер задания и полное решение
10. Сколько молекул содержат 140 г азота N2?
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 2
Простые вещества. Количественные соотношения
ВАРИАНТ-3
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Больше металлических свойств проявляет:
1) литий
3) калий
2) рубидий
4) натрий
2. Аллотропная модификация фосфора:
1) кислород
3) красный фосфор
2) алмаз
4) карбин
3. Атому элемента, образующему простое вещество - металл, соответствует электронная схема:
1) +16Э)2)8)6
3) +12Э)2)8)2
2) +14Э)2)8)4
4) +10Э)2)8
4. Запись 4N означает:
1) 4 молекулы азота
3) 4 атома азота
2) 2 молекулы азота
4) 4 атома натрия
5. Химическая связь является ковалентной неполярной в веществе:
1) вода
3) цинк
2) кислород
4) поваренная соль
6. Верны ли следующие высказывания?
А. При нормальных условиях сера твердая.
Б. При нормальных условиях сера газообразная.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
Ответом к заданиям 7- 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
7. Масса 3 кмоль воды равна _______________кг.
8. Количество вещества алюминия, в котором содержится 24•1023 атомов, равно_____ моль.
9. 4 кмоль хлора C12 (н.у.) занимают объем _____м3. (Запишите число с точностью до десятых).
Часть 2
Запишите номер задания и полное решение
10. Рассчитайте объем для 20 г водорода (н. у.).
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3» 11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 2
Простые вещества. Количественные соотношения
ВАРИАНТ-4
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Больше неметаллических свойств проявляет:
1) азот
3) мышьяк
2) фосфор
4) кремний
2. Аллотропная модификация олова:
1) графит
3) озон
2) алмаз
4) серое олово
3. Атому элемента, образующему простое вещество - неметалл, соответствует электронная схема:
1) +13Э)2)8)3
3) +9Э)2)7
2) +12Э)2)8)2
4) +3Э)2)1
4. Запись 6Н означает:
1) 6 молекул водорода
3) 6 атомов водорода
2) 3 молекулы водорода
4) 6 атомов гелия
5. Химическая связь является металлической в веществе:
1) озон
3) железо
2) графит
4) оксид натрия
6. Верны ли следующие высказывания?
А. При нормальных условиях азот твердый.
Б. При нормальных условиях азот газообразный.
1) верно только А
3) верно только Б
2) верны оба суждения
4) оба суждения не верны
Ответом к заданиям 7- 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
7. Масса 5 моль аммиака NН3 равна __________ г:
8. Количество вещества сернистого газа SO2, в котором содержится 3•1023 молекул, равно _____моль.
9. 2 кмоль газа метана СН4 занимают объем (н.у.)____м3.
Часть 2
Запишите номер задания и полное решение
10. Сколько молекул содержит 44,8 л сероводорода H2S (н.у.)?
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ -1
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Смесью веществ в отличие от чистого вещества является:
1) алюминий 3) магний.
2) водопроводная вода 4) углекислый газ
2. Ряд формул, в котором все вещества - оксиды:
1) SO3, MgO, CuO 3) ZnO, ZnCl2, H2O.
2) KOH, K2O, MgO 4) H2SO4, Al2O3, HCl
3. Азот проявляет наибольшую степень окисления в соединении с формулой:
1) NO2 3) NH3
2) NO 4) N2O5
4. Формула сульфата железа (III):
1) FeS 3) Fe2 (SO4)3
2) FeSO4 4) Fe2(SO3)3
5. В 80г воды растворили 20г соли. Массовая доля соли в полученном растворе равна:
1) 40% 2) 25% 3) 50% 4) 20%
6. Верны ли следующие высказывания?
А. В состав оснований входит ион металла.
Б. В состав оснований входит кислотный остаток.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Оксид алюминия
Б) Серная кислота
В) Гидроксид алюминия
Г) Сульфат алюминия
1) Al(OH)3
2) Al2 (SO4)3
3) AlО
4) Al2O3
5) H2SO4
6) H2SO3
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. К кислотам относятся:
1) H2CO3
2) Fe(OH)2
3) H2SiO3
4) Hg(NO3)2
5) HCl
6) SO2
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Массовая доля кислорода в серной кислоте равна ________(%)
Часть 2
Запишите номер задания и полное решение
10. Рассчитайте объем кислорода, полученного из 200л воздуха, если известно, что объемная доля кислорода в воздухе составляет 21%?
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ -2
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Чистое вещество в отличие от смеси - это:
1) морская вода 3) кислород
2) воздух 4) молоко
2. Ряд формул, в котором все вещества - основания:
1) СuOH, CuCl2, NaOH. 3) Ca(OH)2, Mg(OH)2, MgOHCl.
2) K2O, HCl, Ca(OH)2 4) KOH, Ba(OH)2, Cu(OH)2
3.Углерод проявляет наименьшую степень окисления в соединении с формулой:
1) СаСО3 2) СH4 3) СO2 4) СO
4.Формула хлорида меди (II):
1) CuCl 2) Cu(NO3)2 3) CuCl2 4) CuSO4
5. В 180г воды растворили 20г хлорида натрия. Массовая доля соли в полученном растворе равна:
1) 15% 2) 20% 3) 30% 4) 10%
6. Верны ли следующие высказывания?
А. В состав кислот входит ион водорода.
Б. В состав кислот входит кислотный остаток.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Оксид магния 1) MnCl2
Б) Соляная кислота 2) Mg(OH)2
В) Гидроксид магния 3) HF
Г) Хлорид магния 4) HCl
5) MgCl2
6) MgO
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. К солям относятся:
1) H2CO3
2) KNO3
3) Ba(OH)2
4) SO2
5) Na2S
6) CaCO3
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Массовая доля кислорода в оксиде алюминия равна ________(%)
Часть 2
Запишите номер задания и полное решение
10. Рассчитайте объём воздуха, необходимого для получения 39л азота, если известно, что объёмная доля азота в воздухе составляет 78%?
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ -3
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Смесью веществ не является:
1) речная вода 3) воздух
2) дистиллированная вода 4) почва
2. Ряд формул, в котором все вещества - кислоты:
1) HCl, CaCl2, H2SO4 3) HNO3, H2SO3, H3PO4.
2) NaOH, H2CO3, H2S 4) CaO, Na2CO3, H2S
3. Cера проявляет наибольшую степень окисления в соединении с формулой:
1) H2 S 2) SO2 3) Na 2S 4) SO3
4. Формула сульфита хрома (Ш):
1) Cr2S3 3) CrSO4
2) Cr2(SO4)3 4) Cr2(SO3)3
5. В 120г воды растворили 30г соли. Массовая доля соли в полученном растворе равна:
1) 20% 2) 25% 3) 30% 4) 10%
6. Верны ли следующие высказывания?
А. В состав солей входит ион металла.
Б. В состав солей входит кислотный остаток.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Оксид меди (II) 1) Cu2O
Б) Нитрат меди (II) 2) HNO3
В) Азотная кислота 3) Cu(OH)2
Г) Гидроксид меди (II) 4) Cu(NO3)2
5) H3PO4
6) CuO
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. К оксидам относятся:
1) NaOH 4) K2O
2) MgO 5) SO2
3) BaSO4 6) OF2
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Массовая доля кислорода в азотной кислоте равна__________(%)
Часть 2
Запишите номер задания и полное решение
10. Рассчитайте объём газа метана СН4, полученного из 500л природного газа, если известно, что объёмная доля метана в природном газе составляет 95%?
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 15 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 13 баллов - «4» 14 - 15 баллов - «5»
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ -4
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Смесью веществ, в отличие от чистого вещества, является:
1) алюминий 3) азот
2) воздух 4) золото
2. Ряд формул, в котором все вещества - соли:
1) NaCl, BaSO4, KNO3 3) MgSO3, CaO, AlCl3
2) CaSO4 , Na2CO3 , H2CO3 4) ZnS, CaI2, Al2O3
3. Фосфор проявляет наименьшую степень окисления в соединении с формулой:
1) Р2O5 3) РН3
2) Р2O3 4) Н3РО4
4. Формула нитрата железа (II):
1) Fe(NO3)2 3) Fe(NO3)3
2) Fe3N2 4) Fe(NO2)2
5. В 450г воды растворили 50г соли. Массовая доля соли в полученном растворе равна:
1) 9% 2)10% 3) 14% 4) 11%
6. Верны ли следующие высказывания?
А. Оксиды состоят из двух элементов.
Б. Степень окисления кислорода в оксидах +2
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Сернистая кислота 1) H2SO4
Б) Гидроксид бария 2) BaSO3
В) Сульфат бария 3) BaO
Г) Оксид бария 4) BaSO4
5) Ва(OH)2
6) H2 SO3
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. К основаниям относятся:
1) H2SO3 4) Fe(OH)2
2) NaOH 5) K2S
3) MgO 6) Ba(OH)2
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Массовая доля углерода в карбонате кальция равна ________(%).
Часть 2
Запишите номер задания и полное решение
10. Рассчитайте объём воздуха, необходимого для получения 50л кислорода, если известно, что объёмная доля кислорода в воздухе составляет 21%?
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 8 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 8 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 4.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 13 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 9 баллов - «3»
10 - 11 баллов - «4» 12 - 13 баллов - «5»
Контрольная работа № 4
Изменения, происходящие с веществами.
ВАРИАНТ -1
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Физическое явление - это:
1) ржавление железа 3) скисание молока
2) горение древесины 4) плавление свинца
2. Сумма вех коэффициентов в уравнении реакции, схема которой Al + Cl2 AlCl3, равна:
1) 4 2) 5 3) 8 4) 7
3. Схема, являющаяся уравнением химической реакции:
1) H2 + Cl2 HCl 3) Zn +HCl ZnCl2+H2
2) 2Ca + O2 2CaO 4) H2 + О2 H2О
4. Вещество «Х» в схеме: Х + 2HCl = FeCl2 + H2.
1) железо 3) хлор
2) оксид железа 4) гидроксид железа
5. Объём водорода, который полностью прореагирует по уравнению реакции
2H2 + O2 = 2H2O с 1 моль кислорода, равен:
1) 8,96л 3) 44,8л
2) 22, 4л4) 67,2л
6. Верны ли следующие высказывания?
А. Из нескольких простых или сложных веществ образуется одно более сложное вещество в реакции соединения.
Б. Из нескольких простых или сложных веществ образуется одно более сложное вещество в реакции разложения.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между левой и правой частями уравнений:
Левая часть: Правая часть:
А) CuO + H2SO4= 1) CuSO4 + H2O
Б) CuCl2 + 2NaOH =. 2) CuSO4 + 2H2O
В) Cu(OН)2 +2HCl = 3) CuCl2 + H2O
Г) Cu(OН)2 + H2SO4= 4) Cu(OH)2 + NaCl
5) CuCl2 + 2H2O
6) Cu(OH)2 + 2NaCl
А
Б
В
Г
Ответом к заданию 8 является последовательность трех цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Уравнения реакции обмена:
1) CaO + 2HCl= CaСl2 + H2O
2) FeS + 2HCl = FeCl2 + H2S
3) 2KClO3 = 2KCl + 3O2
4) Fe2O3 + 2Al = Al2O3 + 2Fe.
5) LiСl + AgNO3 = LiNO3 + AgCl.
6) 2Ca + O2 = 2CaO.
Часть 2
Запишите номер задания и полное решение
9. По уравнению реакции Cu (OH)2 = CuO + H2O найдите массу оксида меди (II), образовавшегося при разложении 39,2г гидроксида меди (II).
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 8 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 8 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 4.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 13 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 9 баллов - «3»
10 - 11 баллов - «4» 12 - 13 баллов - «5»
Контрольная работа № 4
Изменения, происходящие с веществами.
ВАРИАНТ -2
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Химическое явление - это:
1) горение свечи 3) испарение бензина
2) плавление льда 4) образование льда
2. Сумма вех коэффициентов в уравнении реакции, схема которой
Ca + HCl CaCl2 + H2, равна:
1) 6 2) 5 3) 3 4) 4
3. Схема, являющаяся уравнением химической реакции:
1) CaCO3 CaO + CO2 3) Ca + O2 CaO.
2) Mg + HCl MgCl2 + H2. 4) CO + O2 CO2
4. Вещество «Х» в схеме: Fe2O3 + 3H2 2Х + 3H2O
1) железо 3) водород
2) оксид железа 4) гидроксид железа
5. Объём водорода, который полностью прореагирует по уравнению реакции
H2 + Cl2 = 2HCl с 0,2 моль хлора (н.у.), равен:
1) 4,48л 3) 44,8л
2) 22, 4л4) 67,2л
6. Верны ли следующие высказывания?
А. Из одного сложного вещества образуются два или более новых веществ в реакции
соединения
Б. Из одного сложного вещества образуются два или более новых веществ в реакции
замещения
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между левой и правой частями уравнений
Левая часть: Правая часть:
А) Na2O + H2SO4= 1) Fe(OH)2 + KCl
Б) FeCl2 + 2KOH = 2) Fe(NO3)2 + 2H2O
В) Fe(OН)2 +2HNO3 = 3) FeNO3 + 2H2O
Г) 2NaOН + H2SO4= 4) Fe(OH)2 + 2KCl
5) Na2SO4 + 2H2O
6) Na2SO4 + H2O
А
Б
В
Г
Ответом к заданию 8 является последовательность трех цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Уравнения реакции разложения:
1) CaSiO3 = CaO + SiO2
2) FeS + 2HCl = FeCl2 + H2S
3) 2KNO3 = 2KNO2 + O2
4) Fe2O3 + 2Al = Al2O3 + 2Fe.
5) NaСl + AgNO3 = NaNO3 + AgCl.
6) 2Al(OH)3 = Al2O3 + 3H2O
Часть 2
Запишите номер задания и полное решение
9. По уравнению реакции Zn(OH)2 = Zn O + H2O определите массу оксида цинка, который образуется при разложении 198г исходного вещества.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 8 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 8 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 4.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 13 баллов.
Система оценивания работы.
0 - 6 баллов - «2» 7 - 9 баллов - «3»
10 - 11 баллов - «4» 12 - 13 баллов - «5»
Контрольная работа № 4
Изменения, происходящие с веществами.
ВАРИАНТ -3
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Физическое явление - это:
1) испарение воды 3) горение керосина
2) скисание молока 4) появление ржавчины
2. Сумма вех коэффициентов в уравнении реакции, схема которой
Al + O2 Al2O3 равна:
1) 6 2) 3 3) 9 4) 4
3. Схема, являющаяся уравнением химической реакции:
1) Cu + O2 CuO 3) 2HgO 2Hg + O2.
2) KClO3 KCl + O2. 4) HCl + Zn H2 + ZnCl2
4. Вещество «Х» в схеме: Х +H2SO4 = ZnSO4 + H2
1) цинк 3) оксид цинка
2) гидроксид цинка 4) вода
5 Объём водорода, который полностью прореагирует по уравнению реакции
H2 + Cl2 = 2HCl с 0,5 моль хлора (н.у.), равен:
1) 5,6л 3) 44,8л
2) 11,2л4) 22,4л
6. Верны ли следующие высказывания?
А. Атомы простого вещества замещают атомы одного из химических элементов в составе сложного вещества в реакции обмена.
Б. Атомы простого вещества замещают атомы одного из химических элементов в составе сложного вещества в реакции замещения.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между левой и правой частями уравнений:
Левая часть: Правая часть:
А) ZnO + 2HCl = 1) ZnCl2 + 2H2O
Б) Zn(OH)2 + 2HCl = 2) ZnCl2 + H2O
В) Zn + 2HCl = 3) Zn(OH)2 + 2KCl
Г) ZnCl2 + 2KOH = 4) ZnCl2 + H2
5) ZnOH + 2KCl
6) ZnCl2 + 2H2
А
Б
В
Г
Ответом к заданию 8 является последовательность трех цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Уравнения реакции замещения:
1) BaO + H2O = Ba(OH)2.
2) CuO + H2 = Cu + H2O.
3) 3KOH + H3PO4 = K3PO4 + 3H2O.
4) CaI2 + Cl2 = CaCl2+I2.
5) 2NH3 = N2 + 3H2.
6) Mg + 2HCl = MgCl2 + H2
Часть 2
Запишите номер задания и полное решение
9. По уравнению реакции Fe(OH)2 = FeO + H2O определите массу оксида железа (II), образовавшегося при разложении 45г исходного вещества.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 8 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 8 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 4.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 3 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 13 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 9 баллов - «3»
10 - 11 баллов - «4» 12 - 13 баллов - «5»
Контрольная работа № 4
Изменения, происходящие с веществами.
ВАРИАНТ -4
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Химическое явление - это:
1) плавление олова 3) горения магния
2) замерзания воды 4) образование тумана
2. Сумма вех коэффициентов в уравнении реакции, схема которой
N2 + H2 NH3 равна:
1) 6 2) 3 3) 4 4) 5
3. Схема, являющаяся уравнением химической реакции:
1) 3Fe + 2O2 Fe3O4 3) HgO Hg + O2.
2) 2Al + O2 Al2O3. 4) Ca + HCl CaCl2 + H2.
4. Формула вещества «Х» в схеме: 2Na + Х 2NаCl.
1) Cl 3) Cl2
2) HCl 4) Cl2O7
5 Объём водорода (н.у.), который полностью прореагирует по уравнению реакции
N2 + 3H2 2NH3c 1 моль азота, равен:
1) 67,2л 3) 44,8л
2) 11,2л4) 22,4л
6. Верны ли следующие высказывания?
А. Из двух сложных веществ образуется два новых сложных вещества в реакции обмена.
Б. Из двух сложных веществ образуется два новых сложных вещества в реакции соединения.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между левой и правой частями уравнений
Левая часть: Правая часть:
А) Mg(NO3)2 + 2KOH = 1) Mg(NO3)2 + 2H2O
Б) Mg(OH)2 + 2HNO3 = 2) MgNO3 + 2H2O
В) Mg + 2HCl = 3) Mg(OH)2 + 2KNO3
Г) MgO + 2HCl = 4) MgCl2+ H2
5) MgCl2+ H2O
6) Mg(OH)2 + KNO3
А
Б
В
Г
Ответом к заданию 8 является последовательность трех цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Уравнения реакции соединения:
1) BaO + H2O = Ba(OH)2.
2) CuO + H2 = Cu + H2O.
3) N2 + O2 = 2NO
4) Ca(OH)2 + 2HCl = CaCl2+2H2O.
5) N2 + 3H2 = 2NH3
6) Mg + 2HCl = MgCl2 + H2
Часть 2
Запишите номер задания и полное решение
9. По уравнению реакции CaО + H2O Ca (OH)2 определите массу гидроксида кальция, образовавшегося при взаимодействии 112г оксида кальция с водой.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 5
Классы неорганических соединений
ВАРИАНТ -1
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Группа формул веществ, включающая формулы основания, кислоты, соли и кислотного оксида.
1) CuO, Zn(OH)2, AlCl3, K2S 3) SO2, H2SO4, NaCl, CuO
2) Cu(OH)2, HCl, NaNO3, SO3 4) Zn(OH)2 ,HCl, K2S, Na2O
2. Формула сульфата натрия:
1) Na2SO4 3) Na2S
2) Na2SO3 4) Na2SiO3
3. Изменение свойств оксидов от кислотных к основным происходит в ряду веществ с формулами:
1) Li2O - BeO - B2O3 3) NO2 - CO2 - SO2
2) P2O5 - SiO2 - Al2O3 4) P2O5 - CаO - SO3
4. Пара формул веществ, реагирующих с оксидом серы (IV):
1) Ca(OH)2, H2O 3) H2O, NaCl
2) Na2O, Na4) SO3, H2SO4
5. Металл, реагирующий с водным раствором хлорида меди (II):
1) Золото 2) Железо 3) Ртуть 4) Серебро
6. Верны ли следующие высказывания?
А. В уравнении реакции: Х + HCl = NaCl + H2O веществом Х является
вещество с формулой Na.
Б. В уравнении реакции: Х + HCl = NaCl + H2O веществом Х является
вещество с формулой NaOH.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой оксида и соответствующего ему гидроксида.
Формула оксида Формула гидроксида
А) Cu2O 1) H2SO4
Б) CO2 2) Al (OH)3
В) Al2O3 3) Cu (OH)2
Г) SO3 4) H2CO3
5) CuOH
6) H2SO3
А
Б
В
Г
Ответом к заданиям 8, 9 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Металлы, реагирующие с раствором соляной кислоты:
1) Ca 4) Cu
2) Mg 5) Ag
3) Zn 6) С
9. Вещества, реагирующие с раствором гидроксида натрия:
1) Соляная кислота 4) Хлорид натрия
2) Нитрат меди 5) Углекислый газ
3) Вода 6) Оксид калия
Часть 2
Запишите номер задания и полное решение
10. Предложите два способа получения сульфата магния. Составьте уравнения реакций в молекулярном и ионном виде, укажите тип реакций.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 5
Классы неорганических соединений
ВАРИАНТ -2
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Группа формул веществ, включающая формулы основания, кислоты, соли и основного оксида
1) BaO, AlCl3, H3PO4, Pb(NO3)2 3) FeSO4 , SO2 , H2CO3, Fe(OH)2
2) CuO, H2SO3, KNO3, Ba(OH)2 4) Ca(OH)2 ,NaCl, Na2S, Na2O
2. Формула хлорида хрома (III)
1) CrClO3 3) CrCl3
2) CrOHCl2 4) CrCl2
3. Изменение свойств оксидов от основных к кислотным происходит в ряду веществ с формулами:
1) SO3 - MgO -Al2O3 3) P2O5 - Li2O - SiO2
2) MgO - Al2O3 - SiO2 4) Li2O - P2O5 - CаO
4. Пара формул веществ, реагирующих с оксидом кальция:
1) Ca(OH)2, H2O 3) HCl, NaOH
2) NaCl, K 2O 4) CO2, HCl
5. Металл, реагирующий с водным раствором сульфата меди (II):
1) Цинк 2) Платина 3) Ртуть 4) Серебро
6. Верны ли следующие высказывания?
А. В уравнении реакции: Х + 2HNO3 = 2KNO3 + H2O
веществом Х является вещество с формулой K2O
Б. В уравнении реакции: Х + 2HNO3 = 2KNO3 + H2O
веществом Х является вещество с формулой K
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой гидроксида и соответствующего ему оксида.
Формула гидроксида Формула оксида
А) H3PO4 1) SO2
Б) Fe(OH)3 2) FeO
В) H2SO4 3) Fe2O3
Г) Ba(OH)2 4) BaO
5) P2O5
6) SO3
А
Б
В
Г
Ответом к заданиям 8, 9 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Вещества, реагирующие с раствором серной кислоты:
1) Zn 4) NaСl
2) Ba(OH)2 5) Cu
3) CO2 6) MgO
9. Вещества, реагирующие с раствором гидроксида бария:
1) Соляная кислота 4) Оксид меди (II)
2) Сульфат калия 5) Оксид серы (IV)
3) Гидроксид калия 6) Нитрат натрия
Часть 2
Запишите номер задания и полное решение
10. Предложите два способа получения хлорида цинка. Составьте уравнения реакций в молекулярном и ионном виде, укажите тип реакций.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 5
Классы неорганических соединений
ВАРИАНТ - 3
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Группа формул веществ, включающая формулы основания, кислоты, соли и основного оксида
1) HCl , SO3 , NaNO3, Ca(OH)2 3) CuCl2, К2О, NaNO3, Ca(OH)2
2) CuCl2, H3PO4, KOH, CO2 4) HNO3, FeS, Cu(OH)2, FeO
2.Формула сульфита железа (II)
1) FeCl2 3) FeSO3
2) FeSO4 4) FeOHCl
3. Изменение свойств оксидов от кислотных к основным происходит в ряду веществ с формулами:
1) P2O5 - Al2O3 - MgO 3) Al2O3- SiO2 - MgO
2) CaO - CO2 - Al2 O3 4) P2O5 - MgO - SiO2
4. Пара формул веществ, реагирующих с оксидом углерода (IV):
1) H2O, P2O5 3) К2О, О2
2) NaOH, H2O 4) Ca(OH)2, H2SO4
5. Металл, реагирующий с водным раствором нитрата железа (II):
1) Алюминий 2) Золото 3) Медь 4) Платина
6. Верны ли следующие высказывания?
А. В уравнении реакции: CaO + X = CaSO4 + H2O веществом Х является
вещество с формулой H2SO3.
Б. В уравнении реакции: CaO + X = CaSO4 + H2O веществом Х является вещество с формулой H2SO4.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой оксида и соответствующего ему гидроксида.
Формула оксида Формула гидроксида
А) Fe2O3 1) Н2СО3
Б) CO2 2) Fe(OН)3
В) CaO 3) Fe(OH)2
Г) P2O5 4) Ca(OH)2
5) H3PO4
6) HPO2
А
Б
В
Г
Ответом к заданиям 8, 9 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Металлы, реагирующие с раствором серной кислоты:
1) Mg 4) Au
2) Zn 5) Cu
3) Ag 6) Fe
9. Вещества, реагирующие с раствором гидроксида калия:
1) Серная кислота 4) Нитрат натрия
2) Гидроксид магния 5) Хлорид меди (II)
3) Оксид фосфора (V) 6) Оксид железа (II)
Часть 2
Запишите номер задания и полное решение
10. Предложите два способа получения фосфата натрия. Составьте уравнения реакций в молекулярном и ионном виде, укажите тип реакций.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 5
Классы неорганических соединений
ВАРИАНТ - 4
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Группа формул веществ, включающая формулы представителей четырех классов неорганических соединений;
1) HNO3, CaO, Na2S, KOH 3) MgO, HCl, Cu(OH)2, CO2
2) Al2O3, H2SO4, LiOH, HBr 4) HCl, CaSO3 , NaNO3, Ca(OH)2
2.Формула сульфида меди (II):
1) CuCl2 3) CuCl
2) CuS4) CuI2
3. Изменение свойств оксидов от основных к кислотным происходит в ряду веществ с формулами:
1) SiO2 -MgO - P2O5 3) MgO- SiO2 -P2O5
2) P2 O5 - MgO - Li2 O 4) CaO - CO2 - Al2 O3
4. Пара формул веществ, реагирующих с оксидом лития:
1) H2O, CaO 3) NaOH, HCl
2) NaOH, H2O 4) CO2, H2SO4
5. Металл, реагирующий с водным раствором хлорида железа (II):
1) Платина 2) Серебро 3) Цинк 4) Медь
6. Верны ли следующие высказывания?
А. В уравнении реакции: Х + H2SO4 = CuSO4 + H2O веществом Х является
вещество с формулой CuO:
Б. В уравнении реакции: Х + H2SO4 = CuSO4 + H2O веществом Х является
вещество с формулой Cu2O:
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой гидроксида и соответствующего ему оксида.
Формула гидроксида Формула оксида
А) KOH 1) КO
Б) Cu(OH)2 2) CrO3
В) Cr(OH)3 3) Cr2O3
Г) H2CrO4 4) CuO
5) K2O
6) Cu2O
А
Б
В
Г
Ответом к заданиям 8, 9 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. Вещества, реагирующие с разбавленной соляной кислотой:
1) HgO 4) CO2
2) HNO3 5) NaNO3
3) Mg 6) AgNO3
9. Вещества, реагирующие с раствором гидроксида кальция:
1) Вода 4) Оксид серы (IV)
2) Азотная кислота 5) Угарный газ
3) Оксид магния 6) Сульфат меди
Часть 2
Запишите номер задания и полное решение
10. Предложите два способа получения нитрата кальция. Составьте уравнения реакций в молекулярном и ионном виде, укажите тип реакций.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 6
Итоговая контрольная работа за курс 8 класса
ВАРИАНТ -1
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Число атомов всех химических элементов в молекуле серной кислоты равно:
1) 3 2) 4 3) 7 4) 6
2. Число протонов, нейтронов и электронов в атоме фтора 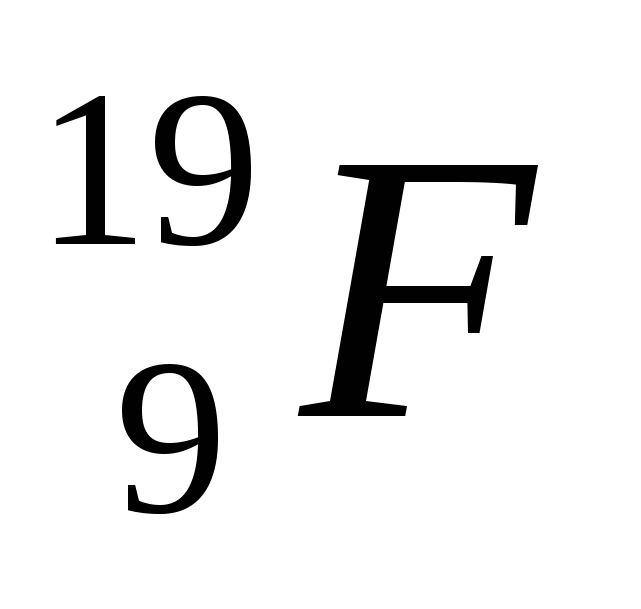
1) p+ - 9; n0 - 10; ē - 19 3) p+ - 9; n0 - 10; ē - 9
2) p+ - 10; n0 - 9; ē - 10 4) p+ - 9; n0 - 9; ē - 19
3. Группа формул веществ с ковалентным типом связи:
1) H2S, P4, CO2 3) HCl, NaCl, H2O
2) H2, Na, CuO 4) CaO, SO2, CH4
4. Вещество, при растворении которого в воде электролитической диссоциации практически не происходит:
1) гидроксид натрия 3) хлорид серебра
2) сульфат калия4) нитрат алюминия
5. Одновременно могут находиться в растворе ионы:
1) Na+, H+, Ba2+, OH- 3) Mg2+, K+, NO3-, SO42 -
2) Fe2+, Na+, OH- , SO42- 4) Ca2+, H+, CO32-, Cl -
6. Верны ли следующие высказывания?
А. Оксид фосфора (V) - кислотный оксид
Б. Соляная кислота - одноосновная кислота
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой вещества и классом соединения:
Формула вещества: Класс соединения:
А) Н3РО4 1) соль
Б) SO3 2) основный оксид
В) Сu(OH)2 3) нерастворимое основание
Г) CaCl2 4) кислотный оксид
5) кислота
6) растворимое основание
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. С раствором гидроксида натрия реагируют:
1) сульфат меди (II) 4) азотная кислота
2) оксид меди (II) 5) магний
3) гидроксид калия6) оксид углерода (IV)
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Масса соли, содержащейся в 150г 5% -ного раствора соли, равна _______г.
Часть 2
Запишите номер задания и полное решение
10. Составьте уравнения химических реакций согласно схеме
Fe(OH)3 → Fe2O3 → Fe → FeSO4 → Fe(OH)2
Назовите все сложные вещества, укажите тип реакции.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 6
Итоговая контрольная работа за курс 8 класса
ВАРИАНТ -2
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Число атомов всех химических элементов в молекуле фосфорной кислоты равно:
1) 3 2) 6 3) 10 4) 8
2. Число протонов, нейтронов и электронов в атоме хлора 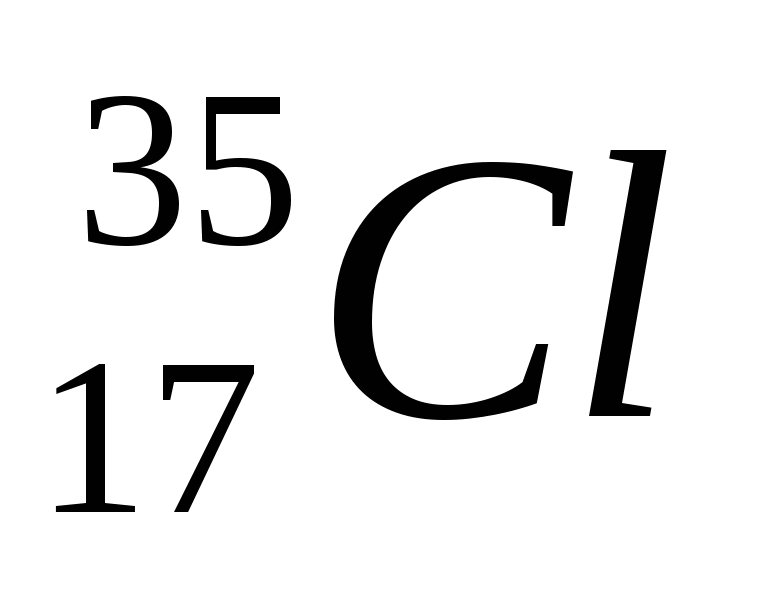
1) p+ - 18; n0 - 18; ē - 18 3) p+ - 17; n0 - 18; ē - 18
2) p+ - 17; n0 - 17; ē - 17 4) p+ - 17; n0 - 18; ē - 17
3. Группа формул веществ с ионным типом химической связи:
1) Na2S, KCl, HF 3) CO2, BaCl2, NaOH
2) K2O, NaH, NaF 4) Ca, O2, AlCl3
4.Вещество, которое в водном растворе полностью диссоциирует:
1) оксид меди 3) сульфат бария
2) нитрат калия4) гидроксид железа (III)
5. Одновременно не могут находиться в растворе ионы:
1) H+, Ba2+, OH- , NO3- 3) Zn2+, K+, Cl -, SO42 -
2) Fe2+, Na+, NO3- , SO42- 4) K+, Na+, OH-, Cl -
6. Верны ли следующие высказывания?
А. Серная кислота - двухосновная
Б. Оксид калия - основный оксид.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой вещества и классом соединения:
Формула вещества: Класс соединения:
А) LiOH 1) соль
Б) SO2 2) основный оксид
В) HNO3 3) нерастворимое основание
Г) CaCO3 4) кислотный оксид
5) кислота
6) растворимое основание
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. В реакцию с раствором соляной кислоты вступают:
1) ртуть 4) карбонат натрия
2) гидроксид магния 5) хлорид бария
3) оксид натрия6) оксид серы (VI)
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. В 450г воды растворили 50г соли. Массовая доля соли в полученном растворе равна_____(%)
Часть 2
Запишите номер задания и полное решение
10. Составьте уравнения химических реакций согласно схеме
Na → NaOH → Cu(OH)2 → CuO → Cu
Назовите все сложные вещества, укажите тип реакции.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 6
Итоговая контрольная работа за курс 8 класса
ВАРИАНТ -3
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Число атомов всех химических элементов в молекуле азотной кислоты равно:
1) 3 2) 4 3) 7 4) 5
2. Число протонов, нейтронов и электронов в атоме калия 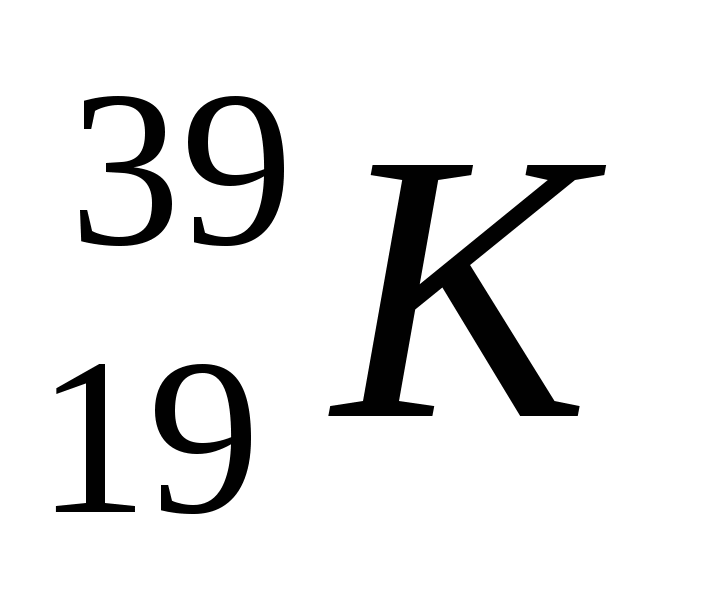 :
:
1) p+ - 19; n0 - 20; ē - 19 3) p+ - 20; n0 - 19; ē - 20
2) p+ - 19; n0 - 20; ē - 39 4) p+ - 19; n0 - 19; ē - 19
3. Группа формул веществ с ковалентным типом связи:
1) BaCl2, Cl2, SO3 3) NaOH, NH3, HF
2) H2, Ca, ZnCl2 4) N2, H2O, SO2
4.Вещество, при растворении которого в воде электролитической диссоциации практически не происходит:
1) гидроксид меди (II) 3) нитрат цинка
2) серная кислота 4) хлорид магния
5. Одновременно могут находиться в растворе ионы:
1) К+, Cl-, Сa2+, CO32- 3) Mg2+, H+, NO3-, CO32 -
2) Al3+, Na+, NO3- , SO42- 4) Fe3+, H+, OH-, Cl -
6. Верны ли следующие высказывания?
А. Азотная кислота - кислородсодержащая.
Б. Соляная кислота - кислородсодержащая.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой вещества и классом соединения:
Формула вещества: Класс соединения:
А) Zn(OH)2 1) соль
Б) H2SO3 2) основный оксид
В) NaCl 3) нерастворимое основание
Г) CaO 4) кислотный оксид
5) кислота
6) растворимое основание
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. С раствором гидроксида кальция реагируют:
1) серная кислота 4) медь
2) оксид углерода (IV) 5) хлорид натрия
3) карбонат натрия 6) оксид калия
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. Масса соли, содержащейся в 300г 3%-ного раствора соли, равна______г
Часть 2
Запишите номер задания и полное решение
10. Составьте уравнения химических реакций согласно схеме
HCl → ZnCl2 → Zn(OH)2 → Zn(NO3)2
ZnO
Назовите все сложные вещества, укажите тип реакции.
Дорогой восьмиклассник!
На выполнение контрольной работы отводится 45 минут. Работа состоит из 2 частей и включает 10 заданий.
Часть 1 включает 9 заданий с кратким ответом. К заданиям 1 - 6 дается 4 варианта ответа, из которых только один правильный. За каждый правильный ответ дается 1 балл. Максимальный балл - 6.
Задания 7 - 9 повышенного уровня, на которые надо дать краткий ответ в виде числа или последовательности цифр. За каждый правильный ответ ты получишь 2 балла. Максимальный балл - 6.
Часть 2 содержит 1 наиболее сложное, объемное задание, которое требует полного ответа. За правильное выполнение задания ты можешь получить 4 балла.
Баллы, полученные за выполненные задания, суммируются. Постарайся набрать наибольшее количество баллов. Максимальный первичный балл - 16 баллов
Система оценивания работы.
0 - 6 баллов - «2» 7 - 10 баллов - «3»
11 - 14 баллов - «4» 15 - 16 баллов - «5»
Контрольная работа № 6
Итоговая контрольная работа за курс 8 класса
ВАРИАНТ -4
Часть 1
Ответом к заданиям 1- 6 является одна цифра. Запиши ответ в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки.
1. Число атомов всех химических элементов в молекуле сернистой кислоты
1) 3 2) 7 3) 5 4) 6
2. Число протонов, нейтронов и электронов в атоме натрия 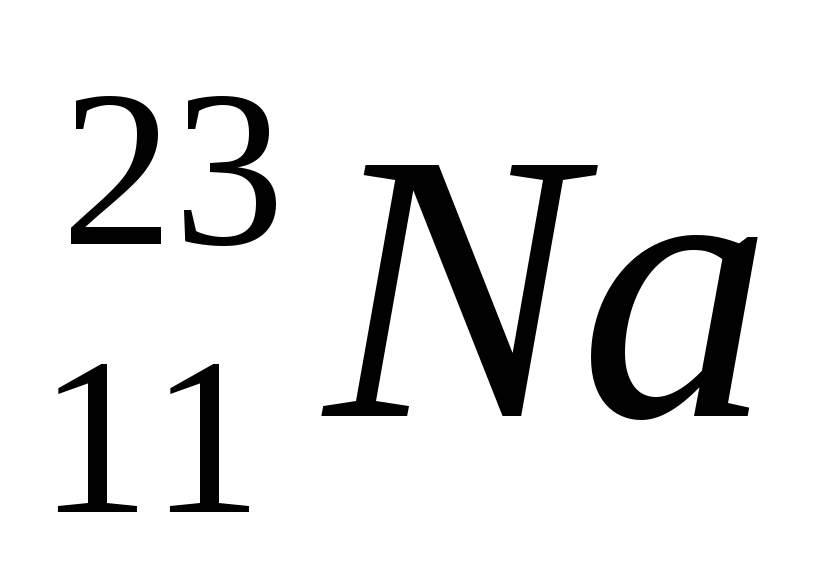
1) p+ - 11; n0 - 12; ē - 23 3) p+ - 11; n0 - 11; ē - 11
2) p+ - 12; n0 - 11; ē - 12 4) p+ - 11; n0 - 12; ē - 11
3. Группа формул веществ с ионным типом связи:
1) ВаО, Na2S, MgCl2 3) BaS, SO2, CaF2
2) Na2O, NaCl, HCl 4) BaO, ZnO, HCl
4.Вещество, при растворении которого в воде электролитической диссоциации практически не происходит:
1) нитрат бария 3) серная кислота
2) хлорид серебра 4) сульфат железа (II)
5. Одновременно не могут находиться в растворе ионы:
1) K+, Al3+, Cl-, NO3- 3) Na+, Ba2+, Cl-, CO32 -
2) H+, Mg2+, NO3- , SO42- 4) Ca2+, H+, NO3-, Cl -
6. Верны ли следующие высказывания?
А. Оксид углерода (IV) - кислотный оксид
Б. Оксид натрия - основный оксид.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
В задании 7 к каждому элементу первого столбца подберите соответствующий элемент второго столбца и запишите в таблицу на черновике выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться
7. Установите соответствие между формулой вещества и классом соединения:
Формула вещества: Класс соединения:
А) MgO 1) соль
Б) H2SO4 2) основный оксид
В) KOH 3) нерастворимое основание
Г) Ba(NO3)2 4) кислотный оксид
5) кислота
6) растворимое основание
А
Б
В
Г
Ответом к заданию 8 является последовательность трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания в БЛАНК ОТВЕТОВ справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
8. В реакцию с раствором серной кислоты вступают:
1) медь 4) магний
2) оксид меди (II) 5) хлорид натрия
3) гидроксид натрия6) оксид серы (IV)
Ответом к заданию 9 является число. Запишите это число в БЛАНК ОТВЕТОВ без указания единиц измерения с точностью до десятых.
9. В 180г воды растворили 20г соли. Массовая доля соли в полученном растворе равна _____%
Часть 2
Запишите номер задания и полное решение
10. Составьте уравнения химических реакций в молекулярном и ионном видах согласно схеме
Fe → FeCl2 → Fe(OH)2 → FeO → Fe
Назовите все вещества, укажите тип реакции.
Приложение 1
План характеристики химического элемента
по периодической системе Д. И. Менделеева
I. Положение элемента в периодической системе:
1. Порядковый номер, название.
2. Период (большой, малый).
3. Ряд.
4. Группа, подгруппа.
5. Относительная атомная масса.
II. Строение атома элемента:
1. Заряд ядра атома.
2. Формула состава атома (количество р+; n0; е-).
3. Схема строения атома.
4. Формула электронной конфигурации.
5. Квантовые ячейки.
6. Число е- на последнем уровне.
7. Металл или неметалл.
III. Формулы соединений:
1. Летучего водородного соединения (для неметаллов).
2. Оксида.
3. Гидроксида (основания или кислоты).
IV. Химический характер соединений, его доказательство:
1. Кислотный: кислотный оксид + щелочь; кислота + основание.
2. Основный: основный оксид + кислота; основание + кислота.
3. Амфотерный: (1 и 2).
V. Сравнение металлических и неметаллических свойств с соседями:
1. По периоду.
2. По группе.
(Металлы с неметаллами не сравнивать)
Приложение 2

ОТВЕТЫ
Контрольная работа № 1 Атомы химических элементов
Часть 1
1
2
3
4
5
6
Вариант 1
1
3
3
1
4
3
Вариант 2
2
3
2
4
4
3
Вариант 3
3
3
3
1
1
4
Вариант 4
2
4
1
2
3
1
7
8
9
Вариант 1
1663
345
208
Вариант 2
2654
124
102
Вариант 3
6215
145
101
Вариант 4
4632
136
142
Часть 2
План характеристики
Вариант 1
Вариант 2
Вариант 3
Вариант 4
I. Положение элемента в
периодической системе:
1.порядковый номер, название
Z = 11
Z = 16
Z = 14
Z = 20
2. период (большой, малый)
3, малый
3, малый
3, малый
4, большой
3.ряд
3
3
3
3
4.группа, подгруппа
1, главная
6, главная
4, главная
2, главная
5.относительная атомная масса
Ar = 23
Ar = 32
Ar = 28
Ar = 40
II. Строение атома элемента
1. заряд ядра атома
+q = + 11
+q = + 16
+q = + 14
+q = + 20
2. формула состава атома
(количество р; n; е- )
Na (11p;12n;) 11 е-
S (16p; 16n;) 16 е-
Si ( 14p;14n;) 14е-
Ca ( 20p;20n;)
20 е-
3. схема строения атома
+11 Na ) ) )
2 8 1
+16 S ) ) )
2 8 6
+14 Si ) ) )
2 8 4
+20 Ca ) ) ) )
2 8 8 2
4. формула электронной конфигурации
1s2 2s2 2p6 3s1
1s2 2s2 2p6 3s23p4
1s2 2s2 2p6 3s23p2
1s2 2s2 2p6 3s23p64s2
5. число е- на последнем уровне, металл или неметалл
1, металл
6, неметалл
4, неметалл
2, металл
III. Сравнение металлических и неметаллических свойств с соседями:
1. по периоду
Na >Mg
S >P
S < Cl
Si < C
Ca >Sc
Ca < K
2. по группе (металл с неметаллом не сравнивать)
Na >Li
Na < K
S > Se
S < O
Si < P
Ca >Mg
Ca < Sr
Схема строения иона
+11Na+ ) )
2 8
+16S2- ) ) )
2 8 8
+14Si4+ ) )
2 8
+20Ca2+ ) ) )
2 8 8
Контрольная работа № 2 Простые вещества. Количественные соотношения.
Часть 1
1
2
3
4
5
6
Вариант 1
2
3
3
2
2
1
Вариант 2
3
4
2
2
2
4
Вариант 3
2
3
3
3
2
1
Вариант 4
1
4
3
3
3
3
7
8
9
Вариант 1
102
6,0
44,8
Вариант 2
88
2,0
67,2
Вариант 3
54
4,0
89,6
Вариант 4
85
0,5
44,8
Часть 2
Вар
Содержание верного ответа и указания по оцениванию
Баллы
Элементы ответа:
-
Записано краткое условие задачи
-
Приведены формулы для нахождения объема и количества вещества.
-
Рассчитаны количество вещества и объем углекислого газа; записан ответ
Ответ правильный и полный
3
В ответе допущена ошибка в одном элементе
2
В ответе допущена ошибка в двух элементах
1
Все элементы ответа записаны неверно
0
1
Решение

 Дано: V = Vm • n n = 160г /32г/моль n = 5моль
Дано: V = Vm • n n = 160г /32г/моль n = 5моль
m (О2 ) = 160г n = m / M V = 22,4л/моль • 5моль V = 112л
V (О2) = X л
Ответ: объем кислорода 112л
2
Решение

 Дано: N = NA • n n = 140г /28г/моль n = 5моль
Дано: N = NA • n n = 140г /28г/моль n = 5моль
m (N2 ) = 140г n = m / M N = 6 •1023 • 5моль N = 30 •1023 молекул
N (N2) = X молекул
Ответ: 30 •1023 молекул азота
3
 Решение
Решение
 Дано: V = Vm • n n = 20г /2г/моль n = 10моль
Дано: V = Vm • n n = 20г /2г/моль n = 10моль
m (Н2 ) = 20г n = m / M V = 22,4л/моль • 10моль V = 224л
V (Н2 ) = Xл
Ответ: объем водорода 224л
4
Решение

 Дано: N = NA • n n = 44,8л /22,4л/моль n = 2моль
Дано: N = NA • n n = 44,8л /22,4л/моль n = 2моль
V (H2S ) = 44,8л n = V / Vm N = 6 •1023 • 2моль N = 12 •1023 молекул
N (H2S) = X молекул
Ответ: 12 •1023 молекул азота
Контрольная работа № 3 Соединения химических элементов
Часть 1
1
2
3
4
5
6
Вариант 1
2
1
4
3
4
1
Вариант 2
3
4
2
3
4
2
Вариант 3
2
3
4
4
1
2
Вариант 4
2
1
3
1
2
1
7
8
9
Вариант 1
4512
135
65,3
Вариант 2
6425
256
47,1
Вариант 3
6423
245
76,2
Вариант 4
6543
246
12,0
Часть 2
Вар
Содержание верного ответа и указания по оцениванию
Баллы
Элементы ответа:
-
Записано краткое условие задачи
-
Приведены формулы для нахождения объема и количества вещества.
-
Рассчитаны количество вещества и объем углекислого газа; записан ответ
Ответ правильный и полный
3
В ответе допущена ошибка в одном элементе
2
В ответе допущена ошибка в двух элементах
1
Все элементы ответа записаны неверно
0
1
Решение

 Дано: V (О2) =
Дано: V (О2) =![]() Vвоз • ω (О2) V (О2) =
Vвоз • ω (О2) V (О2) = 200 • 21%
200 • 21%
Vвоз. = 200л 100% 100%
ω (О2) = 21%
V (О2) = X л V (О2) = 42л
42л
Ответ: объем кислорода 42л
2
Решение

 Дано: Vвоз. =
Дано: Vвоз. =![]() V(N2) • 100% Vвоз. =
V(N2) • 100% Vвоз. = 39 • 100%
39 • 100%
V(N2). = 39л ω (N2) 78%
ω (N2) = 78%
V воз. = X л V воз. = 50л
50л
Ответ: объем воздуха 50л
3
Решение

 Дано: V (СН4) =
Дано: V (СН4) = Vвоз • ω (СН4) V (N2) =
Vвоз • ω (СН4) V (N2) = 500 • 95%
500 • 95%
Vпр.газа. = 500л 100% 100%
ω (СН4) = 95%
V (СН4) = X л V (N2) = 475л
475л
Ответ: объем метана 475л
4
Решение

 Дано: Vвоз. =
Дано: Vвоз. =![]() V(О2) • 100% Vвоз. =
V(О2) • 100% Vвоз. = 50 • 100%
50 • 100%
V(О2). = 50л ω (О2) 21%
ω (О2) = 21%
V воз. = X л V воз. = 238,1л
238,1л
Ответ: объем воздуха 238,1л
Контрольная работа № 4 Изменения, происходящие с веществами
Часть 1
1
2
3
4
5
6
Вариант 1
4
4
2
1
3
1
Вариант 2
1
2
1
1
1
4
Вариант 3
1
3
3
1
2
3
Вариант 4
3
1
1
3
1
1
7
8
Вариант 1
1652
125
Вариант 2
6425
136
Вариант 3
2143
246
Вариант 4
3145
135
ЧАСТЬ 2
ВАР.
Содержание верного ответа и указания по оцениванию
Баллы
Элементы ответа:
-
Записано краткое условие задачи
-
В уравнении химической реакции записаны необходимые данные.
Составлена и решена пропорция, записан ответ
Ответ правильный и полный
3
В ответе допущена ошибка в одном элементе
2
В ответе допущена ошибка в двух элементах
1
Все элементы ответа записаны неверно
0
1
 Дано: 39,2г Хг
Дано: 39,2г Хг
m (Cu(OH)2) = 39,2г Cu(OH)2 = CuO + H2O
m (CuO) = Хг 1моль 1моль
98г/моль 80г/моль
98г 80г
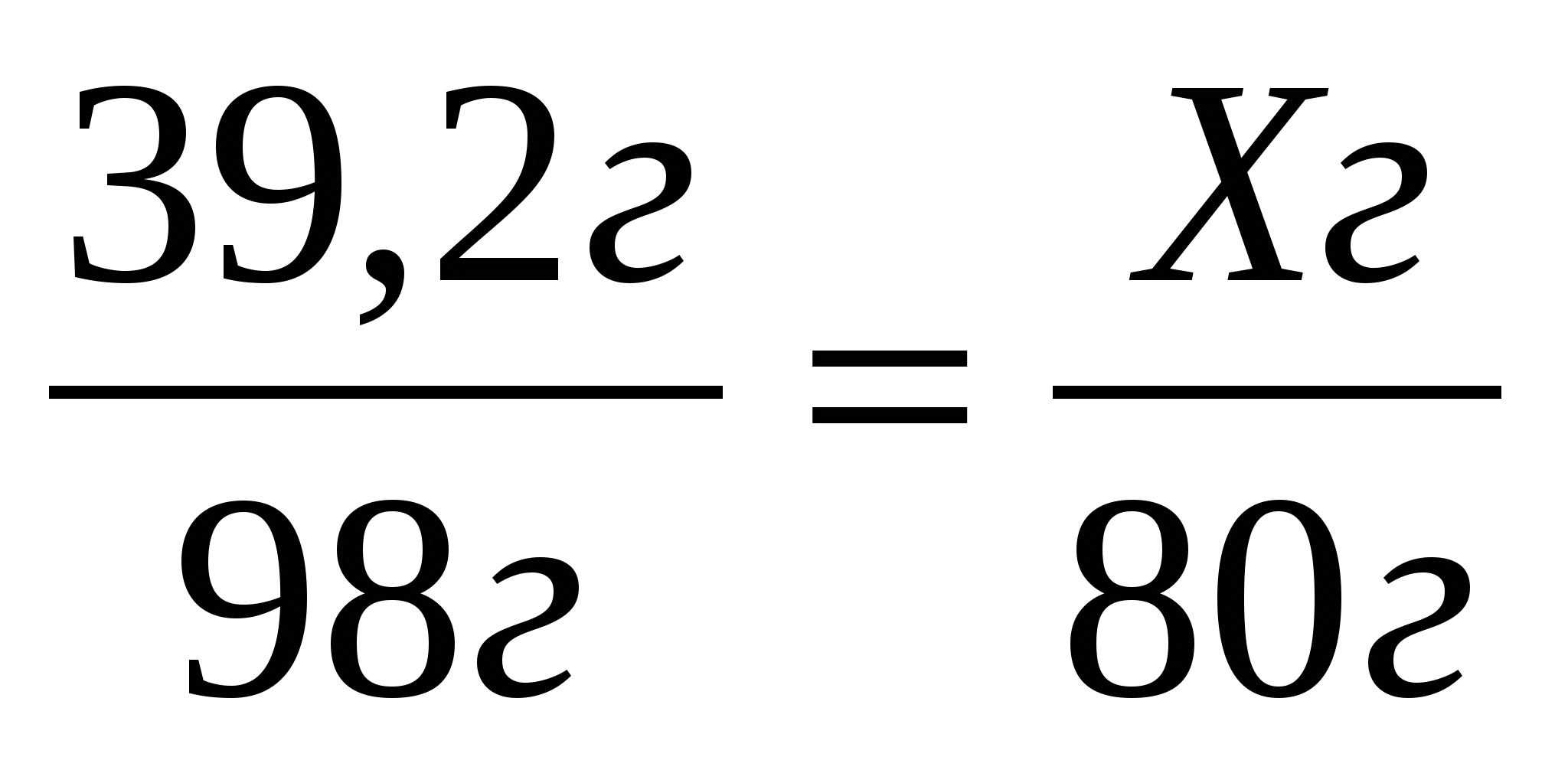
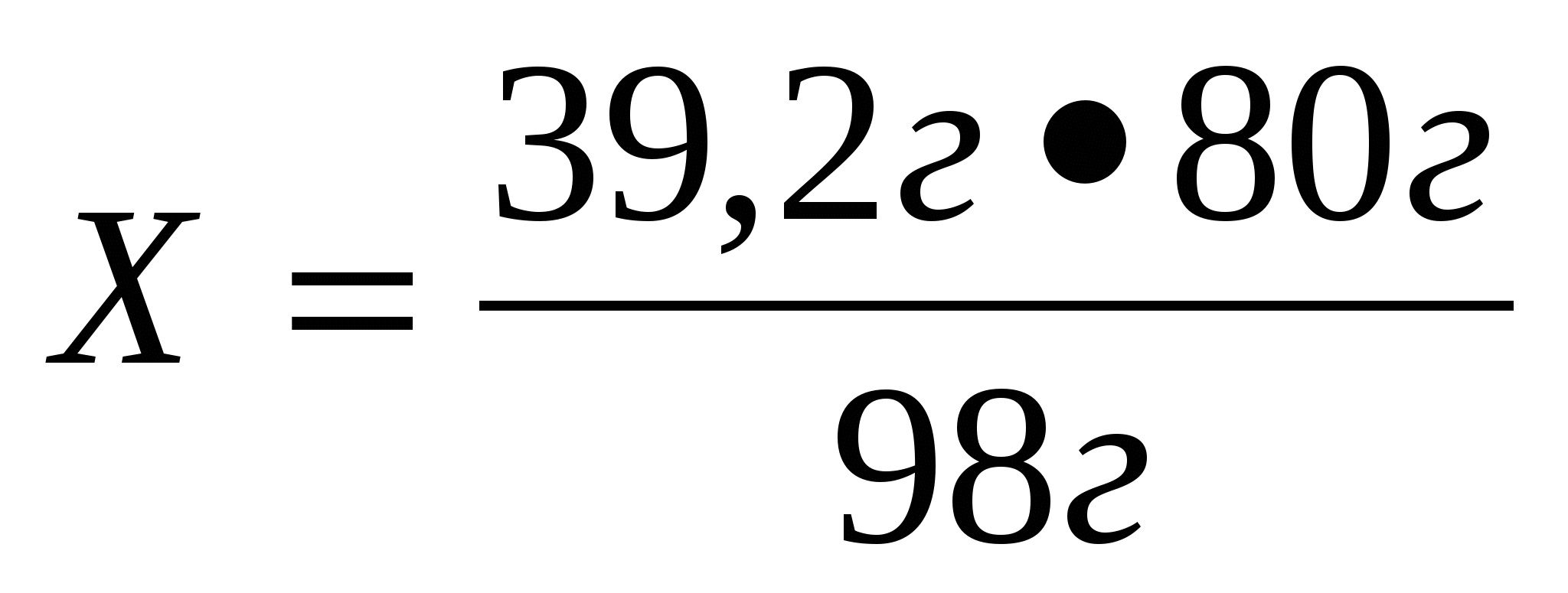
Х = 32г
Ответ: образуется 32г оксида меди
2
 Дано: 198г Хг
Дано: 198г Хг
m (Zn(OH)2) = 198г Zn(OH)2 = ZnO + H2O
m (ZnO) = Хг 1моль 1моль
99г/моль 81г/моль
99г 81г
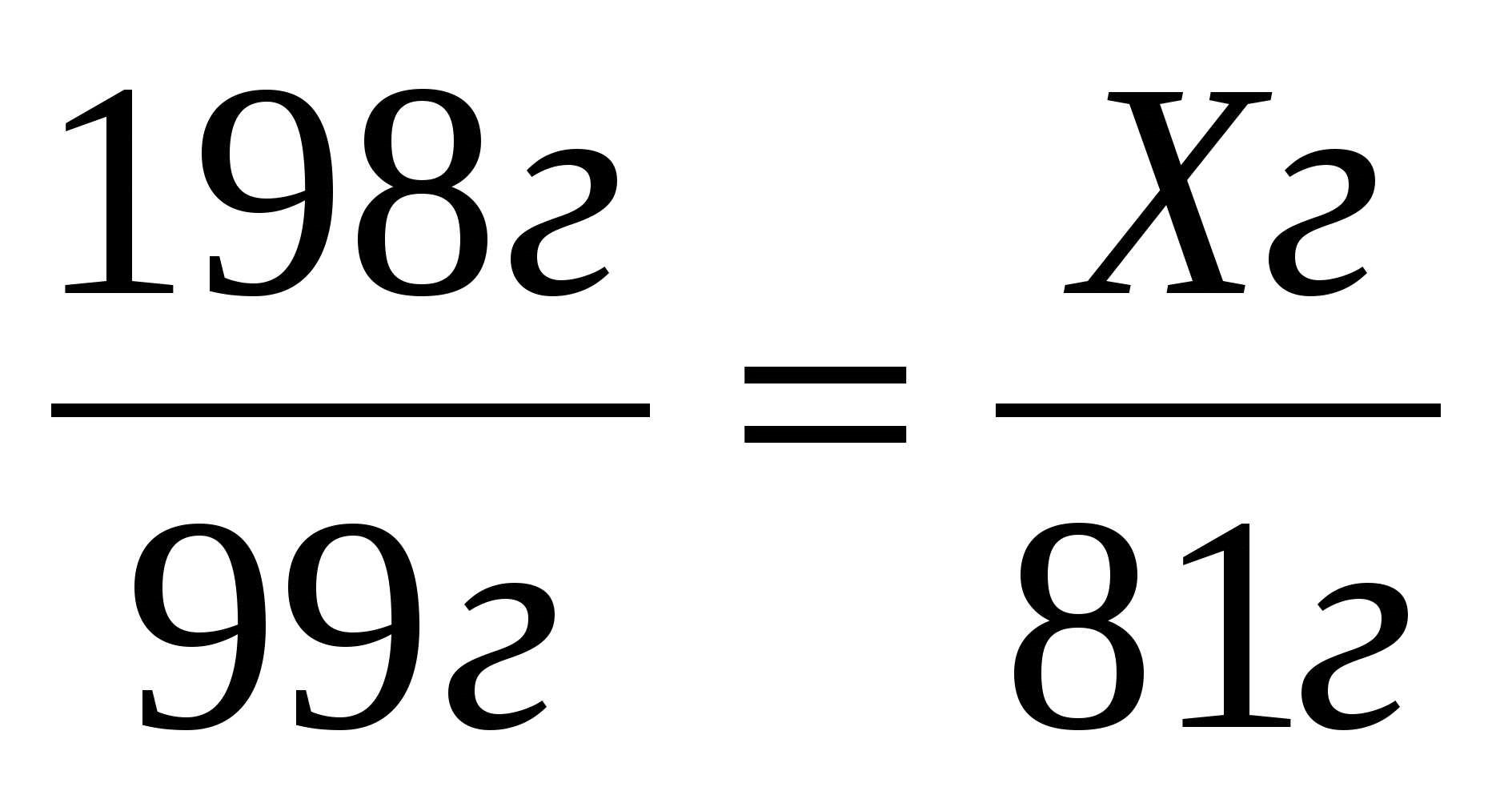
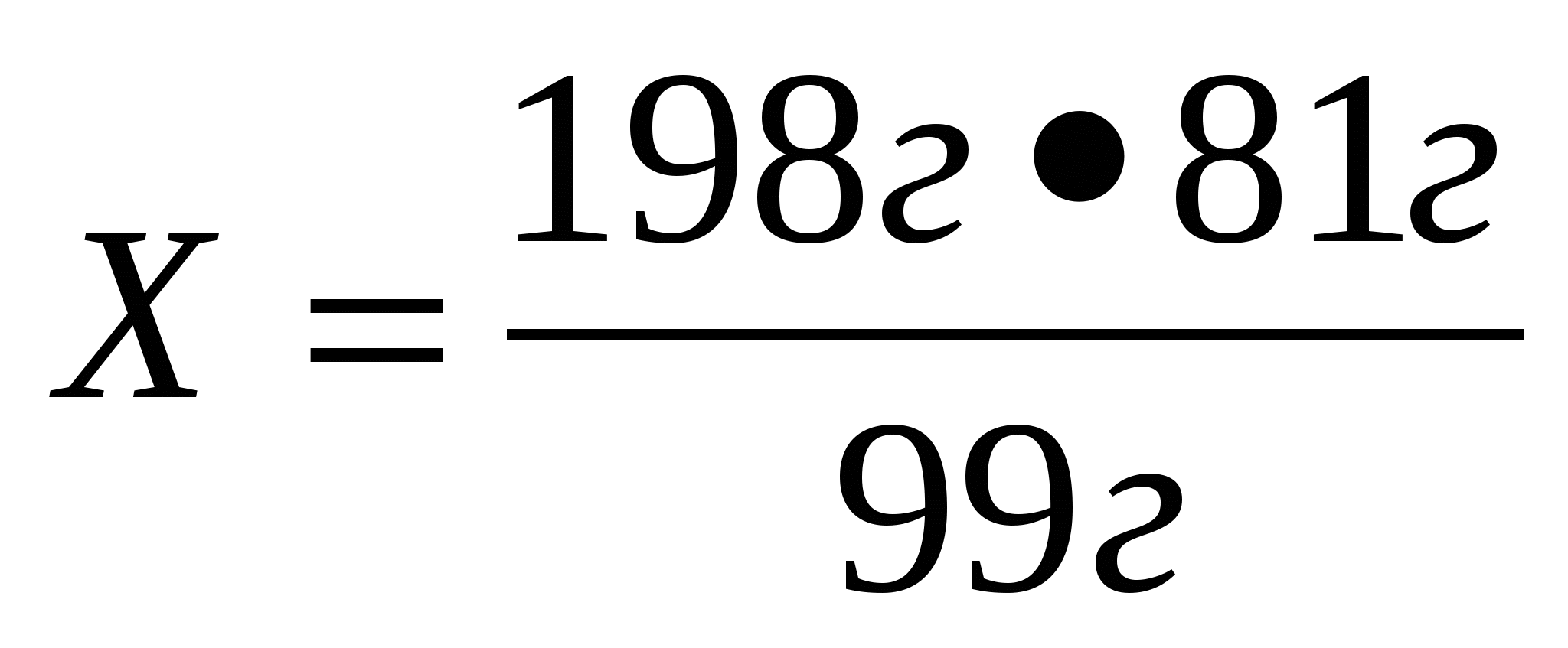
Х = 162г
Ответ: образуется 162г оксида цинка
3
 Дано: 45г Хг
Дано: 45г Хг
m (Fe(OH)2) = 45г Fe(OH)2 = FeO + H2O
m (FeO) = Хг 1моль 1моль
90г/моль 72г/моль
90г 72г
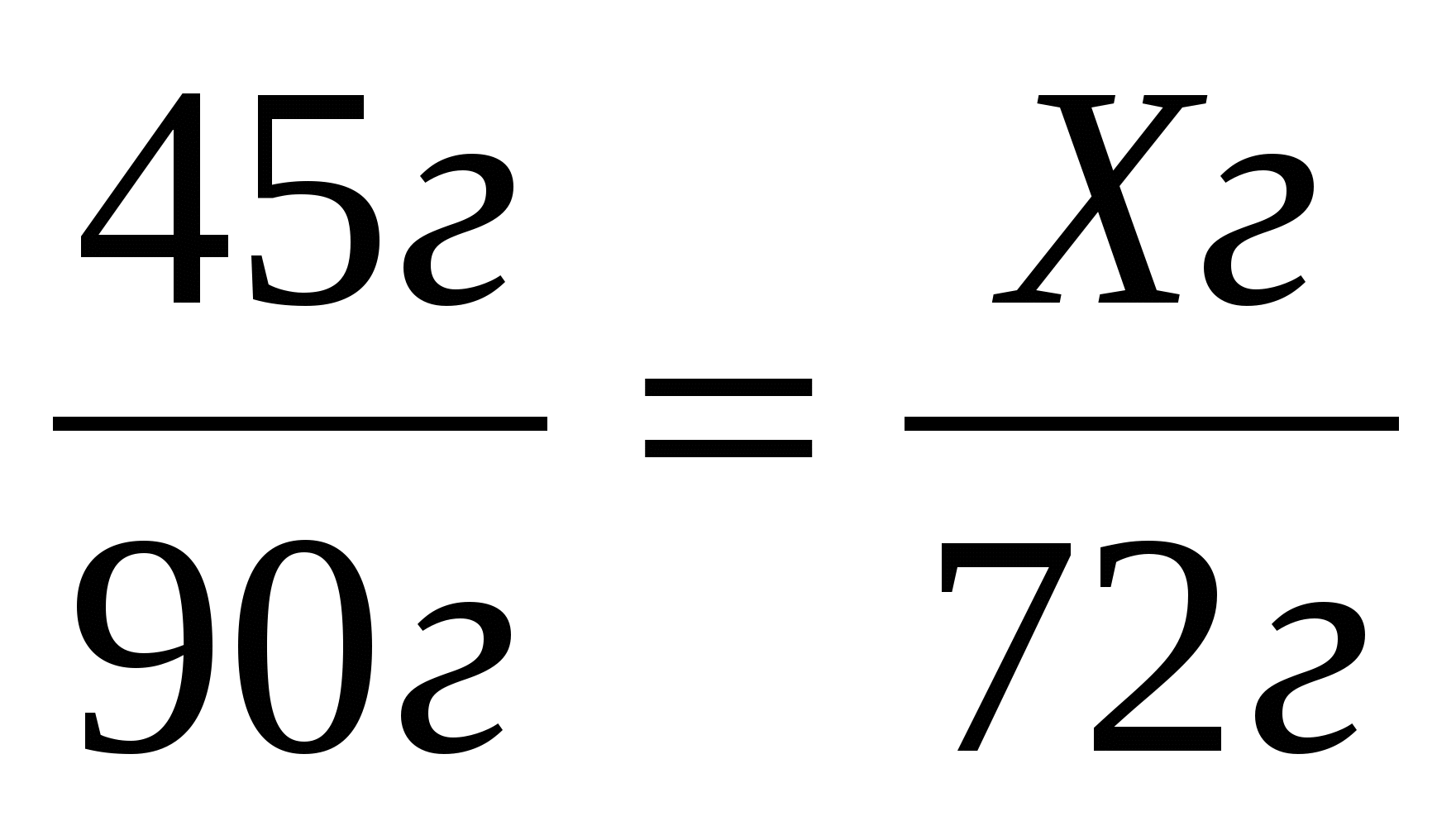
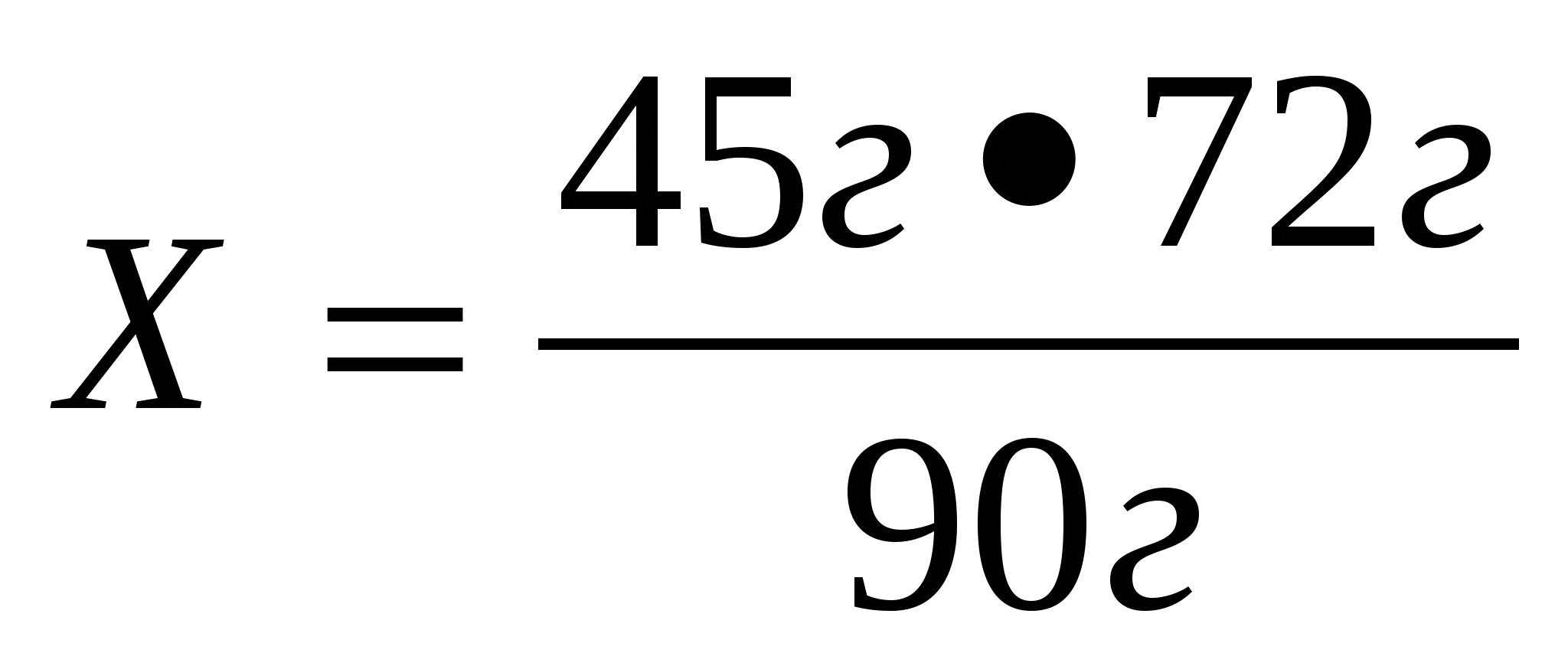
Х = 36г
Ответ: образуется 36г оксида железа
4
 Дано: 112г Хг
Дано: 112г Хг
m (CаО) = 112г CаO + H2O = Са(ОН)2
m (Cа(ОН)2 ) = Хг 1моль 1моль
56г/моль 74г/моль
56г 74г
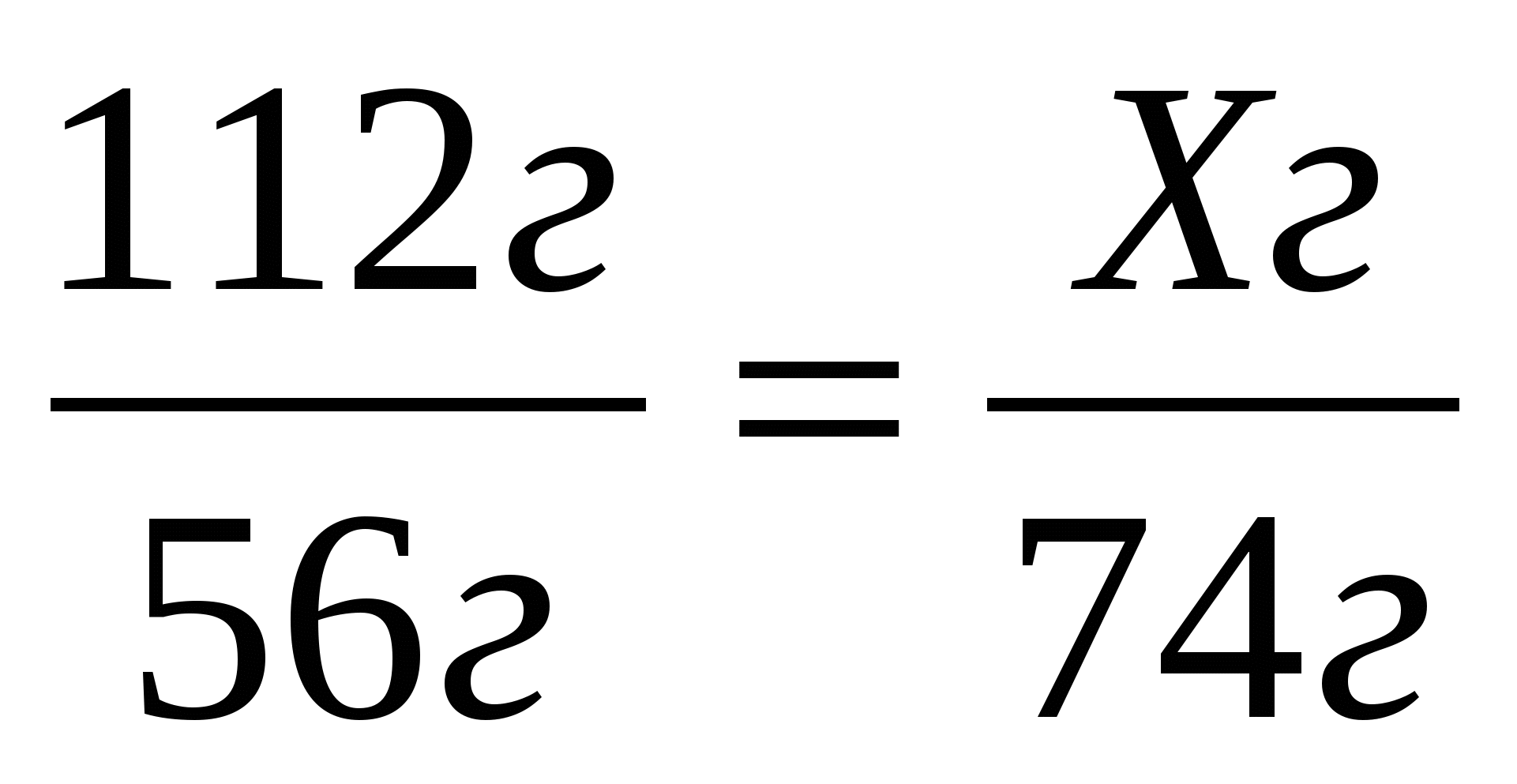
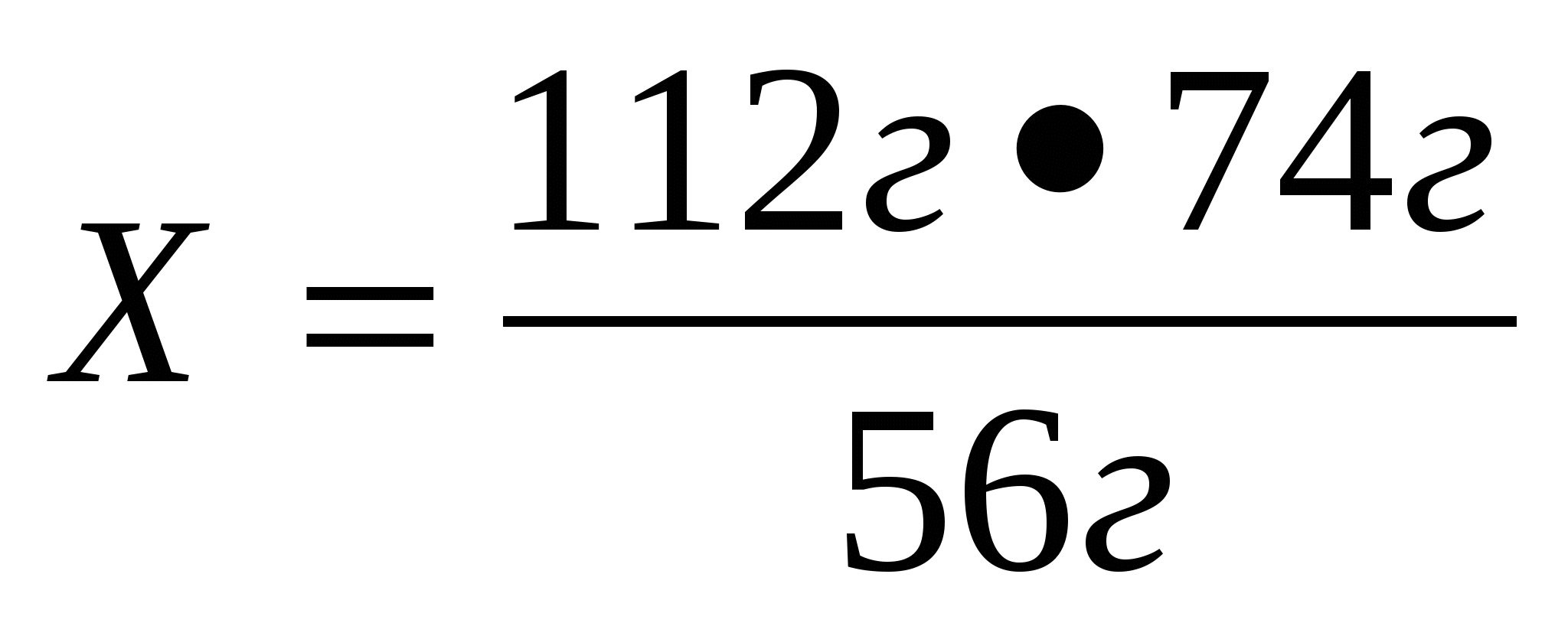
Х = 148г
Ответ: образуется 148г гидроксида кальция
Контрольная работа № 5 Классы неорганических соединений
Часть 1
1
2
3
4
5
6
Вариант 1
2
1
2
1
2
3
Вариант 2
2
3
2
4
1
1
Вариант 3
4
3
1
2
1
3
Вариант 4
1
2
3
4
3
1
7
8
9
Вариант 1
5421
123
125
Вариант 2
5364
126
125
Вариант 3
2145
126
135
Вариант 4
5432
136
246
Часть 2 (возможный вариант ответа)
Вар
Содержание верного ответа и указания по оцениванию
Баллы
Элементы ответа:
-
Записано уравнение реакции в молекулярном виде, указан тип реакции.
-
Записано полное и сокращенное ионное уравнение
Правильно записаны два уравнения в молекулярном виде и два уравнения в ионном виде, указан тип реакции
4
В ответе допущена ошибка в одном уравнении реакции
3
В ответе допущена ошибка в двух уравнениях реакций
2
В ответе допущена ошибка в трех уравнениях реакций
1
Все элементы ответа записаны неверно
0
1
1) H2SO4 + MgO = MgSO4 + H2O - реакция обмена
2H++ SO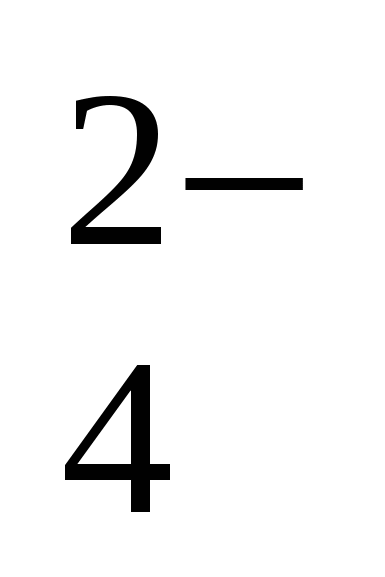 + MgO = Mg2+ + SO
+ MgO = Mg2+ + SO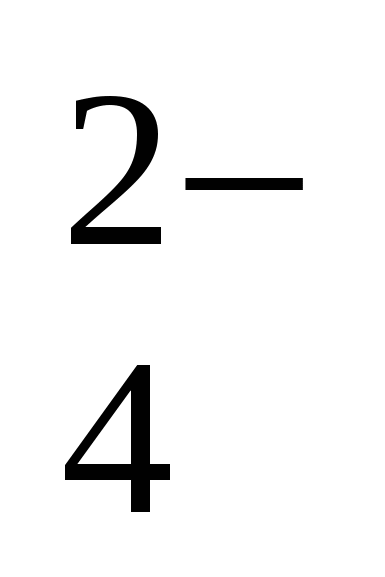 + H2O
+ H2O
2H++ MgO = Mg2+ + H2O
2) H2SO4 + Mg(OH)2 = MgSO4 + 2H2O - реакция обмена
2H++ SO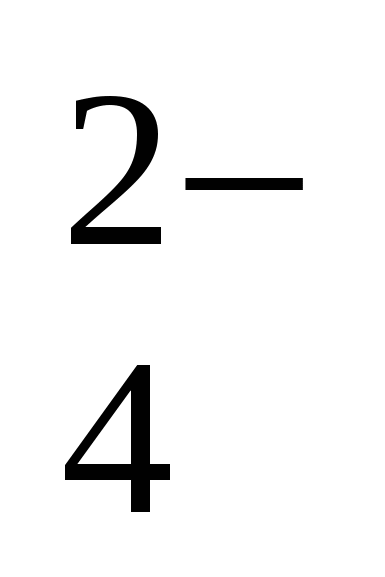 + Mg(OH)2 = Mg2+ + SO
+ Mg(OH)2 = Mg2+ + SO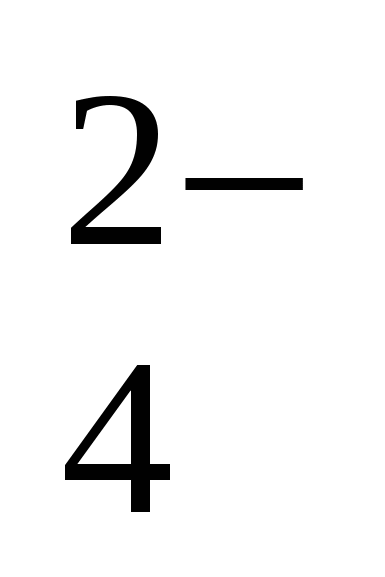 + 2H2O
+ 2H2O
2H++ Mg(OH)2 = Mg2+ + 2H2O
2
1) 2HCl + Zn(OH)2 = ZnCl2 + 2H2O - реакция обмена
2H++ 2Cl + Zn(OH)2 = Zn2+ + 2Cl
+ Zn(OH)2 = Zn2+ + 2Cl + 2H2O
+ 2H2O
2H++ Zn(OH)2 = Zn2+ + 2H2O
2) 2HCl + Zn = ZnCl2 + H2 - реакция замещения
2H++ 2Cl + Zn = Zn2+ + 2Cl
+ Zn = Zn2+ + 2Cl + H2
+ H2
2H++ Zn = Zn2+ + H2
3
1) H3PO4 + 3NaOH = Na3PO4 + 3H2O - реакция обмена
3H+ + PO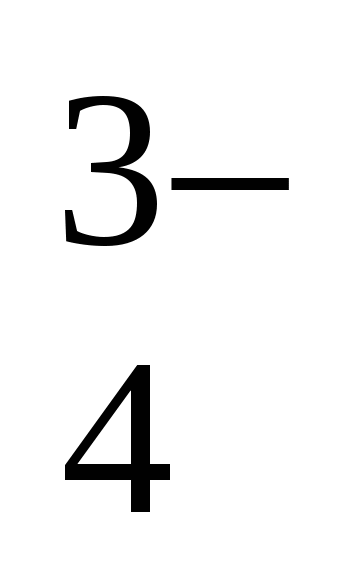 + 3Na+ + 3OH
+ 3Na+ + 3OH = 3Na+ + РO
= 3Na+ + РO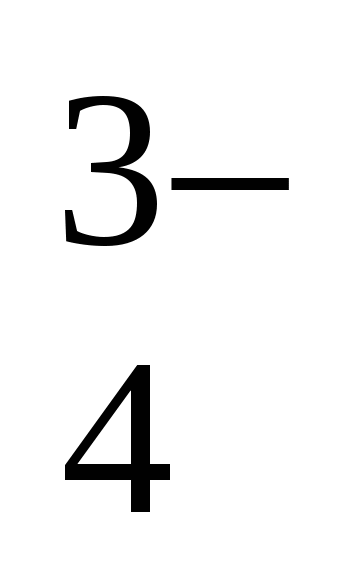 + 3H2O
+ 3H2O
H+ + OH = H2O
= H2O
2) 2H3PO4 + 3Na 2O = 2Na3PO4 + 3H2O - реакция обмена
6H+ + 2PO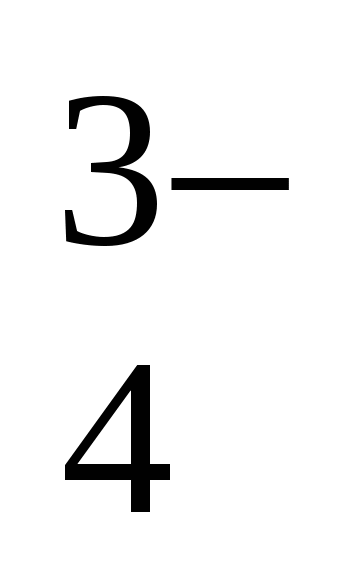 + 3Na2O= 6Na+ + 2PO
+ 3Na2O= 6Na+ + 2PO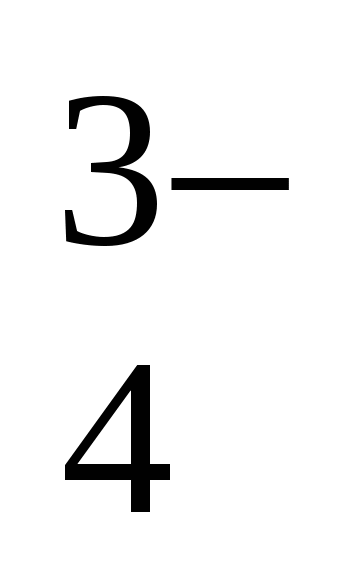 + 3H2O
+ 3H2O
2H+ + Na2O = 2Na+ + H2O
4
1) 2HNO3 + Ca(OH)2 = Ca(NO3)2 + 2H2O - реакция обмена
2H+ + 2NO + Ca2+ + 2OH
+ Ca2+ + 2OH = Ca2+ + 2NO
= Ca2+ + 2NO + 2H2O
+ 2H2O
H+ + OH = H2O
= H2O
2) N2O5 + Ca(OH)2 = Ca(NO3)2 + H2O - реакция обмена
N2O5 + Ca2+ + 2OH = Ca2+ + 2NO
= Ca2+ + 2NO + H2O
+ H2O
N2O5 + 2OH = 2NO
= 2NO + H2O
+ H2O
Контрольная работа № 6
Итоговая контрольная работа за курс 8 класса
Часть 1
1
2
3
4
5
6
Вариант 1
3
3
1
3
3
2
Вариант 2
4
4
2
2
1
2
Вариант 3
4
1
4
1
2
1
Вариант 4
4
4
1
2
3
2
7
8
9
Вариант 1
5431
146
7,5
Вариант 2
6451
234
10,0
Вариант 3
3512
123
9,0
Вариант 4
2561
234
10
Часть 2 (возможный вариант ответа)
Вар
Содержание верного ответа и указания по оцениванию
Баллы
Правильно записаны 4 уравнения в молекулярном виде, указан тип реакции, названы сложные вещества
4
В одном уравнении реакции допущена ошибка или ответ неполный
3
В двух уравнениях реакций допущена ошибка или ответ неполный
2
В трех уравнениях реакций допущена ошибка или ответ неполный
1
Все элементы ответа записаны неверно
0
1
1) 2Fe(OH)3 → Fe2O3 + 3H2O - реакция разложения
гидроксид оксид вода
железа(III) железа(III)
2) Fe2O3 + 3Н2 = 2Fe + 3Н2О- реакция замещения
3) Fe + H2SO4 = FeSO4 + H2 - реакция замещения
серная сульфат
кислота железа(II)
4) FeSO4 + 2NaOH = Fe(OH)2 + Na2SO4 - реакция обмена
гидроксид гидроксид сульфат
натрия железа (II) натрия
2
1) 2Na + 2H2O = 2NaOH + H2 реакция замещения
вода гидроксид
натрия
2) 2NaOH + CuCl2 = Cu(OH)2 + 2NaCl - реакция обмена
хлорид гидроксид хлорид
меди (II) меди (II) натрия
3) Cu(OH)2 = CuO + H2O- реакция разложения
оксид
меди(II)
4) CuO + H2 = Cu + H2O- реакция замещения
3
1) Zn + 2HCl = ZnCl2 + H2 реакция замещения
соляная хлорид
кислота цинка
2) ZnCl2+ 2NaOH = Zn(OH)2 + 2NaCl - реакция обмена
гидроксид гидроксид хлорид
натрия цинка натрия
3) Zn(OH)2 + 2HNO3= Zn(NO3)2 + 2H2O - реакция обмена
азотная нитрат вода
кислота цинка
4) Zn(OH)2 = ZnO + H2O- реакция разложения
оксид
цинка
4
1) Fe + 2HСl = FeCl2 + H2 - реакция замещения
соляная хлорид
кислота железа (II)
2) FeCl2+ 2NaOH = Fe(OH)2 + 2NaCl - реакция обмена
гидроксид гидроксид хлорид
натрия железа (II) натрия
3) Fe(OH)2 → FeO + H2O - реакция разложения
гидроксид оксид вода
железа(II) железа(II)
4) FeO + 3Н2 = 2Fe + 3Н2О- реакция замещения


