- Преподавателю
- Химия
- Алгоэвристическая программа на тему Водород
Алгоэвристическая программа на тему Водород
| Раздел | Химия |
| Класс | 8 класс |
| Тип | Рабочие программы |
| Автор | Шаль О.В. |
| Дата | 30.12.2015 |
| Формат | doc |
| Изображения | Есть |
Алгоэвристическая программа
водород



Сегодня тебе предстоит увлекательное путеествие по миру химии! Ты на поезде посетишь город «водород». Ты узнаешь много нового и интересного! Смелей! В добрый путь!


 Станция 1
Станция 1



 Станция 2
Станция 2
Водород - самый распространённый элемент во Вселенной. На его долю приходится около 92 % всех атомов (8 % составляют атомы гелия, доля всех остальных вместе взятых элементов - менее 0,1 %). Таким образом, водород - основная составная часть звёзд и межзвёздного газа. В условиях звёздных температур (например, температура поверхности Солнца ~ 6000 °C) в межзвёздном пространстве этот элемент существует в виде отдельных молекул, атомов и ионов и может образовывать молекулярные облака, значительно различающиеся по размерам, плотности и температуры. 
Массовая доля водорода в земной коре составляет 1 % - это десятый по распространённости элемент. Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и кислорода. В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях, практически весь водород на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества содержится в атмосфере (0,00005 % по объёму).
Водород входит в состав практически всех органических веществ и присутствует во всех живых клетках. В живых клетках по числу атомов на водород приходится почти 50 %.
Задание 1: заполните таблицу исходя из текста
Я это знал
Я узнал нового…

 Станция 3
Станция 3
Задание 2 охарактеризуйте положение водорода в периодической системе химических элементов Д. И. Менделеева, дополните предложения:
1
Водород
H
1,0079
 1s1
1s1
водород - элемент …… подгруппы ….. группы …… периода периодической системы химических элементов Д. И. Менделеева, с атомным номером ….. Обозначается символом …..Так как у атома водорода на внешнем уровне ___ электрона, то водород в соединениях проявляет степень окисления ___.

 станция 4
станция 4
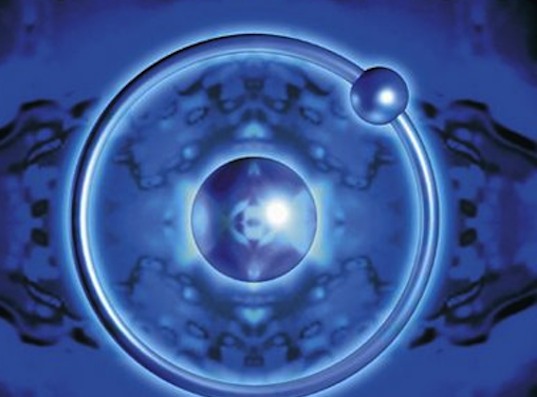
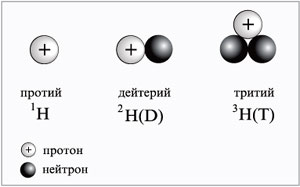
. Водород - это самый легкий газ (он в 14,4 раза легче воздуха), не имеет цвета, вкуса и запаха. Мало растворим в воде (в 1 л воды при 20°С растворяется 18 мл водорода). При температуре - 252,8°С и атмосферном давлении переходит в жидкое состояние. Жидкий водород бесцветен. Кроме водорода с массовым числом 1 существуют изотопы с массовыми числами 2 и 3 - дейтерий D и тритий Т.

З
 адание 4
адание 4




 ….
…. 







…. 

 Станция 5
Станция 5
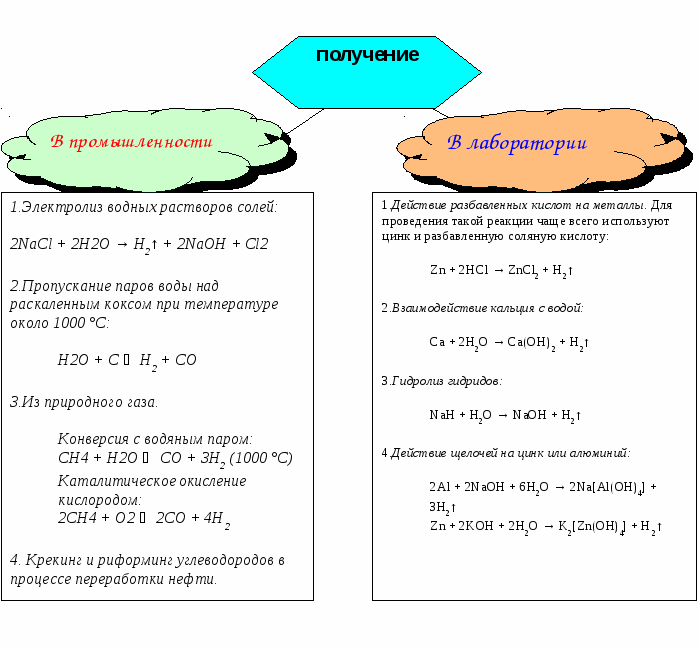

 Станция 5
Станция 5
Задание! Допиши уравнения реакций
Молекулы водорода Н2 довольно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:
Н2 = 2Н − 432 кДж
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция: (уравнение!..........................................................................................)
и с единственным неметаллом - фтором, образуя фтороводород
(уравнение!..........................................................................................)
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии
Взаимодействие со щелочными и щёлочноземельными металлами
При взаимодействии с активными металлами водород образует гидриды:
2Na + H2 → …..
Ca + H2 → ….
Mg + H2 → …
С галогенами образует галогеноводороды:
F2 + H2 →…(протекает со взрывом в темноте
и при любой температуре)
Cl2 + H2 →…(реакция протекает со взрывом,
только на свету)
Взаимодействие с оксидами металлов
Оксиды восстанавливаются до металлов
CuO + H2 → …
Fe2O3 + 3H2 → …
WO3 + 3H2 → ….

 Станция 6
Станция 6
Запомни!!!



Превосходно!!! Ты преодалел этот сложный путь по изучению города «Водород»…остается последняя станция!.... с

 пеши мой друг!...осталось немного!
пеши мой друг!...осталось немного!

 Станция 7
Станция 7