- Преподавателю
- Химия
- Разработка урока по химии
Разработка урока по химии
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Махмутова О.А. |
| Дата | 20.04.2015 |
| Формат | docx |
| Изображения | Есть |
План-конспект
Урок №
Дата проведения: ________________
Тема урока: Решение расчетных задач: вычисление массовой доли растворенного вещества, массы растворителя, растворенного вещества.
Цели урока:
- образовательные: Создать условия для развития навыков решения задач по формулам.
- воспитательные: Воспитание чувства товарищества, ответственности.
- развивающие: Развитие умения анализировать, рассуждать.
Тип урока: урок комплексного применения знаний
Ход урока
-
Организационный момент
Приветствие!
Проверка готовности к уроку. (Учащиеся заранее делятся на группы)
Учащиеся записывают тему урока и на полях в тетради отмечают смайликом свое настроение на начало урока.
-
Повторение полученных ранее знаний
Блок № 1
(Учащиеся работают в парах, результаты работы заносят в листы ответов)
Найти соответствие (соединить стрелочками):
-
Количество вещества
г/моль, кг/моль
Массовая доля растворенного
вещества
Дж, кДж, мДж
Количества теплоты
г, кг
Масса
Моль/л
Объем
6,02 * 1023
Молярная концентрация
%
Число Авогадро
22,4 л
Молярный объем
л, м3
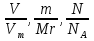
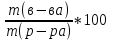
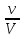
Далее идет взаимопроверка (ответы на слайде презентации), обучающиеся ставят отметку о правильности выполнения на полях в листе ответа («*» - все правильно, «+» - одна - две ошибки, «-» три и более ошибок).
Блок № 2
Работа в группах (каждый участник выбирает 1 задачу, задачи расположены от простой к более сложной)
-
Определите, сколько потребуется соли и воды, чтобы приготовить 200 г раствора, содержащего 15% соли.
-
Для консервирования огурцов используют 5%-ный раствор поваренной соли. Сколько потребуется поваренной соли NaCl и воды для приготовления 1 кг (1000г) 5% - ного раствора?
-
Вычислите массу гидроксида натрия, необходимого для приготовления 400 г 20%-го раствора гидроксида натрия.
-
К 100 г 20% - ного раствора соли добавили 50 г 32% -ного раствора соли. Вычислите массовую долю растворенного вещества в полученном растворе.
Во время работы групп на интерактивной доске работает таймер отсчета времени. Учитель сам устанавливает регламент на решения задач, в зависимости от темпа работы класса. Опрос происходит следующим образом, каждая группа презентует по одной решенной задачи. Другие группы маркеруют на полях своих рабочих листов пометки о правильности решения задач («*» - нет ошибок, «+» - ошибки в вычислении, «-» - все не правильно).
Блок № 3
-
Вычислите массы водорода и кислорода, образовавшегося при разложении 72 г воды.
-
Определите число молей СаО, образовавшегося при горении 20 г Са на воздухе.
-
Дано термохимическое уравнение:
Н2О = Н2 + О2 - 571,6 кДж
Для проведения этой реакции затрачивается 258,5 кДж теплоты. Сколько молей моды при этом разложится?
-
Для образования 1 моля NO требуется 90,37 кДж теплоты. Вычислите массу оксида азота (II), образовавшегося при поглощении теплоты в количестве 9037 кДж.
Проверка происходит также как и во втором блоке.
-
Рефлексия
Момент урока, вызвавший интерес
Что не понравилось на уроке
Моя (личная) активность (по пятибалльной системе)
Моя оценка за весь урок (1-5 баллов)
Мои предложения по уроку
-
Домашнее задания
§ 38 с.97-100 № 5,6
Учащиеся выходя из кабинета на стикерах пишут свое отношение к уроку и клеят их либо на солнышко, либо на тучку.


