- Преподавателю
- Химия
- Учебный материал к темеНЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
Учебный материал к темеНЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Ермакова Е.В. |
| Дата | 17.09.2015 |
| Формат | docx |
| Изображения | Есть |



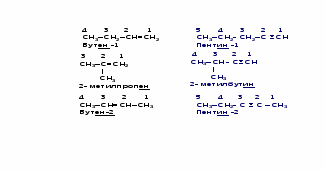
 НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
-
Гомологи - вещества, сходные по строению и химическим свойствам, но отличающиеся друг от друга по составу молекул на одну или несколько групп атомов - СН2-
-
Группа атомов - СН2- называется гомологической разностью.
ВИДЫ ИЗОМЕРИИ
НОМЕНКЛАТУРА
АЛКАНЫ
Углеродного скелета
Суффикс ан. Нумеруют углеродную цепь со стороны, где ближе радикал.
АЛКЕНЫ
Углеродного скелета.
Положения двойной связи. Межклассовая. Пространственная
Суффикс ан, меняется на ен или илен.
Нумеруют углеродную цепь со стороны, где ближе двойная связь, её местоположение указывается цифрой в конце названия.
АЛКИНЫ
Углеродного скелета.
Положения тройной связи.
Межклассовая.
Суффикс ан, меняется на ин.
Нумеруют углеродную цепь со стороны где ближе тройная связь, её местоположение указывается цифрой в конце названия.
Тип гибридизации
Строение атома С в пространстве
Валентный угол между гибридными орбиталями
Пример молекулы
Длина связи между атомами С, нм
Энергия связи между атомами С, кДж/моль
Виды КС
SP3
тетраэдрическое
109028/
СН3 - СН3
0,154
369
σ
SP2
тригональное
1200
СН2= СН2
0,134
712
σ и π
SP
линейное
1800
СН ≡ СН
0,120
962
σ и π
ФИЗИЧЕСКИЕ СВОЙСТВА
С2 - С4 Газы.
С5 - С18 Жидкости.
С19 … Твердые.
Mr, Т кипения и плавления увеличиваются.
Растворимость в воде уменьшается
ХИМИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ
I. Реакции присоединения
1. галогенирование: СН2=СН2+ Br2 → BrCH2-CH2Br (дибромэтан) качественная реакция на непредельные углеводороды, красно-бурая окраска бромной воды обесцвечивается.
2. с галогеноводородами по правилу Марковникова: CH3-CH=CH2+HBr→CH3-CHBr-СH3;
галоген присоединяется к менее гидрированному атому С, водород к более гидрированному атому углерода при присоединении по двойной связи.
3. с водой, реакция гидратации: СН2=СН2+Н20 →СН3-СН2ОН
4. гидрирование: СН2=СН2 + Н2 → СН3 - СН3
II. Реакции окисления 1. ЗСН2=СН2 + 4Н20 + 2КМп04 → ЗСН2ОН-СН2ОН + 2Mn02 + 2KOH
обесцвечивание раствора, качественная реакция.
2. Горение С2Н4 + 302 → 2С02 + 2Н20 светящееся пламя
III. Полимеризация nСН2=СН2 → (- СН2- СН2-)n
ПОЛУЧЕНИЕ АЛКЕНОВ
Дегидратация спиртов (лабораторный способ)
при t > 150 °C в присутствии водоотнимающих реагентов (H2SO4) CH3CH2OH ® CH2=CH2 + H2O
Крекинг алканов: CnH 2n+2 ®¾ CnH2n + CnH 2n+2, Например: С7Н16 ®¾ СН3-СН=СН2 + С4Н10
Дегидрогалогенирование моногалогеналканов при действии спиртового_раствора щелочи:
СН3-СНBr-CH3 + KOH (спирт) ® CH3-CH=CH2 + KBr + H2O
Дегалогенирование дигалогеналканов, имеющих атомы галогена у соседних атомов углерода, при действии активных металлов: СH2Br-CHBr-CH3 + Mg ® CH2=CH-CH3 + MgBr2
Дегидрирование алканов при 500 °С Cr2O3
СH3-CH-CH2 ® CH3-CH =CH2 + Н2
½ ½
Н Н
ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
I. Реакции присоединения
1. галогенирование: СН ≡ СН+ Cl2 →ClCH = CHCl качественная реакция на непредельные углеводороды, красно-бурая окраска бромной воды обесцвечивается.
2. с галогеноводородами по правилу Марковникова: CH3-C≡CH+HBr → CH3-CBr=СH2;
3. с водой реакция гидратации: СН ≡ СН+Н20 → СН3-СОН
4. гидрирование: СН ≡ СН + Н2 → СН2 = СН2
II. Реакции окисления 1. СН≡СН + КМп04 → обесцвечивание раствора, качественная реакция.
2. Горение 2С2Н2 + 502 → 4С02 + 2Н20 коптящее пламя
III. Тримеризация 3СН≡СН → С6Н6
ПОЛУЧЕНИЕ АЛКИНОВ
1. Гидролиз карбида кальция:CaC2 + 2H2O ® C2H2 + Ca(OH)2
2. Термический крекинг метана: 1500°С
2СН4 ® С2Н2 + 3Н2
Для синтеза гомологов ацетилена применяют следующие методы:
3. Каталитическое дегидрирование алканов: СnH2n+2 ® CnH2n-2 + 2H2
4. Дегидрогалогенирование дигалогеналканов спиртовым раствором щелочи (щелочь и спирт берутся в избытке): спирт
СН3-CH2-CBr2- СН3 + 2KOH ® СН3-CºC- СН3 + 2KBr + 2H2O
спирт
СН3-CHBr-CHBr-СН3 + 2KOH ® СН3-CºC- СН3 + 2KBr + 2H2O


