- Преподавателю
- Химия
- Тематические тесты за курс основной школы по химии
Тематические тесты за курс основной школы по химии
| Раздел | Химия |
| Класс | - |
| Тип | Тесты |
| Автор | Ларина О.В. |
| Дата | 23.10.2014 |
| Формат | docx |
| Изображения | Есть |
Характерные химические свойства оксидов: основных, амфотерных, кислотных.
1.Оксид углерода (IV) реагирует с каждым из двух веществ:
1)
водой и оксидом кальция
2)
кислородом и оксидом серы (IV)
3)
сульфатом калия и гидроксидом натрия
4)
фосфорной кислотой и водородом
2.Оксид серы (VI) взаимодействует с каждым из двух веществ:
1)
вода и соляная кислота
2)
кислород и оксид магния
3)
оксид кальция и гидроксид натрия
4)
вода и медь
3.Оксид серы (VI) взаимодействует с каждым из двух веществ:
1)
вода и кислород
2)
оксид магния и азотная кислота
3)
оксид кальция и гидроксид натрия
4)
вода и водород
4.Между собой взаимодействуют
1)
SiO2 и H2O
2)
CO2 и H2SO4
3)
CO2 и Сa(OH)2
4)
Na2O и Сa(OH)2
5.Вещество, которое может реагировать с водородом, серной кислотой и алюминием, имеет формулу
1)
P2O5
2)
CuO
3)
Ba(NO3)2
4)
K2O
6.Оксид серы (IV) не взаимодействует с
1)
O2
2)
H2O
3)
CO2
4)
NaOH
7. Оксид серы (IV) проявляет свойства
1)
основного оксида
2)
амфотерного оксида
3)
кислотного оксида
4)
несолеобразующего оксида
8. Оксид кальция взаимодействует с каждым из трех веществ:
1)
кислород, вода, серная кислота
2)
соляная кислота, углекислый газ, вода
3)
оксид магния, оксид серы (IV), аммиак
4)
железо, азотная кислота, оксид фосфора (V)
9.Вещество, которое может реагировать с водородом, серной кислотой и углеродом, имеет формулу
1)
NH3
2)
CuO
3)
CaCO3
4)
NaOH
Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот.
-
Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с
1)
CuO
2)
H2SO4
3)
CO2
4)
NaOH
2.Гидроксид цинка реагирует с каждым веществом пары
1)
сульфат кальция и оксид серы (VI)
2)
гидроксид натрия (р-р) и соляная кислота
3)
вода и хлорид натрия
4)
сульфат бария и гидроксид железа (III)
3. Гидроксид алюминия реагирует с каждым веществом
1)
сульфат кальция и оксид серы (VI)
2)
гидроксид натрия (р-р) и азотная кислота
3)
водород и хлорид натрия
4)
сульфат бария и гидроксид железа (III)
4. Разбавленная серная кислота может реагировать с каждым из двух веществ:
1)
серой и магнием
2)
оксидом железа (II) и оксидом кремния (IV)
3)
гидроксидом калия и хлоридом калия
4)
нитратом бария и гидроксидом меди (II)
5.Реакция нейтрализации происходит между
1)
цинком и соляной кислотой
2)
серной кислотой и хлоридом бария
3)
гидроксидом кальция и азотной кислотой
4)
гидроксидом натрия и сульфатом меди
6.Гидроксид кальция реагирует с каждым веществом пары
1)
сульфат натрия и оксид серы (VI)
2)
гидроксид натрия (р-р) и соляная кислота
3)
хлорид натрия и оксид углерода (IV)
4)
сульфат бария и гидроксид железа (III)
7.Соляная кислота не взаимодействует ни с одним из двух веществ:
1)
цинком и гидроксидом натрия
2)
медью и оксидом меди (II)
3)
ртутью и оксидом углерода (IV)
4)
магнием и аммиаком
8. Гидроксид натрия не реагирует с
1)
Al(OH)3
2)
ZnO
3)
H2SO4
4)
Ba(OH)2
9. Разбавленная серная кислота реагирует с каждым из двух веществ:
1)
Na2SiO3 и HNO3
2)
Fe2O3 и KNO3
3)
Ag и Cu(OH)2
4)
Fe и Al2O3
10. Концентрированная азотная кислота при обычных условиях не взаимодействует с
1)
магнием
2)
гидроксидом натрия
3)
железом
4)
оксидом магния
Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка).
-
Карбонат калия в растворе не взаимодействует с
1)
азотной кислотой
2)
углекислым газом
3)
сульфатом натрия
4)
хлоридом меди (II)
-
С каждым из перечисленных веществ:
H2S, KOH, Zn
взаимодействует
1)
Pb(NO3)2
2)
ZnSO4
3)
Na2CO3
4)
HCl
-
В уравнении реакции
2AgNO3 = 2Ag + 2X + O2
веществом «X» является
1)
оксид азота (IV)
2)
оксид азота (II)
3)
азот
4)
оксид азота (V)
-
Раствор сульфата меди (II) реагирует с каждым из двух веществ:
1)
HCl и H2SiO3
2)
H2O и Cu(OH)2
3)
О2 и HNO3
4)
NaOH и BaCl2
-
С гидроксидом натрия, хлороводородной кислотой и хлоридом бария может реагировать
1)
Cr(OH)3
2)
CuSO4
3)
(NH4)2CO3
4)
Zn
-
В результате кипячения водного раствора гидрокарбоната кальция в осадок выпадает
1)
оксид кальция
2)
карбид кальция
3)
гидроксид кальция
4)
карбонат кальция
-
Хлорид железа (II) реагирует с каждым из двух веществ:
1)
MgO и HCl
2)
Zn и AgNO3
3)
HNO3 и CO2
4)
CaO и CO2
-
Карбонат натрия в растворе не взаимодействует с
1)
серной кислотой
2)
углекислым газом
3)
сульфатом натрия
4)
хлоридом железа (II)
-
С водными растворами хлороводорода, гидроксида бария и хлорида меди (II) реагирует
1)
CaCO3
2)
K2SO3
3)
Na2SO4
4)
Al2(SO4)3
-
Хлорид меди (II) реагирует с каждым из двух веществ:
1)
MgO и HNO3
2)
AgNO3 и Fe
3)
CO2 и H3N
4)
CaO и NaOH
Взаимосвязь неорганических веществ
-
В схеме превращений
FeCl2 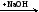 X1
X1 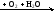 X2
X2
веществом «X2» является
1)
FeO
2)
Fe(OH)3
3)
FeCl2
4)
FeCl3
-
В схеме превращений
FeCl3 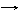 X1
X1 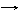 X2
X2 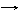 Fe(OH)3
Fe(OH)3
веществами «Х1» и «Х2» могут быть соответственно
1)
Fe2(SO4)3 и Fe2O3
2)
FePO4 и Fe3O4
3)
Fe(NO3)3 и Fe2O3
4)
Fe(OH)3 и Fe2(SO4)3
-
В схеме превращений
CaCO3 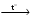 X1
X1 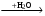 X2
X2
веществом «X2» является
1)
CaO
2)
Ca(OH)2
3)
Ca(HCO3)2
4)
CaH2
-
В схеме превращений
CaCO3  X1
X1 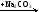 X2 + NaCl
X2 + NaCl
веществом «X2» является
1)
CaCO3
2)
CaCl2
3)
CaO
4)
Ca(OH)2
-
В cхеме превращений
ZnO ® X1 ® X2 ® Zn(OH)2
веществами «Х1» и «Х2» соответственно являются
1)
Zn(OH)2 и ZnCl2
2)
Zn(OH)2 и ZnSO4
3)
ZnCl2 и ZnSO4
4)
ZnCl2 и ZnO
-
В схеме превращений
Cu(OH)2 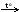 A
A 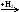 B
B 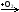 X
X
веществом «X» является
1)
CuO
2)
Cu
3)
Cu(OH)2
4)
CuCl2
-
В схеме превращений
Fe(OH)3 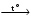 X1
X1 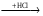 X2
X2
веществом «X2» является
1)
Fe2O3
2)
FeO
3)
FeCl3
4)
FeCl2
-
В схеме превращений
Al(OH)3 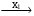 Y
Y 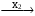 Al(OH)3
Al(OH)3
веществами «X1» и «X2» могут быть соответственно
1)
K2SO4 и KOH
2)
NaCl и HCl
3)
Na2SO4 и H2SO4
4)
HNO3 и NaOH
-
В схеме превращений
Al 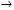 X1
X1 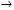 X2
X2 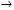 Al
Al
веществами «X1» и «X2» могут быть, соответственно,
1)
Al(NO3)3 и Al(OH)3
2)
AlPO4 и Al(OH)3
3)
Al(OH)3 и Al2(SO4)3
4)
Al2O3 и AlCl3
Часть А. Свойства оснований, кислот, солей.
1. Гидроксид алюминия реагирует с каждым из двух веществ:
1. HCl и Fe
2 NaCl и NH3
3. CO и H2S
4 NaOH и HNO3
2.Наиболее сильные кислотные свойства проявляет
1. Гидроксид цинка
2 Гидроксид фосфора (V)
3. Гидроксид серы (VI)
4 Гидроксид алюминия (III)
3.Соль образуется при взаимодействии разбавленной соляной кислоты с
каждым из двух веществ:
1 Zn и ZnO
2. SO3 и Zn(OH)2
3 SO2 и Cu(OH)2
4. Cu и CuO
4. Основные свойства гидроксид железа (III) проявляет в реакции:
1 FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
2 2Fe(OH)3 → Fe2O3 + 3H2O
3. Fe(OH)3 + 3 KOH → K3[Fe(OH)3]
4 Fe(OH)3 + 3HCl → FeCl3 + 3H2O
5.Концентрированная азотная кислота реагирует с каждым из двух веществ:
1. Au и NaOH
2. Cu и NaOH
3. H2SO4 и AgNO3
4. Fe и SiO2
6.C концентрированной серной кислотой не будут взаимодействовать при обычных условиях:
1. Fe, Al
2 Cu, Al
3. Mg, Zn
4 Cu, Ag
5.C разбавленной серной кислотой взаимодействует
1. кремний
2 медь
3 ртуть
4. цинк
6.И с серной кислотой и с гидроксидом калия в их водных растворах вступают в реакцию все вещества набора:
1. H2, Na2CO3, Al2O3
2. Al(OH)3, Zn, K2CO3
3. Ag, Zn(OH)2, CaCO3
4 Al, (NH4)2CO3, Ba(NO3)2
7.Гидроксид алюминия реагирует с каждым из двух веществ:
1. CO и H2S
2. HCl и Fe
3. NaCl и NH3
4. NaOH и HNO3
8.С разбавленной серной кислотой взаимодействует каждое из двух
веществ:
1 цинк и оксид меди (II)
2 медь и оксид азота (IV)
3. водород и сероводород
4. оксид железа (II) и ртуть
9.C разбавленной серной кислотой реагирует каждое из двух веществ:
1 Zn и MgO
2. NaCl и Ag
3 Cu и KNO3
4. CaO и Au
10.Раствор гидроксида калия взаимодействует с:
1 раствором сульфата натрия
2 раствором аммиака
3 оксидом серы (VI)
4 оксидом железа (II)
11 .Гидроксид меди (II) реагирует с каждым из двух веществ:
1 FeO и HCl
2. HNO3 и Al2O3
3 HCl и HNO3
4 HCl и MgO
12. Соль образуется при взаимодействии разбавленной соляной кислоты с
каждым из двух веществ:
1. SO2 и Cu(OH)2
2 Zn и ZnO
3 SO3 и Zn(OH)2
4 Cu и CuO
13. .C гидроксидом калия взаимодействует каждое из двух веществ:
1. HNO3 и CO2
2 MgO и H2SO4
3. SO2 и K2SO4
4 Al2O3 и NaOH
14. .Разбавленная серная кислота реагирует с каждым из двух веществ:
1. Хлоридом бария и цинком
2. Азотной кислотой и оксидом цинка
3. Железом и оксидом серы (IV)
4 Оксидом углерода (IV) и оксидом меди (II)
15. При взаимодействии 1 моль NaOH и 1 моль СО2 образуется
1. Оксид натрия
2 Пероксид натрия
3. Гидрокарбонат натрия
4. Карбонат натрия
16.Образование водорода происходит при взаимодействии
1. HNO3 и Zn
2 H2SO4 (разб.) и Cu
3. HNO3 и Cu
4. H2SO4 (разб.) и Zn
17. Гидроксид калия взаимодействует с каждым из группы веществ:
1. CaO, HCl, NaCl
2. CO2, Ca(OH)2, HNO3
3. SO3, H2SO4, CuCl2
4. H2S, CuO, H2SO3
18. Взаимодействует как с кислотами, так и со щелочами, каждое из пары веществ:
1. Гидроксид бериллия и оксид кремния;
2 Оксид бериллия и гидроксид алюминия;
3. Оксид алюминия и соляная кислота;
4. Оксид цинка и оксид калия.
19. С каждым из веществ, формулы которых KOH, Al2O3, Pb(NO3)2, взаимодействует:
1. Серная кислота;
2. Соляная кислота;
3. Гидроксид натрия;
4. Хлорид натрия.
20. С каждым из веществ, формулы которых HCl, ZnO, CuSO4, взаимодействует:
1. Оксид серы (IV) 2 Азотная кислота;
3. Гидроксид натрия; 4. Гидроксид железа (III).
21. С хлоридом меди (II) взаимодействует:
1. Оксид серы (VI)
2 Гидроксид кальция;
3. Гидроксид железа (III)
4. Серная кислота.
22. Сульфат железа (II) не взаимодействует с:
1. Гидроксидом натрия;
2 Карбонатом кальция;
3. Хлоридом бария;
4 Сероводородной кислотой.
23. Сульфат натрия реагирует с:
1. KOH
2 BaSO3
3. H3PO4
4. Ba(NO3)2
24. Хлорид цинка и вода образуются при взаимодействии
1. Цинка с газообразным хлором;
2 Цинка с соляной кислотой;
3, Цинка с хлоридом меди (II)
4. Гидроксида цинка с соляной кислотой.
25. Как гидроксид натрия, так и железо реагируют с
1. Карбонатом калия
2. Хлоридом бария
3. Сульфатом меди (II)
4. Сульфатом натрия.
26. Как гидроксид калия, так и цинк реагирует с
1. Карбонатом калия 2. Сульфатом меди (II)
3. Хлоридом натрия 4. Сульфатом натрия


