- Преподавателю
- Химия
- Разработка урока Чистые вещества и смеси
Разработка урока Чистые вещества и смеси
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Кожевникова Е.П. |
| Дата | 03.01.2016 |
| Формат | docx |
| Изображения | Есть |






 Химия 8 класс
Химия 8 класс
Тема:«Чистые вещества и смеси»
Цели урока:
1. Сформировать понятия о чистом веществе и смеси веществ
2. Ознакомить со способами разделения смесей
Ход урока:
1. Организационный момент.
Проверка домашнего задания:
Учитель проводит фронтально химическую разминку - тренинг : выполняем № 6,7 с.91
2. Понятие о чистом веществе и смеси.
Объяснение нового материала учитель начинает с беседы:
- Что называют веществом? (Вещество - это то, из чего состоят физические тела)
- Нам хорошо знакомо, что такое чистота. Чистая комната, чистая тетрадь, чистая одежда… А что подразумевает собой понятие чистое вещество?
- Тема сегодняшнего урока: «Чистые вещества и смеси» (запись даты и темы урока учащимися в тетради ).
- А чем отличается чистое вещество от смеси веществ?
Цели урока обсуждаются с учащимися:
- Выяснить, какое вещество считают чистым. Что такое смесь? Какие бывают смеси? Какими способами можно разделить смеси?
Учитель предлагает ученикам рассмотреть смеси, находящиеся на демонстрационном столе . Далее учитель вместе с учениками формирует определение смеси, как комбинации из нескольких веществ, находящихся в непосредственном контакте друг с другом (учащиеся фиксируют определение в тетради).
Учитель дополняет, что в природе нет абсолютно чистых веществ, все они встречаются преимущественно в виде смесей. Приводим примеры смесей, дети записывают их в тетради:
- воздух (смесь газов - азота, кислорода, аргона и др.) - газообразная смесь
- морская вода, минеральная вода с газом, молоко, сок, кофе, раствор соли (сахара) в воде - жидкие смеси
- гранит, сплавы металлов - твердые смеси
Работа с рис.44 в учебнике .Вывод:
Развивая тему, учитель сообщает, что для научных исследований и в промышленности, в основном, требуются чистые вещества. Некоторые примеси даже в небольших количествах способны сильно поменять свойства веществ. В тоже время, необходимо выделить, что невозможно получить абсолютно чистое вещество, т. к. любое чистое вещество содержит хотя бы ничтожное количество примесей.
Если масса одного компонента в десятки раз меньше массы другого компонента смеси, то его называют примесью. Говорят, что вещество загрязнено. Например, воздух может быть загрязнен угарным газом, продуктом неполного сгорания органических соединений, в частности бензина. Кстати, бензин - это смесь органических веществ - углеводородов.
Даем определение чистого вещества ( запись в тетради):
- Чистым называется вещество, которое обладает постоянными физическими свойствами.
В чистом веществе примеси, хотя и присутствуют в незначительном количестве, но не влияют на его физические и химические свойства. Пример чистого вещества - дистиллированная вода.
Учитель отмечает, что в смесях каждое из составляющих их веществ сохраняет свои индивидуальные свойства. Для подтверждения этих слов учитель демонстрирует смесь порошков железа и серы, разделяет эту смесь действием магнита и делает вывод: железо обладает способностью намагничиваться, а сера - нет.
Развивая тему, учитель обращает внимание учеников на смеси, представленные на демонстрационном столе: смесь речного песка и поваренной соли, смесь сахара и поваренной соли, смесь воды и масла, смесь глины или мела с водой. Сравниваем эти смеси с растворами сахара (соли) в воде. Отмечаем, что в одних смесях мы можем различить отдельные компоненты смеси, в других же - различить частицы веществ, входящих в состав смеси невозможно. Классифицируем по этому признаку смеси на однородные и неоднородные, демонстрируем слайд, приводим схему в тетради:
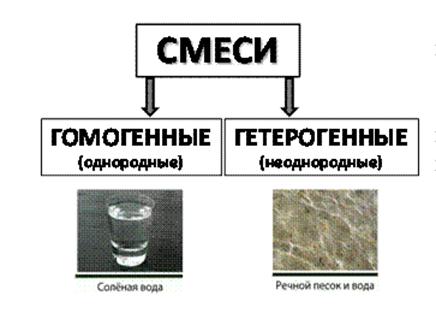
СМЕСИ
Гомогенные (однородные)
(растворы NaCl, сахара в воде, воздух)
Гетерогенные (неоднородные)
(смесь Fe и S, NaCl и сахара, глина с водой, масло с водой)
Формулируем определения:
Неоднородными называются смеси, в которых невооруженным глазом или при помощи микроскопа видны частицы веществ, составляющих смесь.
Однородными называются смеси, в которых нельзя заметить частицы веществ, входящих смесь (даже при помощи микроскопа)
Для закрепления материала на данном этапе ученики работают парами и приводят свои примеры смесей ( однородную и неоднородную)
Сравнение смесей и сложных веществ.
Смесь
Сложное вещество
1. Вещества сохраняют свои свойства.
1. Свойства исходных веществ не сохраняются.
2. Вещества можно разделить физическими методами.
2. Сложное вещество нельзя разделить физическими методами.
3. Количественный состав может быть произвольным.
3. Количественный состав химического соединения всегда одинаков независимо от места нахождения и способа получения.
3. Способы разделения смесей.
Учитель снова обращается к демонстрационному столу и знакомит ребят с основными способами разделения смесей, которые представляет в виде следующей схемы:
Основные способы разделения смесей (очистки веществ)
Неоднородные смеси
Отстаивание и декантация
Отстаивание частиц глины и песка в воде. Применяется для очистки питьевой воды
Фильтрование
Применяется для очистки питьевой воды (бытовые фильтры)
Действие магнитом
(отделение железа от немагнитных веществ)
Однородные смеси
Выпаривание
Выделение NaCl из воды соленых озер
Кристаллизация
Производство сахара
Дистилляция
(перегонка)
Получение дистиллированной воды
4. Демонстрационные опыты.
Учитель проводит лабораторные опыты, демонстрируя основные способы разделения смесей: отстаивание и декантация, фильтрование и выпаривание, действие магнитом.
С такими способами разделения смесей как возгонка, центрифугирование, хроматография учитель знакомит учеников на видеофрагментах (демонстрирует видеоролики на экране с помощью проектора).
5. Закрепление.
Ответы на вопросы по таблице(интеракт.доска)
Учитель обращается к учащимся с дополнительными вопросами:
- Процессы разделения смесей следует относить к физическим или химическим процессам? (к физическим процессам)
- Какие явления подтверждают этот вывод?
6. Подведение итогов урока. Выставление оценок.
Подводя итог урока, учитель обращается к классу с вопросами:
Учащиеся высказываются по желанию.
- Научились ли вы чему-нибудь новому? С какими новыми понятиями мы сегодня познакомились?
- Что вам больше всего понравилось?
-Какие методы разделения смесей мы освоили?
-Где и как нам могут пригодиться полученные сегодня на уроке знания?
7. Домашнее задание:
п. 23 ,ответить на вопросы 1-5


