- Преподавателю
- Химия
- Урок по теме Факторы, влияющие на скорость химической реакции
Урок по теме Факторы, влияющие на скорость химической реакции
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Егорова И.А. |
| Дата | 26.04.2015 |
| Формат | docx |
| Изображения | Есть |


 Тема: Факторы, влияющие на скорость химических реакций.
Тема: Факторы, влияющие на скорость химических реакций.
Цели:
Образовательные:
-
Рассмотреть факторы, которые влияют на скорость химической реакции. Определить их значение в химической промышленности.
-
Научиться решать задачи на формулу Вант-Гоффа и закон действующих масс.
-
Углубить понятие о скорости химической реакции.
Развивающие:
-
Развитие умений выдвигать гипотезы, подтверждать или опровергать их опытными данными, сопоставлять, анализировать, делать выводы.
-
Развитие познавательного интереса к предмету.
-
Развитие навыков работы с лабораторным оборудованием.
-
Развитие навыков самостоятельной работы.
Воспитательные:
-
Формирование научного мировоззрения.
-
Формирование умений научной организации труда.
Оборудование: растворы кислот, цинк, мел, оксид меди, раствор перманганата калия, сульфит натрия, спиртовка, спички, пробирки, держатель.
ХОД ЗАНЯТИЯ
1. Повторение изученного материала. Актуализация знаний.
2. Объяснение нового материала.
Из курса химии вам известно, что реакции протекают с разной скоростью. Некоторые - мгновенно, другие - в течение промежутка времени.
Почему так происходит, что влияет на скорость химических реакций? На данные вопросы мы должны сегодня на уроке ответить.
Студенты записывают тему занятия.
На скорость реакции оказывают влияние различные факторы:
Демонстрационный опыт: В две пробирки наливаем раствор серной
кислоты. В одну добавляем оксид меди, а в
другую раствор марганцовки и сухой
сульфит натрия. В первой пробирке
никаких видимых изменений не
происходит, а во второй произошло
мгновенное обесцвечивание раствора.
1.Природа реагирующих веществ.
Краткий инструктаж по технике безопасности при выполнении лабораторных опытов.
Лабораторный опыт: 1ряд - В две пробирки налить соляную и
уксусную кислоты и в каждую добавить по
грануле цинка. Сравнить, как проходит
взаимодействие металла с кислотами.
2 ряд - В две пробирки налить серную и уксусную
кислоты и в каждую добавить по грануле цинка.
Сравнить, как проходит взаимодействие металла
с кислотами.
Сравним справочные данные для константы диссоциации этих трех кислот. Как видно из таблицы у уксусной кислоты степень диссоциации самая маленькая, т.е. она самая слабая и реакции с ее участием идут очень медленно.
Аналогично кислотам мы можем сравнить активность металлов, используя электрохимический ряд напряжений металлов.
Мы рассмотрели первый фактор, который влияет на скорость реакций. Природу вещества мы поменять не с состоянии и в данном случае можем только подбирать более активные вещества.
С помощью каких факторов мы все - таки можем увеличить или уменьшить скорость реакции?
2. Температура.
Демонстрационный опыт: В две пробирки помещаем оксид меди и в
каждую добавляем раствор серной кислоты.
Одну пробирку нагреваем на спиртовке.
Сравниваем обе пробирки. В каком случае
реакция идет быстрее?
Математическая зависимость скорости реакции от температуры выражается правилом Вант - Гоффа и формулой Вант - Гофф.
Правило Вант - Гоффа: При повышении температуры на каждые 10°С скорость большинства химических реакций увеличивается в 2 - 4 раза.
Т2 - Т1
Формула Вант - Гоффа: 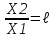 10
10
ɣ - температурный коэффициент скорости реакции
Задачи на формулу Вант - Гоффа:
1. Вычислите, во сколько раз увеличится скорость реакции при повышении температуры от 30°С до 70°С, если температурный коэффициент скорости реакции равен 2.
2. Вычислите, как изменится скорость реакции, если понизить температуру от 120°С до 80°С? Температурный коэффициент скорости равен 3.
3. Концентрация.
Как Вы думаете, температуру можно повышать до бесконечности. Таким образом получается, что с помощью температуры мы можем ускорять далеко не все реакции. Каким образом еще можно повлиять на скорость химической реакции? С помощью концентрации. Из бытовых наблюдений вам хорошо известно, что чем выше концентрация, тем реакция идет быстрее. Убедимся в этом на опыте.
Демонстрационный опыт: В две пробирки помещаем по грануле цинка.
В первую добавляем раствор соляной
кислоты, во вторую - концентрированную
кислоту. Сравниваем обе пробирки.
В каком случае реакция идет быстрее?
Математически зависимость скорости реакции от концентрации выражается законом действующих масс: Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях равных стехиометрическим коэффициентам.
Для реакции: aА + bВ = dD
Ʋ =k× [А]а × [В]b
k - константа скорости химической реакции.
! В выражении здм используются концентрации только жидких и газообразных веществ
Задачи на закон действующих масс:
1. Реакция идет по уравнению N2 + 3H2 = 2NH3. Запишите выражение закона действующих масс и вычислите, как изменится скорость реакции, если концентрации N2 и H2 увеличить в 3 раза.
2. Реакция идет по уравнению CO + Cl2 = COCl2. Запишите выражение закона действующих масс и определите, как изменится скорость химической реакции, если концентрации исходных веществ увеличили в 2 раза.
4. Площадь поверхности раздела реагирующих веществ.
Для гетерогенных реакций важным является такой фактор, как площадь поверхности соприкосновения реагирующих веществ.
Лабораторный опыт: В две пробирки налить соляную кислоту. В одну
добавить кусочек мела, а в другую - порошок
мела. Сравнить, как происходит взаимодействие
мела с кислотой.
Для увеличения площади поверхности твердые вещества измельчают, жидкие и газообразные перемешивают.
5. Катализатор.
Катализатор - вещество, которое ускоряет химическую реакцию, но само при этом не расходуется.
Механизм действия катализатора заключается в следующем:
А + В = АВ - реакция идет медленно
Допустим, что в реакции участвует вещество К - катализатор, тогда:
А + К = АК - быстро
АК + В = АВ + К - быстро
Катализ
Гомогенный Гетерогенный
(Реагирующие вещества и катализатор (Реагирующие вещества и катализатор
находятся в одном агрегатном состоянии) находятся в разных агрегатных
состояниях)
Ингибиторы - отрицательные катализаторы (замедляют)
Ферменты - биологические катализаторы.
Домашнее задание: § 3.1 - 3.3
Приложение
Задачи по теме
«Факторы, влияющие на скорость химических реакций»
-
Температура.
1.1. Вычислите, во сколько раз увеличится скорость реакции при повышении температуры от 30°С до 70°С, если температурный коэффициент скорости реакции равен 2.
1.2. Вычислите, как изменится скорость реакции, если понизить температуру от 120°С до 80°С? Температурный коэффициент скорости реакции равен 3.
2. Концентрация.
2.1. Реакция идет по уравнению N2(г) + 3H2 (г) = 2NH3(г). Запишите выражение закона действующих масс и вычислите, как изменится скорость реакции, если концентрации N2 и H2 увеличить в 3 раза.
2.2. Реакция идет по уравнению CO(г) + Cl2(г) = COCl2(г). Запишите выражение закона действующих масс и определите, как изменится скорость химической реакции, если концентрации исходных веществ увеличили в 2 раза.
Таблица. Константы диссоциации некоторых кислот
Формула кислоты
Константа диссоциации
H2SO4
1×103
HCl
1×107
CH3COOH
1,754×10-5
HBr
1×109
HI
1×1011
HNO3
4,36×10
HNO2
4×10-4
Литература
Основные источники:
1. Белик В.В., Физическая и коллоидная химия: учебник для студ. сред. проф. учеб. заведений. - М.: «Академия», 2012
Дополнительные источники:
1. Лукьянов А.Б. Физическая и коллоидная химия. - М: Высш. шк., 1980. 2. Липатников Е.В. и др. Физическая и коллоидная химия. - М: Высш. шк. 1981.
3. Рыбакова Ю.С. Лабораторные работы по физической и коллоидной химии.- М: Высш. шк. 1968.
4. Романцева Л.М. Сборник задач и упражнений по общей химии: Учеб. пособие для нехим. спец. вузов. - М.: Высш. шк., 1991.
5. Практические работы по физической химии. Под ред. Мищенко К.П., Равделя Л.А. М: Химия. 1967


