- Преподавателю
- Химия
- Конспект открытого урока по теме Кислоты
Конспект открытого урока по теме Кислоты
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Низамиева Г.Ш. |
| Дата | 17.12.2014 |
| Формат | doc |
| Изображения | Есть |
Урок по химии на тему: "Кислоты, их классификация и свойства" в 8 классе с использованием обучающих структур Сингапурского метода обучения
Автор учебника: О.С. Габриелян
Цели: обобщить и углубить знания учащихся о свойствах кислот в свете теории электролитической диссоциации, продолжить совершенствование умения учащихся составлять ионные уравнения реакции.
Задачи:
Образовательные: обобщить и углубить знания учащихся о свойствах кислот, продолжить совершенствовать умения учащихся составлять ионные уравнения реакций;
Развивающие: способствовать развитию умения учащихся проводить эксперимент для получения новых знаний; речевых навыков учащихся. Вести работу над общеучебными умениями: сравнивать, обобщать, делать выводы.
Воспитательные: воспитывать в детях чувства товарищества, умения работать в коллективе, воспитывать интерес у учащихся к урокам химии, соблюдать технику безопасности при работе с кислотами.
Оборудование: спиртовка, газоотводная трубка, пробирки, держатели
Реактивы: соляная кислота, гидроксид натрия, р-р фенолфталеин, серная кислота, хлорид бария, цинк, оксид меди (II).
Методы: беседа, самостоятельная работа по группам, проблемное изложение
Ход урока
I. Организационный момент.
- Здравствуйте, ребята. Каково ваше настроение?
А теперь поприветствуйте друг друга: партнеры по плечу дайте пять друг другу; партнеры по лицу -ударьтесь кулачками и улыбнитесь друг другу.
Итак, начинаем урок.
II.Актуализация знаний и умений.
Сейчас мы с вами проведем СТЁ ЗЕ КЛАСС.
В течение 2 минут вам нужно будет собрать как можно больше формул кислот у своих друзей. Вы встанете с места, найдете пару не из своей команды, встанете рядом с ним и, молча просмотрев записи вашего партнера, скопируете те формулы, которых у вас нет. И таким образом, вы должны встретиться с несколькими партнерами и собрать как можно больше формул кислот.
III. Изучение нового материала.
Учитель:
Сообщаю тему урока, цели, задачи, знакомлю с планом урока (на доске)
Кислоты. Определение
Классификация кислот
Физические и химические свойства.
Учитель: Однако какими бы разными не были кислоты, все они при диссоциации образуют катион водорода.
Задание: написать электролитическую диссоциацию следующих кислот:
Н2 S, Н NО3, Н2SiО3 , что для этого необходимо знать? (растворимость в воде, сильные или слабые электролиты)
Ребята отвечают, что Н2SiО3 не растворяется, поэтому диссоциацию не пишут.
2 ученика пишут на доске электролитическую диссоциацию Н2 S, Н NО3.
Учитель: Как определить, что при диссоциации образуется катион водорода? (действием индикатора)
Назовите окраску лакмуса, фенолфталеина, метилоранжа в кислотной среде (ответы учащихся доказываю демонстрационным опытом)
А сейчас повернитесь и дайте «пять» партнеру по плечу. И в течение 30 секунд предлагайте свои варианты друг другу.(проводим РЕЛЛИ РОБИН - два участника предлагают свои варианты, говорят по очереди). Начинает тот, у кого светлее волосы.
Учитель: Вспомните физические свойства Н2SО4 при демонстрации (бесцветная жидкость, вязкая, не имеющая запаха, гигроскопична, обугливает древесину, кожу, ткани)
- Химические свойства
На доске прикрепляю карточки (зачитываю химические свойства)
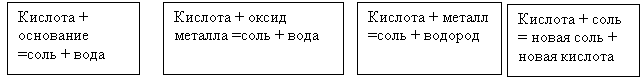
Учитель: вспомнить слова М. Фарадея: "Ни одна наука не нуждается в эксперименте в такой степени как химия. Ее основные законы, теории и выводы опираются на факты, поэтому постоянный контроль опытом необходим". Поэтому опытным путем докажем химические свойства кислот, соблюдая технику безопасности.
Физкультминутка. Упражнения для глаз..
Вращательные движения глазами: сначала в левый нижний угол, потом на межбровье, потом в правый нижний угол, потом на кончик носа.. Повторить несколько раз..
Задание: провести лабораторный опыт (на столе у учащихся лежат карточки разноцветные:
Инструкция "Меры безопасности при работе с кислотами", инструкция проведения опыта), работают по парам, учащиеся разделены на 4 группы. Перед выполнением лабораторного опыта, учащиеся читают инструкцию № 2 (см. Приложение 1).
Первая группа выполняет лабораторный опыт "Взаимодействие кислот с щелочами (основаниями)" Первая группа работает на жёлтых листах. Жёлтый цвет ассоциируется с солнцем и интуицией, стимулирует нервную систему, укрепляет печень и сердце, повышает аппетит.
Лабораторный опыт "Взаимодействие кислот с щелочами (основаниями)"
Порядок выполнения работы:
В пробирку налейте 2 мл раствора гидроксида натрия и прибавьте 1-2 капли фенолфталеина. Что вы наблюдаете?
К раствору щелочи с фенолфталеином приливайте по каплям соляную кислоту, периодически взбалтывая содержимое пробирки. Что вы наблюдаете?
Составьте молекулярное и ионные уравнения проделанной реакции.
Вторая группа - лабораторный опыт " Взаимодействие кислот с солями".
Вторая группа работает на синих листах: синий цвет ассоциируется со спокойствием и умом, снимает раздражительность, понижает высокую температуру при болезни.
Лабораторный опыт "Взаимодействие кислот с солями"
Порядок выполнения работы:
В пробирку налейте 2 мл серной кислоты и прибавьте несколько капель хлорида бария. Что вы наблюдаете?
Напишите молекулярное и ионные уравнения проделанной реакции
Третья группа - лабораторный опыт "Взаимодействие кислот с металлами".
Третья группа работает на красных листах: красный цвет помогает бороться со стрессом, выводят яды и возвращает жизненную силу.
Лабораторный опыт "Взаимодействие кислот с металлами"
Порядок выполнения работы:
В пробирку положите 2 гранулы цинка и прилейте соляную кислоту, закройте пробирку пробкой. Подождите некоторое время, чтобы она заполнилась водородом, затем откройте пробку и поднесите зажженную спичку к отверстию.
Что вы наблюдаете?
Напишите молекулярное уравнение проделанной реакции.
Четвертая группа - лабораторный опыт "Взаимодействие кислот с основными оксидами".
Четвёртая группа работает на фиолетовых листах: регулирует артериальное давление, повышает интеллектуальную способность..
Лабораторный опыт "Взаимодействие кислот с основными оксидами"
Порядок выполнения работы:
1. В пробирку насыпьте немного оксида меди (СиО) и прилейте раствор серной кислоты. Подогрейте смесь. Что вы наблюдаете?
2. Напишите молекулярное уравнение проделанной реакции.
После выполнения работы 4 учащихся от каждой группы выходят к доске и пишут уравнения реакции под соответствующими карточками. В это время 4 других учащихся представляют отчет о проделанной работе.
Затем сообщаю учащимся, что на следующий урок продолжим изучать химические свойства кислот: взаимодействие кислот с металлами, взаимодействие кислот с солями
Затем зачитываю применение кислот в быту. Уксусная и лимонная кислота применяется для удаления пятен от ржавчины на хлопчатобумажных, льняных и шерстяных белых тканях. 1 чайная ложка на 1 стакан воды, подогреть до кипения и ткань с пятном несколько раз окунуть в раствор или пятно протереть раствором, а затем кислоту тщательно смыть водой, лучше с добавлением несколько капель нашатырного спирта - для нейтрализации кислоты.
IV. Закрепление
Задание: составьте возможные уравнения реакций взаимодействия перечисленных веществ с раствором серной кислоты. Из букв, соответствующих правильным ответам, вы составите название одного из элементов четвертого периода таблицы Д.И. Менделеева.
1) SiО2 А
2) LiОН К
3) Ва (NО3 )2 А
4) НСI С
5) К2О Л
6) К2 SiО3 И
7) Н NО3 О
8) Fе(ОН)3 Й
V. Домашнее задание: параграф 38, выучить таблицу,
На оценку
"3" - упр 1,2
"4" - упр 1,2,4
"5" - упр 1,2, 4,5
VI. Итоги урока.
Оценки за урок.
Резюме: самостоятельно сделайте вывод, достигли ли вы учебной цели, было ли интересно вам на уроке или совсем неинтересно?


