- Преподавателю
- Химия
- Конспект урока по теме «Типы химических реакций»
Конспект урока по теме «Типы химических реакций»
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Кунакасова Г.Г. |
| Дата | 27.12.2014 |
| Формат | doc |
| Изображения | Есть |
Конспект урока по теме «Типы химических реакций»
Тип урока: урок обобщения и систематизации знаний по теме.
Форма урока: комбинированный урок с использованием ИКТ.
Оборудование: учебник О.С. Габриеляна- 8 класс, малый химический тренажёр, интерактивная доска, мультимедиапроектор, презентация, реактивы и химическая посуда (растворы сульфата меди (II), гидроксида натрия, соляная (хлороводородная) кислота, цинк, бихромат аммония, 3 пробирки, штатив, спички, спиртовка, защитные очки, лучинка.)
Цели урока:
-
Закрепить понятие «химическая реакция», повторить признаки и условия протекания различных химических реакций.
-
Обобщить знания о классификации химических реакций по составу и количеству исходных веществ и продуктов реакции.
-
Продолжить формирование умения записывать уравнения химических реакций и определять их тип по составу и количеству исходных веществ и продуктов реакции.
Задачи
-
· Обучающие: - систематизировать знания учащихся о классификации веществ, типах химических реакций, продолжить формирование умений наблюдать, записывать уравнения и предвидеть продукты химических реакций, продолжить формирование умения при написании реакций обмена.
-
· Развивающие:- совершенствовать умения школьников при составлении химических уравнений, при выполнении лабораторных опытов; совершенствовать умения учащихся сравнивать и обобщать; развивать память, устойчивое внимание, самостоятельное мышление, умение слушать и слышать другого человека; развивать аналитическое мышление.
-
· Воспитательные:- продолжить формирование диалектико-материалистического мышления учащихся, умение наблюдать, формулировать выводы и обобщать информацию.
Ход урока
I. Все, что нас окружает, состоит из веществ. Кажется, что они живут своей жизнью, таинственной и непостижимой. Взаимодействуя, они изменяют свои свойства и состав. Без химических реакций невозможна жизнь и все многообразие веществ. И задача человека, изучив этот мир, постараться использовать полученные знания во благо.
Сегодня на уроке мы должны систематизировать все полученные вами знания о химических реакциях, для того, чтобы в дальнейшем вы могли правильно описывать химические свойства веществ, а также предсказывать возможности их получения. Хорошо овладев этой темой, вы сможете решать всевозможные химические задачи. Слайд 1,2
Слайд 3:
Вспомните, какие явления мы называем химическими реакциями?
Учащиеся: Химические реакции - это явления, сопровождающиеся образованием новых веществ?
По каким признакам можно определить, что у вещества изменились свойства?
Учащиеся: Появление запаха, выделение газа, выпадение или растворение осадка, изменение цвета, выделение или поглощение тепла и света.
Слайд 4:
Проверим?
Слайд 5:
Реакции протекают повсюду: они происходят в окружающем нас воздухе, листьях растений, в организме человека. Например, в печени человека происходит 20 миллионов различных реакций.
Слайд 6:
Как с помощью химического языка описать происходящие явления?
Учащиеся: С помощью химического уравнения.
Химическое уравнение - это условная запись химической реакции с помощью химических формул и математических знаков.
Слайд 7:
Повторим правила составления химического уравнения.
Учащиеся: Уравнения химических реакций составляют на основании Закона сохранения массы веществ. Число атомов химических элементов до реакции и после неё, остаётся неизменным, а значит, их общая масса тоже не изменяется.
Огромное множество реакций необходимо классифицировать. Зачем?
Учащиеся: Это необходимо сделать, чтобы не запутаться во всём многообразии химических реакций.
Мы классифицировали реакции на 4 группы.
Слайд 8:
Какие типы реакций вы знаете?
Учащиеся: Соединения, разложения, обмена, замещения.
Слайд 9:
Итак, По изменению числа исходных веществ и конечных продуктов реакции делят на
-
Реакции соединения.
-
Реакции разложения.
-
Реакции замещения.
-
Реакции обмена.
Слайд 10:
Рассмотрим примеры реакций соединения.
Какие вещества взаимодействуют между собой?
Какие вещества образуются?
Что общего в этих реакциях?
Какие реакции относятся к данному типу?
Учащиеся:…
Слайд 11
Вывод: Реакции между двумя или несколькими простыми или сложными веществами, в результате которых образуется только одно сложное вещество, называют реакциями соединения.
Слайд 12:
Рассмотрим примеры реакций разложения.
Что общего в этих реакциях?
Какие реакции относятся к данному типу?
Учащиеся:…
Слайд 13
Вывод: Реакции, в результате которых из одного сложного вещества получается несколько простых или сложных веществ, называют реакциями разложения.
Слайд 14:
Рассмотрим примеры реакций замещения.
Назовите исходные вещества и продукты реакций, определите их состав.
Выделите общие признаки этих реакций.
Какие реакции относятся к данному типу?
Учащиеся:…
Слайд 15
Вывод: Реакции замещения -это реакции, в результате которых атомы простого вещества замещают атомы какого-нибудь элемента в сложном веществе
Слайд 16:
Рассмотрим примеры реакций обмена. Какие реакции относятся к данному типу?
Учащиеся:…
Слайд 17
Вывод: Реакции обмена - это реакции, при которых два сложных вещества обмениваются своими составными частями.
II. Работа с дидактическими материалами (см. приложение).
Учащиеся выполняют задания по вариантам.
Найдите такие реакции в своём варианте карты, объясните свой выбор:
1 вариант реакции соединения
2 вариант реакции разложения
3 вариант реакции замещения
4 вариант реакции обмена.
Проверяем выполнение задания.
Слайд 18,19.
А теперь отдохнём.
Выполним гимнастику для глаз.
Внимательно следим глазами за движениями шайбы по экрану.
Слайд 20
А теперь закрепление.
Расставьте коэффициенты в следующих уравнениях реакций. Определите типы реакций, объясните свой выбор.
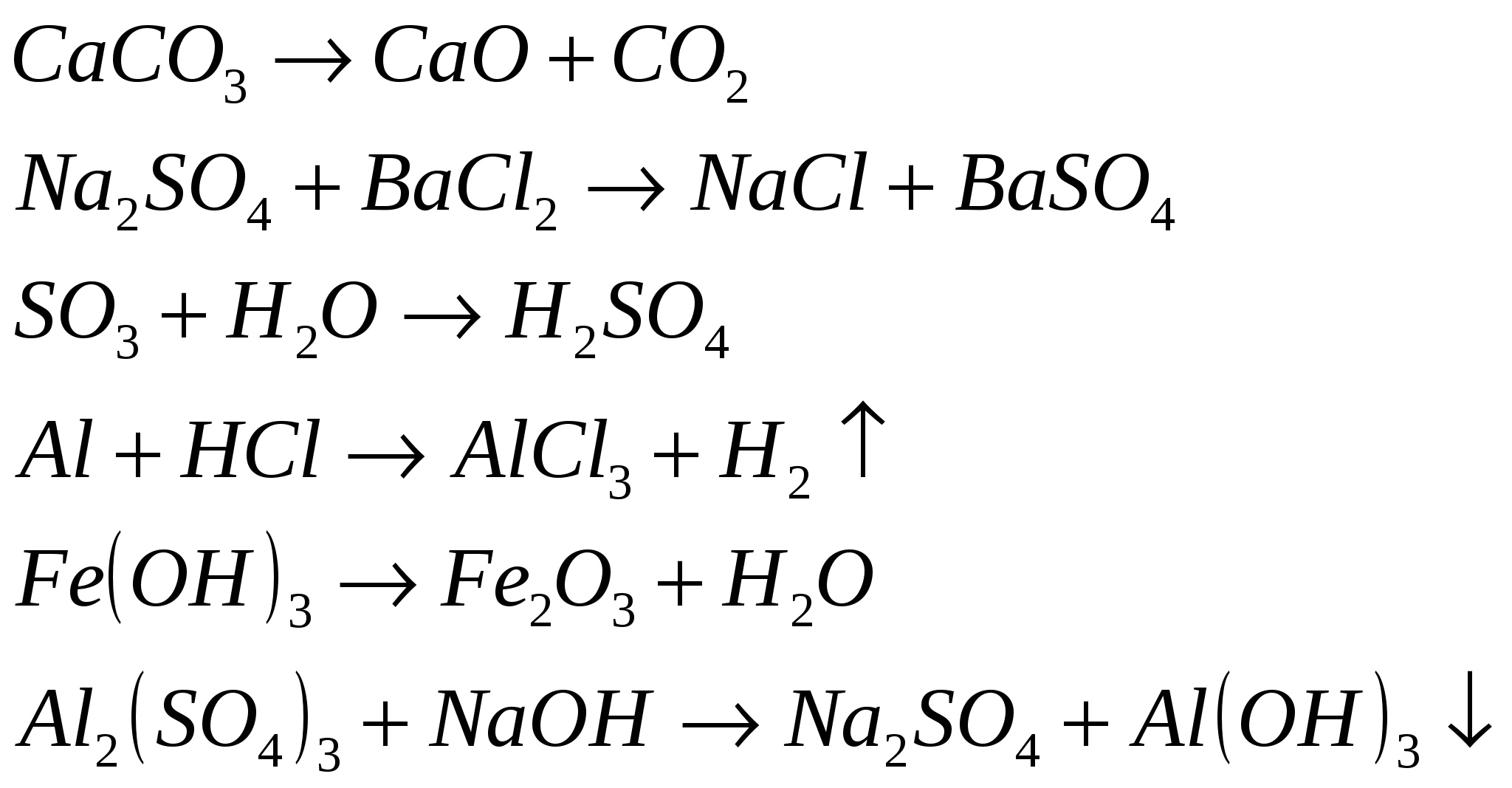
Слайд 21
Усложним задание.
Напишите уравнения реакций по названиям исходных веществ и продуктов реакций. Определите типы реакций.
а) Оксид натрия + оксид азота (V) → нитрат натрия
б) Железо + соляная кислота → хлорид железа (II) + водород
в) Хлорид калия + нитрат серебра → нитрат калия + хлорид серебра
г) Железо + сера → сульфид железа (II)
д) Сульфат магния + гидроксид натрия → гидроксид магния + сульфат натрия
Итак, сегодня мы вспомнили всё, что знаем о химических реакциях. Использовали наши знания при выполнении заданий. Это поможет нам при изучении следующей темы. А теперь запишите домашнее задание:
Слайд 23
-
Упражнение №3, стр. 145
Вам необходимо расставить коэффициенты в химических реакциях и определить их тип, то есть ещё раз повторить то, что мы делали на уроке.
Для любителей решать задачи. Дополнительное задание:
-
Упражнение №7, стр. 128
Вспомните, как решается задача с использованием понятия «массовая доля»
Слайд 24. Урок окончен, спасибо за внимание.
Приложения
карточка - тренажер
Уравнения химических реакций
1 вариант
2 вариант
3 вариант
4 вариант
1
t
2MgO+O2=2MgO
Fe+ CuCl2= Cu+ FeCl2
t
2Cu+ O2 = 2CuO
2Na + 2H2O = 2NaOH + H2↑
2
2K + 2H2O = 2KOH + H2↑
t
4P + 5O2 = 2 P2O5
Fe2O3 + 6HCl = 2FeCl3 + + 3H2O
Zn + Pb(NO3)2 =Pb + Zn(NO3)2
3
Fe + H2sO4 = FeSO4 +H2↑
Mg +2HCl= MgCl2 + H2↑
Ba + H2O = Ba(OH)2 +H2↑
Zn+ H2SO4 = ZnSO4 + H2↑
4
Zn+ Cu(NO3)2= Zn(NO3)2 + Cu
Al2O3+ 6HCl =2AlCl3+ 3H2O
H2O + SO2 ↔ H2SO3
2H2 + O2 = 2H2O
5
CaO +H2O = Ca(OH)2
P2O5+ 3H2O = 2H3PO4
CuCl2 +2KOH =2Cu(OH)2 ↓+ 2KCl
t
Cu(OH)2 = CuO+ H2O
6
3CaO + 2H3PO4=
Ca3(PO4)2 +3H2O
Ba(OH)2 +2HNO3=
Ba(NO3)2 +2H2O
2HNO3+ Ca(OH)2=
Ca(NO3)2 +2H2O
CaCO3+ 2HCl=CaCl2 + H2СO3
⁄\
H2O CO2↑
7
2NaOH + H2SO4=
Na2SO4+ 2H2O
Ca +2H2O =Ca(OH)2 + H2↑
AgNO3 + NaBr = NaNO3 + AgBr↓
HBr + NaOH= NaBr + H2O
8
BaCl2+Na2SO4=BaSO4↓+2NaCl
AgNO3+ KCl = KNO3+ AgCl↓
Cu +Hg(NO3)2= Cu(NO3)2 + Hg
AgNO3+ KI = KNO3 + AgI↓
9
CO2 +H2O ↔ H2CO3
t
2Fe(OH)3= Fe2O3 +3H2O
Mg + 2HCl = MgCl2 + H2↑
Na2O + H2O = 2NaOH


