- Преподавателю
- Химия
- Расчет давления пара по закону Рауля. Вычисление осмотичных давлений растворов
Расчет давления пара по закону Рауля. Вычисление осмотичных давлений растворов
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Матюгина И.И. |
| Дата | 19.10.2014 |
| Формат | docx |
| Изображения | Есть |
Расчет давления пара по закону Рауля. Вычисление осмотичных давлений растворов»
Цель работы: Научиться производить расчеты давлений насыщенного пара растворов по закону Рауля и осмотичных давлений растворов.
Теоретическая часть:
Для всех жидких растворов характерным свойством является понижение давления насыщено пара компонентов по сравнению с давлением насыщенного пара чистых веществ. Количественная связь между концентрацией летучего вещества в идеальном растворе и давлением его пара под раствором выражается законом Рауля.
При постоянной температуре давления насыщенного пара компонента идеального раствора пропорционально его малой доли в растворе.
Pi = Pi0 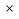 ϗi
ϗi
Pi- нарушают давление летучего компонента над раствором.
Pi0- давление насыщенного пара чистого компонента.
ϗi - мольная доля компонента.
Когда растворяется вещество, то закон Рауля имеет вид: 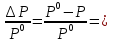 ϗi
ϗi
P0- давление пара растворится над чистым растворителем.
P- давление пара растворителя под чистым раствором.
ϗ- мольная доля растворённого вещества.
Ход работы:
Задание 1. Сколько граммов олова (Sn) надо растворить в 100 г ртути(Hg), чтобы давление пара ртути снизилась от 94637 до 93275 Па.
Задача 2. При температуре 25  упругость пара воды равна 19,64 мм. рт. ст. На сколько понизится давления пара, если в 400 г. H2O растворить 1 г C6H12O6.
упругость пара воды равна 19,64 мм. рт. ст. На сколько понизится давления пара, если в 400 г. H2O растворить 1 г C6H12O6.
Задача 3. Чему равно осматичное давление раствора содержащего 0,1 М сахара в 100 мл. Н2О.


