- Преподавателю
- Химия
- Модульный урок по теме Водород с использованием алгоэвристической программы
Модульный урок по теме Водород с использованием алгоэвристической программы
| Раздел | Химия |
| Класс | 8 класс |
| Тип | Конспекты |
| Автор | Шаль О.В. |
| Дата | 03.01.2016 |
| Формат | doc |
| Изображения | Есть |
Технологическая карта урока.
Тема: Водород в природе.
Водород как химический элемент и простое вещество.
Применение водорода.
№ учебного элемента
Учебный материал с указанием заданий
Рекомендации по выполнению заданий, оценка
М - 0
Интегрирующая цель: Познакомить учащихся
-
с распространением водорода в природе (на Земле и во Вселенной):
-
с положением элемента в Периодической Таблице Д.И.Менделеева;
-
со строением атома элемента водорода;
-
с водородом - как простым веществом, его физическими свойствами и применением
Должны продолжить развивать умения:
-
давать характеристику водороду, как химическому элементу;
-
строить схемы строения атома водорода;
-
наблюдать и выявлять физические свойства водорода - простого вещества;
-
самостоятельно работать с учебной литературой;
-
анализировать, сравнивать;
-
отвечать на вопросы, слушать;
-
наблюдать и делать выводы;
м - 1
История открытия водорода.
Странным на первый взгляд делом занялся однажды английский учёный Кавендиш: он стал пускать мыльные пузыри. Но это было не развлечение. Перед этим Кавендиш заметил, что, когда железные опилки обливают серной кислотой, появляется много пузырьков какого-то газа. Что это за газ? Учёный вывел его по трубочкам из сосуда. Газ был невидим. Имеет ли он запах? Нет. Тогда Кавендиш наполнил им мыльные пузыри, и они легко поднялись вверх! А если поджечь газ? Он загорался голубоватым пламенем, но что удивительно - при горении получалась вода! Кавендиш назвал новый газ горючим воздухом. Ведь он, как и обычный воздух, был без цвета и запаха. Всё это происходило во второй половине XVIII-го века.
Учитель проводит опыт получения водорода и получение мыльных пузырей.
А позже французский химик Лавуазье сделал обратное: получил «горючий газ» из воды. Он же дал новому газу и другое имя - гидрогениум, т.е. водород или «рождающий воду».
- О каком элементе, рождающем воду, идет речь?
Внимательно слушайте учителя
Наблюдайте за опытом
Внимательно слушайте учителя
Предложите свое мнение.
М-2
Цель: дать общую характеристику водорода.
2.1 Пользуясь таблицей Д.И. Менделеева дайте общую характеристику водорода по плану:
Химический знак -
Порядковый номер -
Относительная атомная масса Ar (Н) =
Химическая формула -
Относительная молекулярная масса Mr (Н) =
Молярная масса -
Валентность - .
Ответ запишите в тетрадь.
М-3
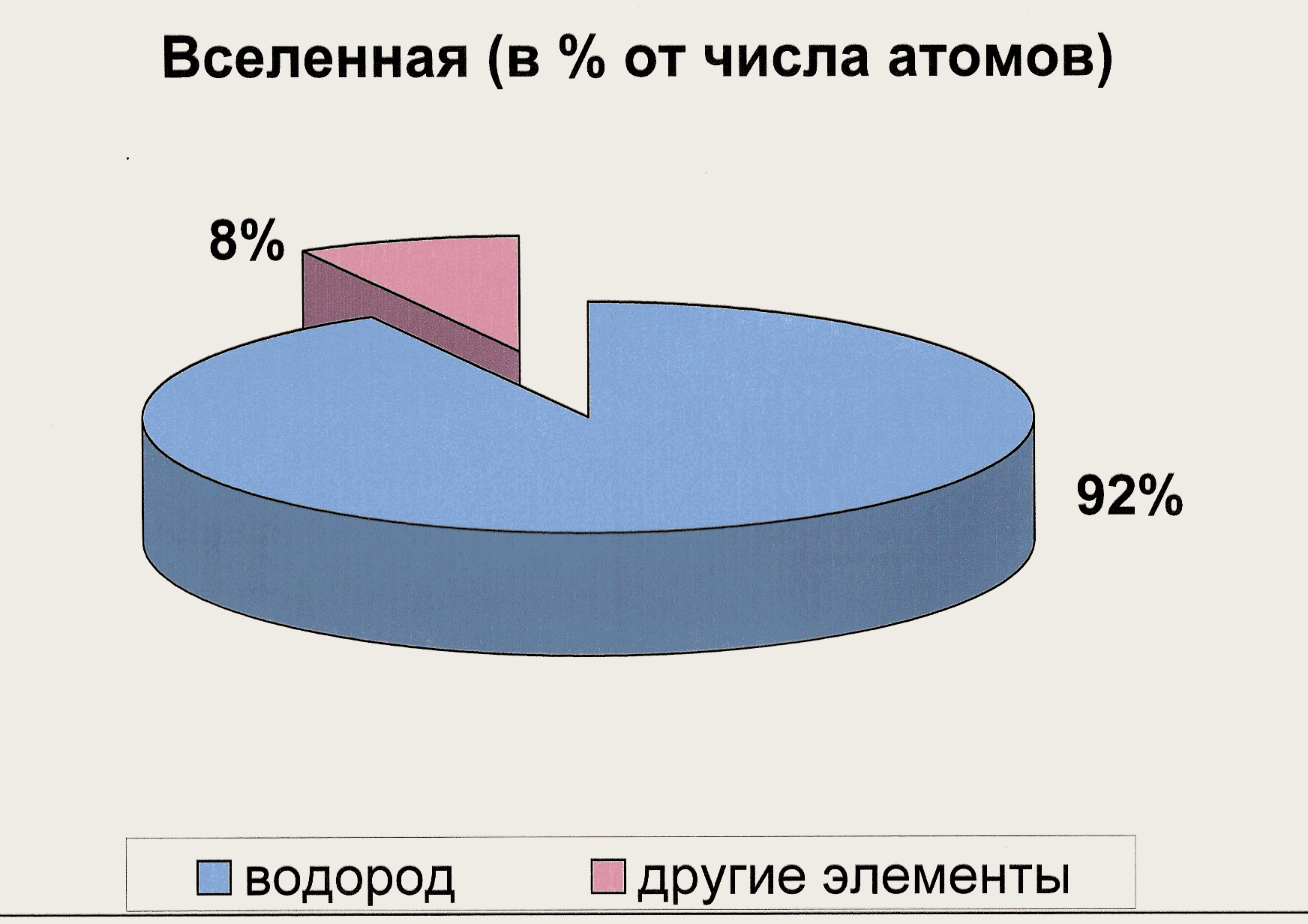
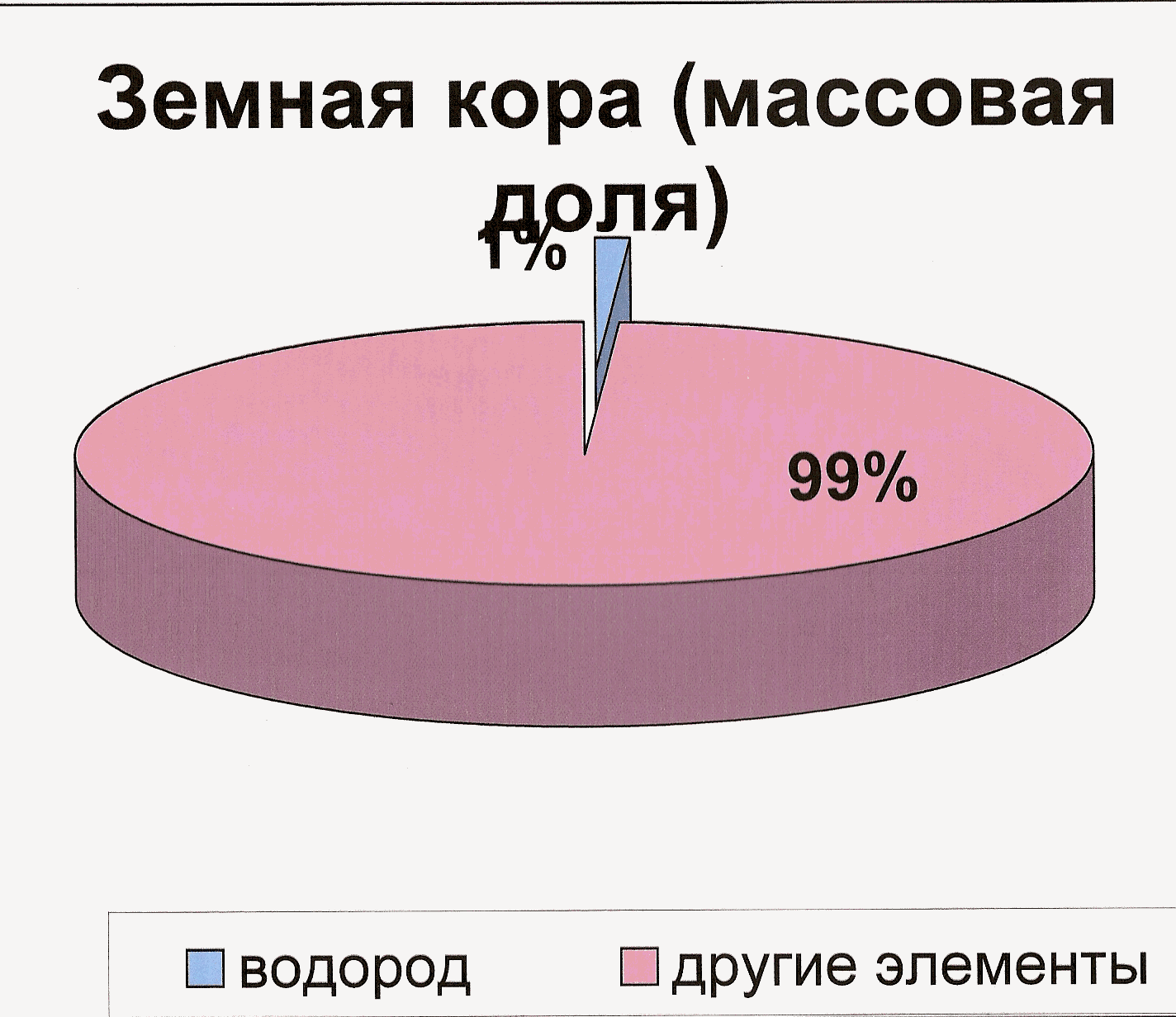
Распространение водорода в природе.
Цель: Ознакомиться с нахождением водорода в природе.
Охарактеризуйте данные диаграммы.
а) Какой процент на долю водорода приходится в Земной коре?
б) Какой процент на долю водорода приходится во Вселенной?
в) Какой можно сделать вывод о распространенности водорода?
г) В каких веществах на Земле можно встретить водород?
Заполнить схему. Нахождение водорода в природе
Работайте с диаграммами
Используйте уже полученные знания.
М-4
Физические свойства водорода. Способы получения.
Цель: Ознакомиться с физическими свойствами водорода, выяснить, какими способами получают водород в промышленности и в лаборатории.
4.1 Ознакомьтесь с текстом. Назовите фамилию ученого открывшего водород и год открытия. Подчеркните в тексте физические свойства водорода.
Впервые этот газ в чистом виде выделил 240 лет назад английский химик Генри Кавендиш. Свойства полученного им газа были настолько удивительны, что ученый принял его за легендарный «флогистон», «теплород» - вещество, по канонам науки того времени определявшее температуру тел. Он прекрасно горел (а огонь считался почти чистым флогистоном), был необычайно легок, в 15 раз легче воздуха, малорастворим в воде, без цвета, без запаха, хорошо впитывался металлами и так далее. Однако другой великий химик, француз Антуан-Лоран Лавуазье, уже в 1787 году доказал, что полученное Кавендишем вещество - вполне обычный, хотя и очень интересный химический элемент. Свое название он получил оттого, что при горении давал не дым, сажу и копоть, а воду. Кстати, именно эта его особенность больше всего привлекает сегодняшних экологов и «зеленых».
-
Исходя их физических свойств водорода, укажите каким способом собирают водород. Почему? Ответ запишите в тетрадь.
4.3. Заполнить схему, записать уравнения реакций, расставить коэффициенты.
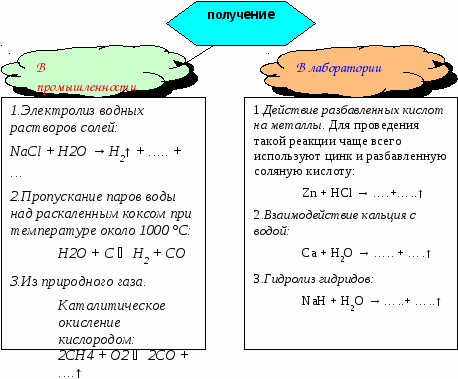
М-5
Химические свойства водорода.
Цель: Изучить химические свойства водорода.
С галогенами образует галогеноводороды:
F2 + H2 →…(протекает со взрывом в темноте
и при любой температуре)
Cl2 + H2 →…(реакция протекает со взрывом,
только на свету)
Взаимодействие с оксидами металлов
Оксиды взаимодействуя с водородом
образуют свободный металл металлов
CuO + H2 → …
Fe2O3 + 3H2 → …
М - 6
Применение водорода.
Цель: Изучить области применения водорода.
5.1. Прочитайте текст и ответьте на поставленный вопрос?
Химическая промышленность
При производстве аммиака, метанола, мыла и пластмасс
Пищевая промышленность
При производстве маргарина из жидких растительных масел.
Топливо
Водород используют в качестве ракетного топлива. Ведутся исследования по применению водорода как топлива для легковых и грузовых автомобилей. Водородные двигатели не загрязняют окружающую среду и выделяют только водяной пар.В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую
В каких областях промышленности применяется водород?
Прочитайте текст
Подумайте и ответьте
Прочитайте и запомните!
М -7
Проверка полученных знаний. Закончите предложение, вставляя нужное слово.
1. Водород - самый распространенный элемент во ............................................... .
2. Важнейшее соединение водорода - ............. .
3. Знак водорода - ......... , атомная масса - ......... , валентность в соединениях - ........ .
4. В Периодической таблице стоит под номером ……. .
5. Молекула водорода состоит из ....... атомов.
6. При обычных условиях водород - это ............... без ... ……….., ... ………, (тяжелее или легче) воздуха (подчеркните), растворим в воде. Водород имеет низкую температуру кипения. Только у гелия температура кипения ниже, чем у водорода.
7. При собирании водорода пробирку держат ............ дном, потому что водород ............. воздуха.
Каждый правиль-ный ответ оцени-вается в 1 балл.
М-8
Домашнее задание.
Стр. 66 упражнение 3, 6, 11.


