- Преподавателю
- Химия
- Урок Химиялық элементтердің электртерістілігі
Урок Химиялық элементтердің электртерістілігі
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Садвакасова Ш.Т. |
| Дата | 30.11.2015 |
| Формат | docx |
| Изображения | Есть |
| тақырыбы | Химиялық элементтердің электтерістілігі | ||
| сілтеме | Ә.Темірболатова, Н.Нұрахметов, Р.Жұмаділова, С.Әлімжанова Алматы «Мектеп» 2012ж, әдістемелік оқулықтар, презентациялар, есептер жинағы | ||
| Жалпы мақсаты: | Оқушы бойында электртерістілік туралы түсінік қалыптастыру | ||
| Күтілетін нәтиже | 1.Электрнтерістілік не екенін біледі; 2.Күрделі заттардағы химиялық элементтердің электртерістілігн салыстыра алады; 3.Атом құрылысы туралы түсініктері одан әрі дамиды; 4.Оқушылардың сөйлеу, есте сақтау, өздігімен жұмыс жасау сияқты дағдылары одан әрі қалыптасады; 4.Өткен материал бойынша қорытынды жасау, оқулықпен жұмыс жасау дағдылары дамиды; | ||
| Түйінді идея | Электртерістілік туралы жалпы білім қалыптастыра отырып, химиялық элементтердің электртерістілігінің периодтағы және топтағы өзгерістерін түсіндіре алады. | ||
| Сабақтың түрі | Жаңа білімді меңгеру | ||
| Сабақтың көрнекілігі | Компьютер, интерактивті тақта, сабақ презентациясы, Д.И.Менделеевтің периодтық кестесі, Полинг суреті. | ||
| Ақпараттық қолдау | Презентация «Химиялық элементтердің электртерістілігі» | ||
| Сабақ барысы | І.Ұйымдастыру кезеңі Оқушылармен амандасу, түгендеу, 3 топқа бөлу. Протон, нейтрон, электрон (2 мин) | ||
| ІІ.Өткен тақырыпқа шолу жасайық: Тапсырмалар: 10 мин
| 1.Тест 1)Натрий атомының электрондық формуласы: а)1s2 2s2 2p6 3s2 3p6 4s2 б)1s2 2s2 2p2 в)1s2 2s2 2p63s1 г)1s2 2s2 2)ІІІ топ негізгі топша элементтерінің ең жоғарғы оксидтерінің жалпы формуласы: а)R2O б)RO в)RO2 г)R2O3 3) Мына қосылыстардағы күкірттің валенттігі: CаS; SO3; SO2. а) I , II, III. б) II, IV, VI. в) II, VI , IV. Г) III, IV, V. 4)Периодтық жүйедегі элементтің реттік нөмірі: а) ядродағы протон санына тең; б)атом массасына тең в) ядродағы нейтрон санына тең; г)атом массасыөскен сайын артады 5.Магний атомындағы электрон саны: а) +12 б) +24 в) +3 г) +2 6.Металдық қасиеті басым элемент: а) Na б) Li в) К г) Сs 7 Реттік нөмір өскен сайын негізгі топша атомдарының атом радиусы: а)кемиді б)өзгермейді в)өседі г)периодты өзгереді 8. Химиялық элементтер қатарында В -- С-N: а)атом ядросының заряды кемиді б)атом радиусы өседі в)сыртқы деңгейдегі электрон саны бірдей болады г) бейметалдық қасиет артады 9)Периодтық кестенің негізгі топшаларында атом ядросының заряды өсуімен атом радиусы: а) өседі б) кемиді в)өзгермейді г) периодты өзгереді 10 Атомының үшінші электронды деңгейінде екі электроны болатын, элемент - бұл: а) Мg б) Si в) B г) Ве Бір-бірін тексеру: Жауаптары: (1в, 2г, 3в, 4а, 5а, 6г, 7в, 8г, 9а, 10 а.). 2. Топтарға тапсырма: 1 топ тапсырмасы: Терминдермен жұмыс. Сәйкестендір: 1.Топ | 1.Химиялық элементтер мен олар түзетін жай және күрделі заттардың қасиеттері олардың атомдық массалырының шамасына периодты түрде тәуелді болады. | |
| 2.Екідайлы зат | 2.Атом ядросынының зарядына тең болады | ||
| 3.Негізгі топша | 3.Химиялық элементтердің тік қатары | ||
| 4.Реттік нөмір | 4.Сілтілік металмен басталып, инертті элементпен аяқталатын химиялық элементтердің көлденең қатары | ||
| 5.Қосымша топша | 5.Оксидтері мен гидроксидтері әрі қышқылмен, әрі сілтімен әрекеттесе алады. | ||
| 6.Период | 6.Кіші және үлкен периодтардың элементтері кіретін қатар | ||
| 7.Периодтық заң анықтамасы | 7.Тек қана үлкен период элементтері кіретін қатар | ||
Бір-бірін тексеру: 1-3, 2-5, 3-6, 4-2, 5-7, 6-4, 7-1.
2 топ тапсырмасы:
1)Мына элементтердің атом құрамын анықтап, электрондық формулаларын құрыңдар:
А) күкірт Б) фтор
2)Мына элементтерді атом радиусының өсуі бойынша орналастырыңдар:
О, 2) Те, 3) Se, 4) S----------------------------------------------------------------------
C, 2) Bе, 3) B, 4)Li ______________________________________________
Al, 2) Cl, 3) P, 4) S ______________________________________________
3)Мына элементтердің жоғарғы оксидінің формуласын құрастырыңдар:
А) хлор б) кремний
3 топ тапсырмасы:
Қандай түсінік туралы айтылып тұр:
1).Ядросындағы протон саны бірдей, бірақ массалары әртүрлі бөлшектер, бұл - ...............................
2)Ядро заряды бірдей атом түрі, бұл - ..........................................................
3)Химиялық бөлінбейтін ең ұсақ бөлшек - ................................
4)Атомның центрінде орналасады - оң зарядталған ...........................
5)Атом ядросы тұрады : ..................................... және ...................................
6.Ядро айналасында тұйық орбиталар бойынша теріс зарядталған.......................... қозғалады .
7.Атомның планетарлық моделін ұсынған .....................................................
ІІІ.Жаңа тақырыпты меңгеру
10 мин
Химиялық элементтердің электртерістілігі (ЭТ)
Сабақта не меңгеру керекпіз:
--- «Электртерістілік», «салыстырмалы электрістілік» ұғымдарының анықтамасын білу керек;
-- Химиялық элементтердің ЭТ-нің периодта және топтағы өзгерісіне сараптама жасай білу керек;
--Әртүрлі химиялық элементтердің ЭТ-н салыстыра білу керек;
--Бинарлы қосылыстардағы электрондардың ығысуын анықтай білу керек;
Оқулықпен жұмыс: Оқулықтың 121 бетіндегі §40 мәтінмен танысыңдар, мына сұрақтарға жауап іздеңдер:
*** Периодтық жүйеде элементтердің қасиеттері периодта және топта қалай өзгереді? Элементтердің металдық қасиеттерінің артуы мен әлсіреуі қалай жүреді?
Периодта, солдан оңға қарай элементтердің металдық қасиеттері кемиді.
Топта, жоғарыдан төмен қарай металдық қасиет артады.
***Мәтінге сүйене отырып, элементтердің металдарға немесе бейметалдарға жататынын қалай анықтауға болатыны туралы қорытынды жасаңдар.
Элементтердің металдарға немесе бейметалдарға жататынын, олардың атомдарының электрондарды беру немесе қосып алу қабілеті бойынша анықтайды.
**** Сонда ЭТ дегеніміз - .......
ЭТ туралы түсінікті американдық химик Полинг енгізді.
Элементтің электронды тарту қабілетін сипаттау үшін салыстырмалы ЭТ пайдаланылады, өйткені абсолютті ЭТ-тің сан мәні қолдануға өте қолайсыз.
Салыстырмалы ЭТ-тің мәнін ЭТ-гі 1-ге тең литиймен салыстыра отырып шығарады.
Сонымен неғұрлым ЭТ жоғары болса, соғұрлым элементтің электронды өзіне тарту қабілеті жоғары болады.
140 беттегі №19 кестемен жұмыс. Мына сұрақтарға жауап беріңдер:
ЭТ ең жоғары элемент, ЭТ ең төмен элемент?
ЭТ ең жоғары фтор, ЭТ ең төмен цезий
Периодта ЭТ қалай өзгереді?
Периодта, солдан оңға қарай ЭТ өседі
Негізгі топшаларда ЭТ қалай өзгереді?
Негізгі топшада, жоғарыдан төмен қарай ЭТ кемиді.
ЭТ-пен атом радиусы арасында қандай байланыс бар?
Периодта, солдан оңға қарай - радиус кемиді, ЭТ артады, электрондар ядроға күшті тартылады. Топта, жоғарыдан төмен қарай - радиус артады, ЭТ кемиді, электрондардың ядромен байланысы әлсірейді.
Қорытынды:Неғұрлым элементтің бейметалдық қасиеті басым болса, соғұрлым оның ЭТ жоғары болады, неғұрлым элементтің металдық қасиеті басым болса, соғұрлым оның ЭТ төмен болады.
ІҮ. Бекіту:
15 мин
1 тапсырма:
19 кестені пайдалана отырып, команда жина:
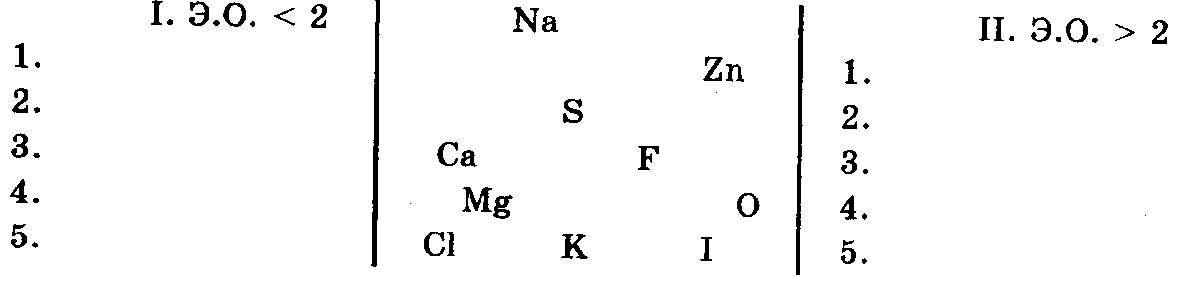
Екі команданың құрамына сараптама жасаңдар:
Жауабы:
І. ЭО< 2 II ЭО>2
1. Na 1. S
2. Zn 2. F
3. Ca 3. O
4. Mg 4. Cl
5.K 5. I
1-ші команда - металдар
2-ші команда - бейметалдар
2тапсырма: Келтірілген формулалардағы ЭТ жоғары элементтің астын сызыңдар:
СаСІ2, К2О, N2, H2S, AI2O3
Жауабы: СаСL2, К2O, N2, H2S, Al2O3.
3 тапсырма: Мына қосылыстарда электрондар қай элементке ығысатынын көрсетіңдер:
NH3; HCl; P2O5; CH4.
Жауабы: NH3; HCl; P2O5; CH4.
4.тапсырма: Атом ядросының заряды белгілі мына элементтердің жұбындағы бір элементтің ЭТ-нің жоғары болу себебін түсіндіріңдер:
а) +6 және +8…………….
б) +12 және +20…………
5.Сөйлемдерді толықтырыңдар:
1.ЭТ мәнін біле отырып, элементтің ............. немесе ................ екенін білуге болады.
2.Металдардың ЭТ әдетте ---------------, ал бейметалдардың ЭТ ....................,.
3.Элементтердің ЭТ периодта ......................,,,,,,,,,,,,,........... өседі, ал негізгі топшаларда ............................................................................................................
4.Химиялық реакция кезінде ЭТ ............................ элемент атомдарынан электрондар ЭТ .............................. элемент атомдарына ..............................
Ү.Сабақты қорытындылау
3 мин
Бағалау:
Бағалау парақшасы:
Оқушының аты-жөні_____________________________________
Тест
Терминмен жұмыс
Бекіту тапсырмасы
Жалпы ұпай
саны
Тест - 10 ұпай
Терминдермен жұмыс - 7 ұпай.
Бекіту тапсырмалары - 1-5. Ұпай
Барлығы - 22 ұпай
Бағалау критерийлері:
20-22 ұпай- "5"
16-19 ұпай- "4"
11-15 ұпай - "3"
10 ұпайдан төмен - "2"
ҮІ Рефлексия
Оқушылар сабақтың алған әсерін бір сөйлеммен жеткізеді:
Бүгін мен білдім ----------------------
Қызықты болды ---------------------
Қиын болды -------------------------
Мен тапсырмаларды орындадым -------------
Мен мынаны түсіндім ---------------------------
Енді мен ---------------------------------------------
Мен мынаны сездім ------------------------------
Мен үйрендім ---------------------------------------
Мен мынаны жасағым келеді ----------------
ҮІІ.Үйге тапсырма:
Параграф 40 оқу,
1. Жұптардағы элементтердің ЭТ-н салыстырыңдар:
бром және хлор, оттек және көміртек , натрий және магний, магний және литий.
2. Кестеге қарамай, элементтердің периодтық жүйедегі орнына сүйене отырып, мына элементтерді олардың ЭТ-нің өсу реті бойынша орналастырыңдар::
а) S, Cl, Br ………………………
б) C, Si, N ……………………………
3. Мына белгілердің көмегімен > , < қай элементтің ЭТ жоғары екенін көрсетіңдер:
H Cl S O Na Cl Cu O
O F Mg Al
Жауабы:
H < Cl S < O Na < Cl Cu< O
O < F Mg< Al


