- Преподавателю
- Химия
- Конспект урока Свойства спиртов
Конспект урока Свойства спиртов
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Арсеньева Е.Н. |
| Дата | 19.10.2014 |
| Формат | doc |
| Изображения | Есть |
МКОУ «Новогуровская средняя общеобразовательная школа»
Тема урока:
«Свойства предельных одноатомных спиртов. Физиологическое действие спиртов на организм человека»
10 класс
Урок подготовила и провела:
учитель химии
Арсеньева Е.Н.
ТЕМА УРОКА: «Свойства предельных одноатомных спиртов. Физиологическое действие спиртов на организм человека».
Цели: - Исходя из строения молекул спиртов, подвести учащихся к выводу о возможных химических свойствах предельных одноатомных спиртов. - Познакомить учащихся с химическими свойствами предельных одноатомных спиртов. - Закрепить и углубить знания учащихся о физиологическом действии спиртов на организм человека. - Продолжить знакомить учащихся с возможностями ИКТ на уроках химии.
Оборудование: учебно-электронные пособия «Химия (8-11 классы). Виртуальная лаборатория», «Химия для всех - XXI», «Органическая химия», «Репетитор по химии Кирилла и Мефодия», компьютер, проектор, экран;
Ход урока:
I.Организационный момент. Сообщаю учащимся тему, цели и задачи урока.
Сегодня мы продолжаем изучать предельные одноатомные спирты. И поможет нам в этом компьютер. Вы познакомитесь с химическими свойствами спиртов, а также рассмотрим какое физиологическое действие могут оказывать одни из них на организм человека.
Но сначала вспомним, какие органические вещества относятся данному классу соединений, каково строение их молекул, изомерия, номенклатура.
II. Проверка домашнего задания. Индивидуальный опрос:
- Рассказать о строении молекул предельных одноатомных спиртов, используя учебно-электронное
пособие «Химия (8-11).Виртуальная лаборатория» (1уч-ся).
- Решение задачи на нахождение химической формулы спирта. (1 уч-ся у доски).
Фронтальный опрос класса.
- Какие органические вещества называются спиртами?
- Какова общая формула спиртов?
- Что означает название - одноатомный спирт?
- Что означает название - предельный спирт?
- Какие виды изомерии характерны для предельных одноатомных спиртов? Приведите примеры.
Ответы уч-ся у доски.
1 уч-ся. Задача. При анализе вещества нашли, что в его состав входят углерод, водород и кислород, массовые доли, которых равны соответственно 0,52, 0,13 и 0,35. Найдите молекулярную формулу и назовите это вещество, если известно, что плотность его паров по воздуху равна 1,586.
Решение.
x : y : z = 0,52/12 : 0,13/1 : 0,35/16 = 0,04 : 0,13 : 0,02 = 2 : 6 : 1, C2H6O - простейшая формула вещества.
Mr(С2H6O) = 46, Mr( CxHyOz) = 1,586 * 29 = 46, C2H5OH.
Ответ: C2H5OH - этанол.
Дополнительный вопрос : - Всегда ли простейшая формула является формулой вещества?
- Как определить истинную формулу?
2 уч-ся. Рассказ о строении предельных одноатомных спиртов с использованием ИКТ на примере метанола и этанола.
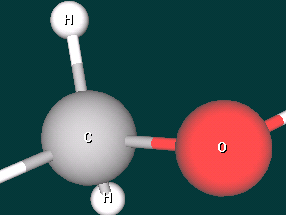
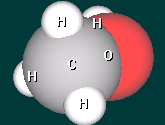
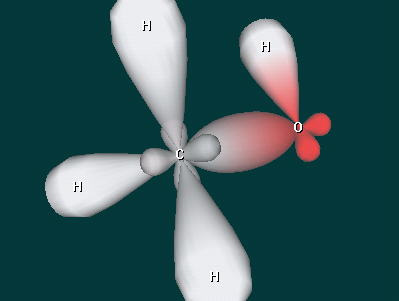
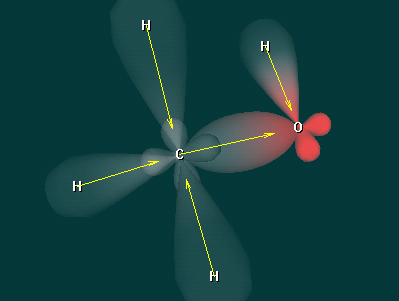
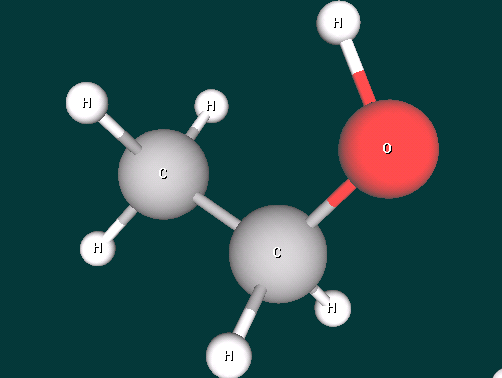
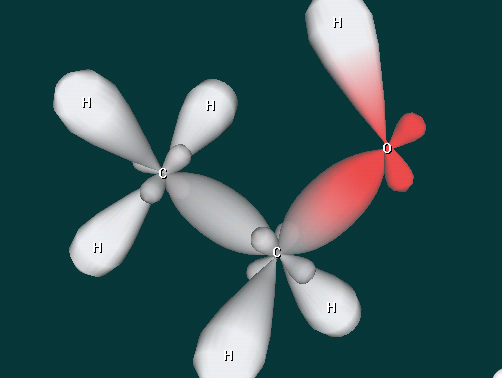
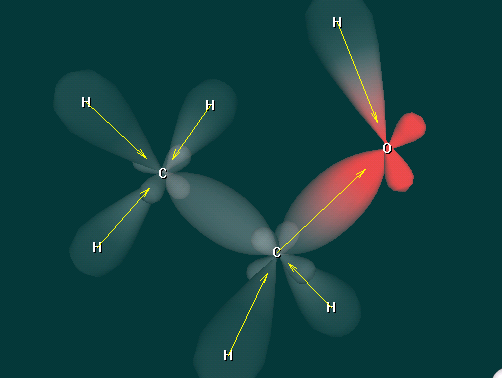
Дополнительный вопрос : - Какой вид химической связи в молекулах спиртов?
- Какие могут быть заместители атомов водорода в углеводородном
радикале спиртов?
III. Объяснение нового материала.
Учитель: - Итак, мы с вами выяснили, что в молекулах спиртов ковалентные полярные связи: C H - слабо полярная, C O и H O - сильно полярные. Вследствие чего, говорят о «кислотном атоме водорода в гидроксильной группе.
Для предельных одноатомных спиртов характерны два типа химических реакций.
Рассмотрение химических свойств, предполагает химический эксперимент. Некоторые опыты по химии с взрывчатыми, дурно-пахнущими, горючими, ядовитыми веществами, хотя изучение химических свойств многих из них входит в школьную программу, я не могу вам продемонстрировать на уроке, в силу опасности для вашего здоровья, за ними желательно наблюдать с экрана. Афрагменты компьютерного сопровождения подобного эксперимента дадут вам знания о веществах и явлениях, сопровождающих данные превращения.
I группа свойств - реакции, идущие по углеводородному радикалу. (Учащиеся самостоятельно у доски и в тетрадях составляют уравнения химических реакций) 1) галогенирование CH3-OH + Cl2 CH2Cl-OH + HCl
2) нитрование CH3-OH + HO-NO2 CH2NO2-OH + H2O
II группа свойств - реакции, идущие по гидроксильной группе. 1) водные растворы спиртов не изменяют окраски индикаторов. 2) взаимодействие с активными металлами - щелочными и щелочноземельными (см. электрохимический ряд напряжений металлов). ! Опыт сначала демонстрируется на экране (ИКТ), а затем составляется уравнение химической реакции: 2CH3-OH + 2Na 2CH3-ONa + H2
Соли спиртов имееют общее название - алкоголята. CH3-ONa называется метилат натрия. Эти соли неустойчивые и в воде легко гидролизуются: CH3-ONa + HOH CH3-OH + NaOH
3) гидрогалогенирование в кислой среде (конц.H2SO4) с образованием галогенопроизводных углеводородов. CH3-OH + HCl CH3Cl + H2O
4) реакции дегидротации а) внутримолекулярная (t>140C, конц.H2SO4) CH3-OH H2C=CH2 + H2O
б) межмолекулярная CH3-CH2-OH + HO-CH2-CH3 CH3-CH2-O-CH2-CH3 + H2O
5 ) реакции окисления: а) окислителями - CuO, KMnO4, K2Cr2O7 O
) реакции окисления: а) окислителями - CuO, KMnO4, K2Cr2O7 O
 CH3-CH2-OH + CuO CH3-C + H2O + Cu
CH3-CH2-OH + CuO CH3-C + H2O + Cu
H
б) реакция горения (Учащиеся самостоятельно у доски и в тетрадях составляют уравнения химических реакций) - 2CH3-OH + 3CO2 2CO2 + 4H2O + Q
Q - имеет очень большое значение и спирты могут применятся как горючее, например в спиртовках.
! Опыты сначала демонстрируются.
IV. Закрепление. Фронтальный опрос класса.
- Почему для спиртов характерны реакции двух типов?
- Назовите заместители атомов водорода в углеводородном радикале.
- С какими веществами у спиртов идут реакции по гидроксильной группе?
- К какому типу можно отнести реакции спиртов с Na, HCl, в избытке спирта, с
растворами KMnO4, K2Cr2O7?
А теперь давайте рассмотрим как действует метанол и этанол на живые организмы. Послушаем подготовленный на эту тему доклад.
V. Домашнее задание: §20 - повторить, §21, вопросы 8, 9, 12, 13 на стр. 88 (устно).
Выставление оценок за урок в электронный журнал.


