- Преподавателю
- Химия
- Таблица Качественные реакции на катионы и анионы
Таблица Качественные реакции на катионы и анионы
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Пригоровская Г.В. |
| Дата | 02.01.2016 |
| Формат | doc |
| Изображения | Есть |
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА КАТИОНЫ
Катион
Воздействие или реактив
Признаки
Li+
Пламя
Карминово-красное окрашивание
Na+
Пламя
Желтое окрашивание
К+
Пламя
Фиолетовое окрашивание
Са2+
Пламя
Кирпично-красное окрашивание
Sr2+
Пламя
Карминово-красное окрашивание
Ва2+
S042-
Выпадение белого осадка, не растворимого в кислотах: Ва2+ + S042- BaS04
BaS04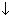
Пламя
Желто-зеленое окрашивание
Сu2+
Вода
Гидратированные ионы Сu2+ имеют голубую окраску
ОН -
Осадок голубого цвета Сu2+ +2ОН- → Сu(OH)2↓
РЬ2+
S2-
Выпадение черного осадка: Pb2+ + S2- ![]() PbS
PbS 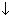
Аg+
Cl-
Выпадение белого осадка; не растворимого в HNO3, но растворимого в конц.
NH3 • Н20:
Аg+ +Cl- AgCl
AgCl 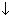
Fe2+
гексацианоферрат (III) калия (красная кровяная соль) K3[Fe(CN)6]
Выпадение синего осадка:
К++ Fe2+ + [Fe(CN)6]3- KFe[Fe(CN)6]4
KFe[Fe(CN)6]4
3Fe2+ +2 [Fe(CN)6]3- Fe3[Fe(CN)6]2
Fe3[Fe(CN)6]2
ОН -
Объемный хлопьевидный осадок белого(светло-зеленого) цвета, буреющий на воздухе в результате окисления Fe2+ +2ОН- → Fe(OH)2↓
Fe3+
гексацианоферрат (II) калия (желтая
кровяная соль)
K4[Fe(CN)6]
Выпадение синего осадка:
К+ + Fe3+ + [Fe(CN)6]4- ![]() KFe[Fe(CN)6]
KFe[Fe(CN)6]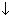
4Fe3+ + 3[Fe(CN)6]4- ![]() Fe4[Fe(CN)6]3
Fe4[Fe(CN)6]3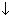
роданид-ион
NCS-
Появление ярко-красного окрашивания Fe3+ +3NCS- =Fe(NCS)3
ОН -
Объемный хлопьевидный осадок бурого цвета Fe3+ +3ОН- → Fe(OH)3↓
Al3+
щелочь (амфотерные свойства гидроксида)
Выпадение объемного осадка белого цвета, растворяющийся в избытке щелочи и растворах кислот Al3+ +3ОН- → Al(OH)3↓
Zn2+
ОН -
Выпадение объемного осадка белого цвета, растворяющийся в избытке щелочи и растворах кислот Zn2+ +2ОН- → Zn(OH)2↓
NH4+
щелочь, нагревание
Запах аммиака: NH4+ + ОН- NH3
NH3 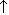 + Н20
+ Н20
Н+
(кислая среда)
Индикаторы: лакмус, метиловый оранжевый
красное окрашивание
красное окрашивание
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА АНИОНЫ
Анион
Реактив
Признаки
S042-
Ва2+ (растворимые соли бария)
Выпадение белого осадка, нерастворимого в кислотах:
Ва2+ + S042- BaS04
BaS04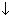
N03-
конц. H2SO4 и Си
Образование голубого раствора, содержащего ионы Сu2+, выделение газа бурого цвета (NO2)
Cu + 4HNO3 Cu(NO3)2 + 2NO2 + 2Н20
Cu(NO3)2 + 2NO2 + 2Н20
РО43-
ионы Ag+
Выпадение светло-желтого осадка в нейтральной среде: ЗАg+ + Р043- Аg3Р04
Аg3Р04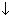
СrO42-
ионы Ва2+
Выпадение желтого осадка, не растворимого в уксусной кислоте, но растворимого в HCI: Ва2+ + СrO42- BaCr04
BaCr04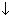
S2-
ионы РЬ2+
Выпадение черного осадка: Pb2+ + S2- PbS
PbS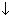
Н+ (растворы кислот)
Выделение газа с запахом тухлых яиц 2H+ + S2- → H2S
СО32-
ионы Н+
Выделение газа 2Н+ + СO32- Н20 + С02↑
Н20 + С02↑
ионы Са2+
выпадение белого осадка, растворимого в
кислотах: Са2+ + С032- = СаСОз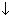
SO32-
ионы Н+
Появление характерного запаха S02: 2Н+ + SO32- Н20 + S02↑
Н20 + S02↑
SiO32-
ионы Н+
Выпадение студенистого осадка 2Н+ + SiO32- H2SiO3↓
H2SiO3↓
F-
ионы Са2+
Выпадение-белого осадка: Са2+ + 2F- CaF2
CaF2
Cl-
ионы Аg+
Выпадение белого осадка, не растворимого в HN03, но растворимого в конц. NH3 • Н20: Аg+ +CI- AgCl
AgCl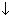
AgCI + 2(NH3• Н20)  [Ag(NH3)2]+ + CI- + 2Н2О
[Ag(NH3)2]+ + CI- + 2Н2О
Br-
ионы Аg+
Выпадение светло-желтого осадка, не растворимого в HN03: Ag+ + Br-= AgBr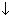 осадок темнеет на свету
осадок темнеет на свету
I-
ионы Аg+
Выпадение желтого осадка, не растворимого в HNO3 и NH3 конц.: Аg+ + I-  АgI
АgI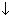 осадок темнеет на свету
осадок темнеет на свету
ОН-
(щелочная среда)
индикаторы: лакмус
фенолфталеин
синее окрашивание,
малиновое окрашивание
ОПРЕДЕЛЕНИЕ НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Вещество
Реагент
Признаки протекания реакции
CO2 газ без цвета и запаха, не ядовит, растворим в воде
известковая вода Са(ОН)2
Са(ОН)2 + С02  СаСО3
СаСО3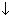 + Н20, СаСО3 + С02 + Н20
+ Н20, СаСО3 + С02 + Н20 ![]() Са(НС03)2 Выпадение белого осадка и его растворение при пропускании изб. С02
Са(НС03)2 Выпадение белого осадка и его растворение при пропускании изб. С02
баритовая вода Ba(OH)2
Bа(ОН)2 + С02  BаСО3
BаСО3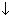 + Н20, BаСО3 + С02 + Н20
+ Н20, BаСО3 + С02 + Н20 ![]() Bа(НС03)2 Выпадение белого осадка и его растворение при пропускании изб. С02
Bа(НС03)2 Выпадение белого осадка и его растворение при пропускании изб. С02
SO2 газ без цвета, с резким запахом, ядовит, растворим в воде
известковая вода Са(ОН)2
Са(ОН)2 + S02  СаSО3
СаSО3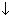 + Н20, СаSО3 + S02 + Н20
+ Н20, СаSО3 + S02 + Н20 ![]() Са(НS03)2 Выпадение белого осадка и его растворение при пропускании изб. S02
Са(НS03)2 Выпадение белого осадка и его растворение при пропускании изб. S02
баритовая вода Ba(OH)2
Bа(ОН)2 + S02  BаSО3
BаSО3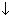 + Н20, BаSО3 + S02 + Н20
+ Н20, BаSО3 + S02 + Н20 ![]() Bа(НS03)2 Выпадение белого осадка и его растворение при пропускании изб. S02
Bа(НS03)2 Выпадение белого осадка и его растворение при пропускании изб. S02
H2S газ без цвета, с запахом тухлых яиц, ядовит, растворим в воде
Растворимые соли Pb2+, Cu2+, Ag+
Образуются осадки черного цвета, нерастворимые в растворах кислот, которые растворяются при нагревании в конц. HNO3 Pb2++ H2S = PbS +2H+
Cu2++ H2S = CuS +2H+
2Ag++ H2S = Ag2S +2H+
NH3 газ без цвета, с резким запахом, очень хорошо растворим в воде, ядовит
Н20, индикаторы
Раствор аммиака ( аммиачная вода, нашатырный спирт) окрашивает индикаторы: лакмус - в синий цвет, метилоранж - в желтый, фенолфталеин - в малиновый.
HCl (газ)
Образуется белый дым
NH3 + HCl = NH4Cl
O2 газ без цвета и запаха, мало растворим в воде
Тлеющая лучинка
Тлеющая лучинка загорается
C+ O2 = CO2


