- Преподавателю
- Химия
- Решение задач по теме «Электролиз»
Решение задач по теме «Электролиз»
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Васильева Г.А. |
| Дата | 11.02.2014 |
| Формат | docx |
| Изображения | Есть |
Решение задач по теме «Электролиз»
-
Какая масса металла выделится на катоде при электролизе с инертными электродами расплава иодида кальция, если на аноде выделилось 570 г иода?
-
Электролизу подвергли 200г 18% водного раствора хлорида меди. После выделения на инертном аноде 2л газа(н.у.) процесс был прекращен. Какова массовая доля вещества в оставшемся растворе?
-
В водный раствор сульфата меди поместили медные пластинки массой по 10г , и подключили к ним источник постоянного тока. Через некоторое время пластинку, служившую анодом, растворили в азотной кислоте, добавили к полученному раствору избыток гидроксида натрия и получили 2,45г осадка. Чему равна масса второй пластинки?
-
в 100 мл воды растворили 2,56 грамм сульфата меди, раствор подвергли электролизу. электролиз прекратили, когда концентрация кислоты стала 5%. вычислить объём водорода.
-
.При электролизе 10 л раствора серной кислоты с
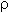 = 1,3 г/cм3 и молярной концентрацией 5 моль/л на катоде выделилось 560 л газа. Определить массовую долю вещества, находящегося в растворе после электролиза.
= 1,3 г/cм3 и молярной концентрацией 5 моль/л на катоде выделилось 560 л газа. Определить массовую долю вещества, находящегося в растворе после электролиза.
-
.При электролизе водного раствора нитрата серебра (I) на аноде выделилось 13,44л кислорода (н.у.). Определите массу выделившегося на катоде серебра, если выход серебра составил 90% от теоретически возможного, а выход кислорода - количественный.
-
.При электролизе водного раствора хлорида цинка на катоде выделился цинк массой 68,25г, а на аноде - хлор объемом 28,22л (н.у.). Определите выход цинка, если выход хлора составил 90% от теоретически возможного.
-
.Определите массу медного купороса, помещенного в электролизёр, если при электролизе его водного раствора выделился кислород объемом 5,71 (н.у.), выход которого ставил 85% от теоретически возможного.
-
Через электролизер, содержащий раствор гидроксида калия объемом 300мл с массовой долей вещества 22,4% (плотность 1,2 г/мл), пропустили электрический ток. Рассчитайте массовую долю гидроксида калия в растворе после отключения тока, если известно, что на катоде выделился газ объемом 89,6л (н.у.)
-
Электролиз 400мл. 6%-ного раствора сульфата меди (II) (плотность 1,02г/мл) продолжали до тех пор, пока масса раствора не уменьшилась на 10г. Определите массовые доли соединений в оставшемся растворе и массы продуктов, выделившихся на инертных электродах.
-
При электролизе раствора хлорида металла катион которого двухзаряден, на катоде выделилось 0,16г металла. При растворении этой массы металла в концентрированной азотной кислоте выделился бурый газ объемом 0,112 (н.у.) Определите состав хлорида и его массу в растворе.
-
1000г 5,1% - ного раствора нитрата серебра подвергнуто электролизу, при этом на катоде выделилось 10,8г вещества. Затем в электролизер добавили 500г 13,5% вещества. Затем в электролизер добавили 500г 13,5% -ного раствора хлорида меди (II). Полученный раствор снова подвергли электролизу до выделения на аноде 8,96л газа (н.у.). Определите массовые доли веществ в конечном растворе.


