- Преподавателю
- Химия
- Разработка урока по теме. «Белки»
Разработка урока по теме. «Белки»
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Гребенюк Т.Н. |
| Дата | 14.02.2014 |
| Формат | doc |
| Изображения | Есть |
Тема : Белки
Цель: актуализировать знания учащихся о белках; изучить более подробно классификацию, химические свойства белков, их биологическое значение и применение.
Задачи: закрепить знания об аминокислотах, продолжить формировать умение учащихся работать с различными источниками информации, работать с реактивами и лабораторным оборудованием;
Оборудование: р-р куриного белка, куриные перья, р-ры: гидроксида натрия, сульфата меди, нитрата свинца; концентрированная азотная кислота, спиртовка, спички, держатель, пробирки, таблица "Белки",транспарант "Классификация белков".
Тип урока: комбинированный
I. Введение: 1. Организационный момент;
2. Постановка познавательных задач. Сообщение темы и цели урока.
Сегодня мы продолжаем изучение органических азотсодержащих соединений. Мы уже знакомы с аминами, аминокислотами. На этом уроке нам предстоит знакомство с природными полимерами, азотсодержащими соединениями - белками. Мы познакомимся с их строением, классификацией, свойствами, биологической ролью в жизни человека, их применением.
3. Актуализация знаний.
Один ученик у доски готовит вопрос: «Химические свойства аминокислот».
В молекулах аминокислот содержатся карбоксильные группы, имеющие
кислотные свойства, и аминогруппы, обладающие основными свойствами.
Они и обуславливают характерные химические свойства этих веществ.
1. Аминокислоты реагируют как с основаниями, так и с кислотами, т.е. они являются амфотерными соединениями:
H2N - CH2 - COOH + NaOH = H2N - CH2 - COONa + H2O
HOOC - CH2 - NH2 + HCI = HOOC - CH2 - NH3 CI
2. Аминокислоты реагируют со спиртами, образуя сложные эфиры:
H2N - CH2 - COOH + HOR = H2N - CH2 - COO-R + H2O
3. Аминокислоты реагируют друг с другом:
Важнейшее свойство аминокислот - их способность вступать в реакцию поликонденсации друг с другом.
Реакция поликонденсации - процессы образования полимеров, которые сопровождаются выделением побочного низкомолекулярного продукта (H2O)
NH2 - CH2 - COOH + H2N - CH2 - COOH = H2O + H2N - CH2 - CO - NH -CH2 -COOH
Связь - СO - NH - образующаяся между остатком NH - аминогруппы одной молекулы аминокислоты и остатком - СО - карбоксильной группы другой молекулы аминокислоты - пептидная связь. Полимер - полипептид. Имеет большое биологическое значение, она лежит в основе биосинтеза белков, а так же важнейшее народнохозяйственное значение. 4.С остальными учащимися проводится беседа по домашнему заданию.
Контрольные вопросы:
-
Какие соединения называются аминами?
-
Каково агрегатное состояние метил амина и анилина? Растворимость в воде?
-
Изменяют ли водные растворы простейших аминов окраску индикаторов? Почему?
-
Чем обусловлены основные свойства аминов? В чем они проявляются?
-
Какие соединения называют аминокислотами? Какие функциональные группы содержатся в их молекулах?
-
Почему аминокислоты называют амфотерными соединениями?
-
Что такое незаменимые аминокислоты?
-
Где используются аминокислоты?
5.Химический диктант.
1.Амины - органические основания
2.Аминокислоты содержат аминогруппу и карбоксильную группу
3.NH2-аминогруппа
4.Анилин - ароматический амин
5.Аминокислоты могут взаимодействовать друг с другом
6.Аммиак более сильное основание, чем метиламин
7.Анилин и фениламин - два разных вещества
8.Амины подвержены горению
9.Аминокислоты содержат аминогруппу при первом атоме углерода
10.Из аминокислот построены белки
Ответы:
№
1
2
3
4
5
6
7
8
9
10
ответ
да
да
да
да
да
нет
нет
да
нет
да
Самопроверка данной работы осуществляется каждым учащимся самостоятельно с последующим выставлением оценок. Подняли руки у кого «5», «4», «3», «2»?
II. Объявление темы и цели урока. ( слайд-2) Мотивация учебной деятельности.
Сегодня мы продолжаем изучение органических азотсодержащих соединений. Мы уже знакомы с аминами, аминокислотами. На этом уроке нам предстоит знакомство с природными полимерами - белками. Мы познакомимся с их строением, классификацией, свойствами, биологической ролью в жизни человека, их применением.
Первый белок, с которыми мы знакомимся в своей жизни - это белок куриного яйца,
1. Работа с текстом учебника- прочитать текст параграфа, подготовить ответы на вопросы (вопросы на слайде):
- что называют белками, белковыми молекулами (записать в тетрадь)?
- каково местонахождение белков?
- каковы строение и структуры белков?
- по каким признакам можно составить классификацию белков (записать одну из возможных в тетрадь, к обсуждению этого вопроса приготовить пример классификации белков по выполняемым функциям)?
- какие свойства характерны для белков?
- каковы качественные реакции на белки?
2. Обсуждение ответов на вопросы.
«Характеристика трех структур белковых молекул».
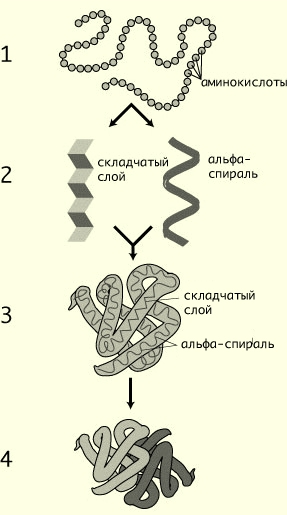 1 - первичная, 2 - вторичная, 3 - третичная, 4 - четвертичная
1 - первичная, 2 - вторичная, 3 - третичная, 4 - четвертичная
5 Физические свойства белков.
Учитель демонстрирует растворимость в воде яичного белка и нерастворимость волос, ногтей.
Химические свойства белков.
Учитель: Вспомните, к каким продуктам в быту мы применяем термин «свернуться»?
Ученики: молоко при длительном стоянии в теплом месте, яичный белок при варке.
Учитель: перед Вами набор химических реактивов.
Выполняем задание №1.Подожгите несколько шерстяных нитей. Охарактеризуйте запах горящей шерсти. (Содержание серы в белках. Запах жженого рога).
Выполняем задания №2. 1).Нагреть пробирку с сырым яичным белком. (Свертывание белка при нагревании - денатурация).
2).Берем пробирку под №3 (молоко) по каплям наливаем уксусную кислоту.
Записываем результаты опытов.
Ученики по-очереди комментируют проведенные опыты. Делаем вывод:
При нагревании, обработки кислотами белок свертывается, то есть происходит необратимый процесс - денатурация (изменения структуры белка под влиянием внешних факторов).
Учитель. Существуют химические реакции, служащие для распознавания белков. Это цветные реакции.
Учитель демонстрирует качественные реакции на белки.
Ксантопротеиновая реакция.
В пробирку налейте два - три мл. раствора белка и несколько капель .НNO3. Нагреть. Желтый осадок. Охлаждаем пробирку + аммиак до щелочной реакции. Изменения окраски на оранжевую (наличие бензольных колец в молекуле белка).
Биуретовая реакция.
В пробирку налить два - три мл. раствора белка и два - три мл. раствора гидроксида натрия, затем 1 - 2 мл. раствора медного купороса. Появляется фиолетовое окрашивание.
Осаждение белка солями тяжелых металлов.
В две пробирки налейте по 1 - 2 мл. раствора белка и медленно, при встряхивании, по каплям добавьте в одну пробирку насыщенный раствор медного купороса, а в другую - раствор ацетата свинца. Образовались труднорастворимые солеобразные соединения белка (применение белка как противоядия при отравлениях солями тяжелых металлов).
6. Обобщение .
Задания для проверки знаний
Задание Вставьте пропущенные слова.
-
Главным носителем жизни являются … .
-
… - это сложные высокомолекулярные соединения, построенные из … .
-
Элементный состав белков: … .
-
Молекулярная масса белков изменяется от … до … .
-
Многие белки растворимы в …, почти все растворяются в … .
-
Нерастворимы белки, из которых построены … .
-
В структуре белка различают … структуры.
-
Функции белков в организме … .
Ответы:
1. Белки.
-
Белки; остатков α - аминокислот.
-
С, Н, О, N, S.
-
Десяти тысяч, миллионов.
-
Воде, растворах солей, кислот; щелочах.
-
Ткани живых организмов: кожа, сухожилия, мышцы, ногти, волосы.
-
Первичную, вторичную, третичную, четвертичную.
-
Строительная, каталитическая, двигательная, транспортная, защитная, энергетическая.
Критерии оценки:
«5» - все ответы правильные; «3» - 3 неверных ответа;
«4» - 1-2 неверных ответа; «2» - 4 и более неверных ответов.
ш. Подведение итогов урока. §§38,37 вопросы и задания 1-8, стр.162


