- Преподавателю
- Химия
- Исследовательская работа Роль рабочего листа в управлении познавательной деятельностью
Исследовательская работа Роль рабочего листа в управлении познавательной деятельностью
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Шеховец М.Д. |
| Дата | 09.10.2014 |
| Формат | doc |
| Изображения | Есть |
«Роль рабочего листа в управлении познавательной деятельностью учащихся, ориентированной на повышение результативности учебного процесса»
Исследовательский проект
(краткое содержание)
Шеховец Марина Дмитриевна,
учитель химии и биологии высшей категории
Объект исследования. Познавательная деятельность учащихся
Предмет исследования. Процесс управления познавательной деятельностью
Цель исследования. Изучить влияние управления познавательной деятельностью учащихся с помощью рабочего листа
Гипотеза. Управление познавательной деятельностью на основе применения рабочего листа повышает результативность учебного процесса.
Методы исследования. Диагностика, наблюдение, мониторинг качества знаний учащихся, анкеты.
Срок проведения исследования: ноябрь 2008- май 2011 гг.
Этапы работы над исследованием
-
Вводная часть. Общее знакомство с проблемой исследования.
Абстракт: обоснование актуальности темы, определение объекта и предмета исследования. Формулировка цели исследования и соотнесенных с целями задач.
-
Диагностический этап. Выбор методологии исходной концепции, опорных теоретических положений, единого, определяющего ход и предполагаемого исследовательского замысла, исследовательского подхода.
-
Прогностический этап. Построение гипотезы исследования - теоретической конструкции, истинность которой предстоит доказать.
-
Организационный этап. Выбор методов исследования. Проведение констатирующего исследования с целью установления исходного состояния предмета исследования.
-
Практический этап. Организация и проведение исследования.
-
Обобщающий этап. Анализ информации по проблеме исследования, интерпретация и оформление результатов исследования
-
Оформление практических материалов.
-
Презентация исследовательской работы. Доклад на ШМО. Открытые уроки с использованием рабочего листа.
-
Рефлексивный этап.
Содержание исследовательской работы
-
Актуальность выбора темы. Из теории вопроса.
-
Описание эксперимента: использование рабочих листов для управления познавательной деятельностью учащихся.
3. Выводы. Верификация гипотезы.
4. Обоснование практической ценности исследования.
1.
Актуальность выбора темы. Из теории вопроса.
Тема выбрана не случайно. Проблема управления познавательной деятельностью на уроке является одной из ключевых при организации образовательного процесса в современной школе. Сложность учебной дисциплины вычленяет важнейшую проблему: помочь ученику обрести уверенность, поддержать его стремление к самостоятельному овладению знаниями, навыками самоконтроля и самооценки, самодвижения.
Потребность школы в новом учителе, который не только «учит», но в первую очередь создает условия для запуска процессов саморазвития, самоопределения, самопознания у своих учеников, учителе, владеющем навыками профессиональной управленческой деятельности, остро ощущается в настоящее время.
Управление учащимися на уроке - это управление их познавательной деятельностью. В условиях развивающего обучения важен не только результат этой деятельности (ЗУН), но и сформированность ее структурных компонентов, способов достижения результатов. Для этого познавательная деятельность должна быть специально организована с учетов закономерностей тех психических процессов, которые лежат в ее основе.
Важно отметить ряд принципов организации познавательной деятельности на уроке:
-
активизация познавательных процессов;
-
развитие умения ребенка управлять собственными познавательными процессами;
-
развитие познавательных способностей.
Качество урока во многом зависит от того, насколько выражены на уроке эти тенденции.
Управление - процесс, состоящий из непрерывной последовательности действий, осуществляемых субъектом управления, в результате которых формируется и изменяется образ управляемого объекта; устанавливаются цели совместной деятельности; определяются способы их достижения; разделяется, если необходимо, работа между участниками. Поурочный рабочий лист - это, прежде всего, средство, помогающее школьнику ориентироваться в учебной теме, работать в своем темпе на отдельных этапах урока; при выполнении самостоятельной работы использовать его как технологическую карту, при пробелах в знаниях - как индивидуальный образовательный маршрут, т.е. самостоятельно управлять своей познавательной деятельностью.
2.
Описание эксперимента.
Исследовательская работа проводилась в течение 3-х лет на базе одного класса (в 8-ом классе - апробирование, в 9-11 классах - учащиеся активно включены в эксперимент). Учебный предмет - химия.
В ходе эксперимента в качестве средства управления познавательной деятельностью использовались рабочие листы, в которых была отражена последовательность действий учащихся в ходе урока. На учебных занятиях активно и в системе использовались приемы управления
-
целеполаганием учащихся;
-
мотивацией их деятельности;
-
формированием умений;
-
созданием обратных связей «учитель-ученик»;
-
потоками информации и коррекцией этих потоков;
-
созданием проблемных ситуаций;
-
комфортным самочувствием всех участников образовательного процесса.
Рабочие листы разрабатывались с ориентацией на реализацию данных приемов. В них отражалась вся необходимая для учащихся информация о ходе урока:
-
цели (знать, уметь, понимать);
-
упражнения на формирование умений;
-
вопросы для изучения нового материала и актуализации ранее изученного;
-
необходимая справочная информация;
-
организация лабораторных работ, демонстрационных опытов;
-
проблемные вопросы.
В результате для всех участников учебного процесса создавались комфортные условия: дети знали последовательность основных моментов урока, они имели возможность в индивидуальном темпе изучать новый материал (особенно сильные учащиеся), снималось напряжение при постановке вопроса (если не услышал, можно прочитать), т.е. осуществлялось активное управление познавательной деятельностью.
В процессе реализации управленческих действий в рамках эксперимента
-
намечалась программа проведения проблемно-ориентированного педагогического анализа с целью проведения коррекционной работы;
-
определялся порядок поиска, сбора, переработки, использования, хранения информации;
-
распределялись права, обязанности и полномочия его участников;
-
изыскивался ресурс для изменения процесса;
-
проводилась оценка результативности анализа на основе уточнения причинно-следственных связей;
-
устранялись негативные отклонения.
Для более эффективного осуществления управления познавательной деятельностью учащихся на основе рабочего листа использовались информационные технологии и специальные управленческие техники (присоединения, обучения, подкрепления, педагогические техники Гина). Присоединение осуществлялось через совместную деятельность учителя и учащихся, в ходе которой создавался и поддерживался необходимый психологический контакт, являющийся условием успешного взаимодействия. Использование техник обучения создавало ситуацию успеха. Этому способствовало полимодальное представление информации, учебные метафоры, визуализация информации, формирование новых мыслительных стратегий. Полимодальное представление учебного материала состояло в многостороннем описании представляемого процесса, явления. Информация представлялась в текстовом описании, в виде таблиц, графиков, диаграмм, рисунков, видеоматериалов, слайдовой презентации в сопровождении речи учителя. В процессе изучения материала использовались учебные и управляющие метафоры. Обучение - процесс сложный и поэтому нуждается в подкреплении, которое отличается от поощрения тем, что следует сразу за правильным действием: с этой целью использовались позитивные оценочные слова и предложения, приемы оптимизации времени и места дисциплинирования.
Большое значение уделялось учету закономерности психических процессов, лежащих в основе познавательной деятельности: внимания, восприятия, памяти, мышления. С целью управления вниманием учащихся использовались словесные указания, жесты, интонации. На всех этапах урока проводилось наблюдение за степенью сосредоточенности отдельных учащихся и класса в целом, устранялись ситуативные причины снижения концентрации внимания, отвлечения внимания (словесные раздражители, функциональное состояние нервной системы: утомление, подавленное настроение), что обеспечивалось чередованием умственной деятельности с практической, применением пауз для отдыха. Уроки проводились в энергичном темпе, школьники активно вовлекались в продуктивную деятельность.
Для управления восприятием использовались следующие приемы:
-
четкое определение цели восприятия и его объекта;
-
выделение объекта из общего фона (предметов, текста);
-
использование различных схем, рисунков, графиков;
-
использование наглядных средства усвоения материала: реальные объекты, муляжи, препараты; картины, рисунки, схемы, графики, слайды, кинофильмы, фотографии;
-
яркое образное словесное описание явлений, событий;
-
сравнение воспринимаемых предметов, определение сходства и различия;
-
варьирование условий восприятия, выделение существенных признаков.
В процессе эксперимента в системе использовались приемы организации понимания материала:
-
выявление непонятного и определение пути преодоления непонимания;
-
соотнесение непонятного с понятным, соотнесение с личным опытом;
-
соотнесение с контекстом: учебный материал излагается в определенной системе;
-
соотнесение с лексическими вариантами: перефразировки, изменения словесной формы изложения являются важнейшим приемом достижения понимания материала;
-
соотнесение с образами: соотнести слово с образом и наглядно представить описываемый факт или явление;
-
перенос данных на новые случаи: приводить собственные примеры, факты, о которых не сообщается в учебнике, но которые относятся к изучаемой теме;
-
решение новых задач и упражнений, поясняющий анализ и синтез;
-
поясняющее сравнение, поясняющая конкретизация, обобщение, абстрагирование.
С целью развития памяти использовались приемы установления ассоциативных связей, выделение опорных пунктов, группировка (разбиение материала на части по смыслу, объему, ассоциациям), классификация (группировка материала по определенным известным основаниям); схематизация (графической форма кодирования информации); структурирование (установление связей между частями предмета или явления, позволяющий представить данный предмет или явление в целом), приемы аналогии, установления последовательностей (сериаций).
Развитие мышления обеспечивалось:
-
проблемным изложением материала, созданием проблемных ситуаций;
-
обучением решению различных задач, анализом ситуаций, поиском ответов на различные вопросы, постановкой риторических вопросов при объяснении материала.
Результаты наблюдения за динамикой обученности при использовании рабочих листов и специальных техник управления познавательным процессом:
ученик
9 класс
10 класс
11 класс
Динамика успешности. Результативность
3
3
3
3
3
3
↑
4
4
4
↑
5
5
5
↑
4
4
4
2 место на районной научно-практической (2010г.) конференции школьников
4
5
5
ВКГУ, химия. Грант
3
3
3
↑
3
3
3
3
3
3
↑
3
3
3
4
4
4
↑
4
4
4
Мед. университет. Грант
3
3
4
3
3
3
↑
3
3
4
Мед.колледж. Грант
3
3
3
↑
3
4
4
3
3
3
4
4
4
↑
3
4
4
4
4
4
↑
4
4
4
↑
Кач-во знаний
41%
50%
59%
Мониторинг качества знаний 2008-2011г.
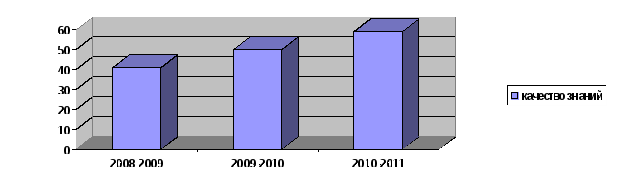
Наблюдение: уровень обученности с начала эксперимента увеличился: на конец 9 класса - 41%, на конец 10 класса - 50%, на конец 11 класса - 59%. Динамика за три года - 18%.
Обоснование:
При стабильной оценке «3», «4» (45%) наблюдаются качественные изменения в знаниях учащихся: прочность, умения обоснованно устанавливать причинно-следственные связи, уверенно (самостоятельно) работать с источниками информации. 23% учащихся повысили оценку по предмету; 3 выпускника выбрали профессии, связанные с изучением химии (педагогическая, медицинская специальности).
У 3 школьников положительной динамики не наблюдается, что объясняется низким уровнем обучаемости по предмету.
С целью изучения уровня удовлетворенности учащихся организацией работы на уроке с опорой на рабочий лист и определения эффективности метода проводилось анкетирование школьников на протяжении их обучения в 9, 10, 11 классе. В рамках опроса выявлялось мнение по следующим вопросам:
Класс
9 класс
10 класс
11 класс
№
Содержание вопросов
Процент положительного воздействия
1
Помогает ли тебе рабочий лист рационально организовать учебный труд на уроке.
16%
90%
75 %
2
Возможно ли успешно управлять своей деятельностью на уроке, ориентируясь на содержание рабочего листа.
75%
81%
84%
3
Позволяет ли рабочий лист работать на уроке в своем темпе, так как все задания и вопросы имеются в рабочем листе.
58%
77%
40%
4
Возможно ли использовать рабочий лист при восполнении знаний в случае пропуска урока
50%
73 %
81 %
5
Помогает ли тебе содержание рабочего листа при выполнении самостоятельной работы на уроке
52%
93%
95%
6
Считаешь ли ты, что работая с опорой на рабочий лист, ты можешь улучшить свои знания по предмету
8%
39 %
45%
7
Считаешь ли ты, что с рабочим листом работать стало интереснее.
16%
45%
75 %
8
Считаешь ли ты, что с рабочим листом учебный материал усваивается легче.
50 %
91%
95%
9
Считаешь ли ты, что рабочий лист не повлиял на эффективность работы на уроке.
8 %
0 %
0 %
Обоснование.
Начиная с 9 класса, учащиеся отмечают положительную роль рабочих листов по пунктам 2, 3, 4, 5 (от 50% и более), а именно: помощь в рациональной организации учебного труда, возможность работать в индивидуальном темпе и использовать рабочий лист для коррекции и восполнения знаний.
Уровень успешности в организации учебного труда на основе рабочего листа (пункт №1 анкеты) значительно повысился в 10 классе, так как учащиеся освоили организационный принцип работы и активно им пользуются. Снижение в 11 классе процента учащихся, отмечающих роль рабочего листа как организационного фактора, может свидетельствовать о достаточном уровне сформированности навыков самоорганизации старших школьников.
Снижение процента положительного воздействия по пункту №3 у учащихся 11 класса возможно объяснить тем, что у выпускников школы в достаточной мере отработан навык работы в заданном темпе.
По остальным вопросам анкеты наблюдается стабильная динамика положительного воздействия рабочего листа на организацию учебной деятельности в рамках школьного урока.
Особая востребованность рабочего листа наблюдается у учащихся 10 класса, так как к этому возрасту формируется прогностическое мышление.
95% одиннадцатиклассников отмечают, что с рабочим листом учебный материал усваивается легче (динамика 45%) , 75% - интереснее (динамика 59%), 45% считают возможным улучшить свои знания по предмету (динамика 37%).
Выводы
Таким образом, предположение (гипотеза), что управление познавательной деятельностью на основе применения рабочих листов повышает результативность учебного процесса, было подтверждено. Труд, затраченный на их разработку, полностью себя оправдал: продуктивнее стало взаимодействие и взаимопонимание между учителем и учащимися; владея информацией о предполагаемых вопросах и заданиях на учебном занятии, школьники могли работать на основных этапах урока в своем темпе. Это создавало и укрепляло ситуации успеха, что способствовало улучшению результатов обучения, повышению интереса к учебной дисциплине, созданию комфортных условий обучения и учения, развитию навыков самоуправления познавательной деятельностью, стимулировало самообразовательную мотивацию.
Использование ИКТ позволяло снимать утомляемость в течение всего урока, так как учебная деятельность совершалась при достаточно высоком интеллектуальном и волевом напряжении.
В ходе эксперимента было установлено, что управление познавательной деятельностью, организованное с учетом закономерностей психических процессов, которые лежат в ее основе (внимание, восприятие, память, мышление), их особенностей проявления и закономерностей формирования на каждом этапе обучения, сделало учебную деятельность более свободной, легкой и увлекательной.
Практическая ценность: найден механизм эффективного управления познавательной деятельностью данного класса; разработаны поурочные рабочие листы по тематическим блокам (химия - 8, 9, 10, 11 класс).
Литература
-
Гаева Е.А. Современные подходы к управлению познавательной деятельностью учащихся на уроке.// school-15-shadr.ucoz.ru › publ/1-1-0-3
-
Тихончук Т.В. Управление деятельностью учеников - важнейшая функция учителя.// ucheba.com › met_rus/k_nachalka/upravlenie.htm
-
Сенновский И.Б. Управленческая деятельность учителя.//portalus.ru
-
Талызина Н.Ф. Управление процессом усвоения знаний.// Москва,1984 г.
-
Ахметов М.А., Мусенова Э.А. Техники управления учебной деятельностью учащихся.//Интернет- журнал «Эйдос». - 2008 г.
-
Клюева Н.В.Педагогическая психология: учебник для вузов. Приемы и техники управления учащимися на уроке.// Москва, 2006 г.
Приложение №1
Образцы рабочих листов к урокам химии 8 - 11 класс
1.
Рабочий лист урока химии по теме «Состав и классификация оснований»
8 класс
Знать: определение основания, классификацию оснований их состав.
Понимать: связь строения оснований и оксидов металлов.
Уметь: определять основания по формуле, составлять формулы оснований и давать им названия.
1.Актуализация знаний.
Закончите уравнения реакций:
Fe + H2O ; CO2 + H2O ; Na + H2O ; CaO + H2O ; LiH + H2O .
Дайте названия полученным веществам.
2.Самостоятельная работа.
А) Прочитать параграф 42 по учебнику и ответить на вопросы:
-
Что общего в формулах всех оснований? Запишите формулу основания в общем виде.
-
Какова валентность гидроксид-группы? Что это за группа? Запишите ее в тетрадь с пояснением.
-
Из каких слов состоит название основания?
-
Дать названия KOH, Mg(OH)2, Fe(OH)3 по международной номенклатуре.
-
По какому признаку делят основания на группы? Назовите эти группы.
-
Как по-другому называются растворимые основания?
-
Как определить, к какой группе относится данное основание?
Б) Разноуровневые задания.
1-й уровень
-
Назовите основания по заданным формулам:
а) Fe(OH)2; б) NaOH; в) Ca(OH)2; г) Ba(OH)2; д) Cu(OH)2; е) Al(OH)3
-
Cоставьте химические формулы оснований по их названиям:
а) гидроксид лития; б) гидроксид магния; в) гидроксид хрома(III); г) гидроксид цинка; д) гидроксид марганца(III); е) гидроксид меди (I).
-
Из приведенного списка выпишите формулы оснований:
HCl, CaO, KNO3, Ba(OH)2, H2SO4, LiOH, CO2, Al(OH)3, KClO, CuOHCl, Cu(OH)2.
-
Из перечня оснований Cu(OH)2, Ca(OH)2, Ba(OH)2, Mg(OH)2, NaOH, KOH, Pb(OH)2, Fe(OH)3, LiOH
выберите:
а) растворимые (щелочи);
б) нерастворимые.
Справочный материал к первому уровню
-
Растворимые (щелочи)
Образуют в ряду активности металлы до Mg
в Т.Р. - Р (искл. Са(ОН)2 -- М)
в П.С. металлы 1-2 группы главной подгруппы (кроме Be , Mg)
-
Нерастворимые
Образуют в ряду активности металлы стоящие после Мg
в Т.Р. - М или Н
в П.С. металлы все остальные, кроме 1-2 А группы и Be,Mg
2-й уровень
-
Составьте формулы оксидов, соответствующих следующим гидроксидам:
а) NaOH ; б) Fe(OH)3 ; в) Ba(OH)2 ; г) CuOH .
(Валентность металла в оксиде такая же, как в основании)
2. Решить стр.112 № 4
3-й уровень
-
Решить на стр. 112 №5, №6.
4. Подумай и определи для себя:
-
Сегодня на уроке я узнал…
-
Я хорошо понял…
-
Мне нужно еще поработать над вопросом…
-
Свою работу на уроке я оцениваю на …
Домашнее задание. Всем - параграф 42. По выбору задания 2-го и 3-го уровня.
РЯД НАПРЯЖЕНИЯ МЕТАЛЛОВ
Li Cs K Rb Ba Sr Ca Na Mg Al Ti Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi Cu Ag Hg Pt Au
2.
Рабочий лист к уроку химии по теме «Характеристика элемента»
8 класс
Знать: основные характеристики элемента.
Уметь: определять основные характеристики элемента по положению в периодической системе
Понимать: связь свойств со строением, положения элемента в периодической системе с его строением и свойствами.
1. Самостоятельная работа в парах:
а) заполнить таблицу;
б) работа по справке: взаимопроверка;
в) охарактеризовать по плану предложенные элементы натрий, кремний, хлор.
Характеристики
Справка
Элементы
Элемент, знак
Na
Si
Cl
As
Положение в периодической системе
-
порядковый номер n/n
-
атомная масса Ar
-
№ периода
-
какой период
-
№ группы
-
подгруппа (главная, побочная)
Горизонтальный ряд
1-3 малые
вертикальный ряд
красным, желтым главные
Строение атома
-
заряд ядра Z
-
протоны p+
-
электроны e
-
нейтроны n0
-
внешние электроны
-
число слоев
-
распределение по слоям
-
электронная формула
= n/n
= n/n номеру
= n/n номеру
= Ar - n/n
= № группы (глав)
= № периода
1s 2s 2p 3s 3p 4s 3d 4p
Свойства простого вещества
-
металл-неметалл
-
валентность по кислороду
-
валентность по водороду
-
сравнение с соседями
= № группы
= 8 № группы
Соединения
-
высший оксид
-
характер оксида (основной, кислотный, амфотерный)
-
гидроксид
-
летучее водородное соединение (для неметаллов)
Валентность по О
Валентность по водороду
Дополнение к справке (5-ый вопрос)
Соответствие оксидов гидроксидам:
Основной оксид
Me2O MeOH MeO Me(OH)2 Me2O3 Me(OH)3
Кислотный оксид
R2O3 HRO2
RO2 H2RO3
R2O5 HRO3, H3RO4
RO3 H2RO4
R2O7 HRO4
Амфотерному соответствует и кислота и основание.
Домашняя работа: знать связь характеристик элемента с положением в периодической системе; охарактеризовать мышьяк.
Подумай и определи для себя:
-
Сегодня на уроке я узнал…
-
Я хорошо понял…
-
Мне нужно еще поработать над вопросом…
-
Свою работу на уроке я оцениваю на …
3.
Рабочий лист к уроку химии по теме «Химические свойства водорода»
8 класс
Знать: химические свойства водорода
Уметь: составлять уравнения с участием водорода, составлять формулы водородных соединений элементов.
Понимать: зависимость состава продуктов реакции от особенностей элементов.
Выполни задания.
Вставьте пропущенные слова в предложения:
-
Какими способами можно собирать водород и почему?
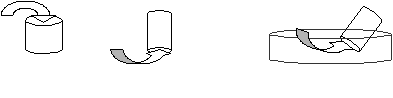
-
Молекула водорода состоит из ____ атомов. Его формула________
-
Относительная атомная масса водорода равна________
-
Относительная молекулярная масса водорода ________
-
Водород имеет постоянную валентность, равную ___
-
Водород - газ без ________, ____________, ______.
-
Водород можно получить при действии электрическим током на _________
-
Металлы вытесняют его из _________ и ________
-
Укажите ряд, в котором все металлы можно использовать для получения водорода (в ряду активности до Н) а) Zn, Ca, Al б) Cu, Ca, Na в) Fe, Zn, Hg г) S, Zn, Ca. Почему?
-
Закончите уравнения реакций:
K + H2O → + ; H2O → + ; HCl + Ca → +
Изучение нового материала.
Ознакомьтесь с материалом параграфа «Химические свойства водорода». Найдите ответ на следующие вопросы:
-
С какими веществами вступает в реакцию водород? Проверьте по схемам.
-
Для чего используют водород?
-
Рассмотрите диаграмму №1 и объясните, почему Циолковский считал водород топливом будущего?
Выполните упражнения:
-
Составьте формулы водородных соединений кислорода, серы, хлора, углерода, азота, фосфора. Валентность элемента определяем по формуле 8 - №группы (столбик в периодической системе).
-
Закончите уравнения реакций водорода с простыми веществами:
H2 + O2 → N2 + H2 → H2 + Cl2 →
Na + H2 → Ba + H2 →
-
Закончите уравнения реакций водорода с оксидами металлов:
Fe2O3 + H2 → CuO + H2 → Pb3O4 + H2 →
-
Напишите уравнение реакции получения водородных соединений(CH4, PH3, H2S, CaH2, KH) из простых веществ.
-
Составьте уравнения реакций взаимодействия водорода с:
а) оксидом вольфрама(VI), б) оксидом ртути (II), в) оксидом меди (I), г) оксидом хрома (III).
Схемы:
-
Ме + Н2 МеН
-
неМе + Н2 неМеН
(валентность неМе определяем по периодической системе 8-группы(столбик)
-
МеО + Н2 Ме + Н2О
Диаграмма №1 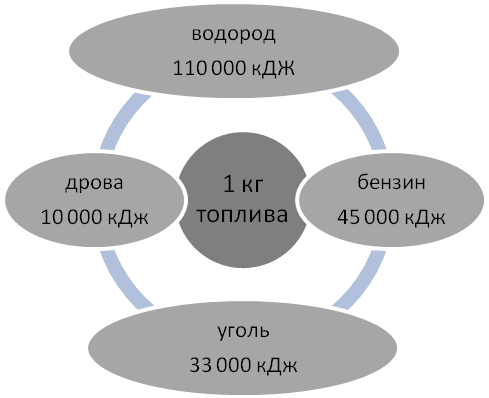
Домашнее задание: учебник стр. 88 №5, №6, параграф 32.
Подумай и определи для себя:
-
Сегодня на уроке я узнал… .
-
Я хорошо понял... .
-
Мне нужно еще поработать над вопросом… .
-
Свою работу на уроке я оцениваю на… .
Рабочий лист к уроку химии по теме «Алканы»
9 класс
Ответь на вопросы:
-
Какие особенности органических веществ вам известны?
-
Как соединяются атомы в молекулах органических веществ?
-
Назовите основные элементы, которые входят в состав большинства органических веществ. Какую валентность они проявляют?
Изучение нового материала:
Подумай: что общего у моторного масла, парафиновой свечи, бензина, газовой зажигалки?
Подумайте, на какие вопросы вы должны ответить сегодня на уроке?
Знать:
Уметь:
Понимать:
Изучите предложенный учителем материал по теме. Найдите ответы на следующие вопросы:
-
Общая формула____________
-
В каких агрегатных состояниях встречаются эти углеводороды__________
-
С чем связано их агрегатное состояние_______________________________
-
Гомологи - это___________________________________________________
-
Физические свойства метана________________________________________
-
Химические свойства метана.
Реакция ___________________________ СН4 + ? → ? + ?
Реакция ___________________________ СН4 + ? → ? + ?
Вклейте результаты в тетрадь.
Выполните лабораторную работу.
-
Используя пластилин и спички, изготовьте модели молекул метана (СН4). Помните, что электронные облака заряжены отрицательно и будут отталкиваться друг от друга. Поэтому все углы должны быть одинаковыми. Какая геометрическая фигура получится, если соединить все атомы водорода? Зарисуйте полученную модель в тетрадь, укажите на рисунках угол между связями.
-
Используя пластилин и спички, смоделируйте реакцию замещения между хлором и метаном. Зарисуйте модель реакции в тетрадь.
-
Используя пластилин и спички, изготовьте модели молекул этана(С2Н6), пропана(С3Н8) и бутана(С4Н10), используя знания о строении предельных углеводородов. Зарисуйте полученные модели в тетрадь, укажите на рисунках угол между связями.
Домашняя работа: параграфы 46,47.
Подумайте и определите для себя:
-
Что нового вы узнали на уроке… .
-
Чему научились… .
-
Что получилось… .
-
Что не получилось… .
-
Свою работу на уроке я оцениваю на… .


