- Преподавателю
- Химия
- Расчёт констант скоростей первого и второго порядка. Расчёт энергии активации
Расчёт констант скоростей первого и второго порядка. Расчёт энергии активации
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Матюгина И.И. |
| Дата | 25.10.2014 |
| Формат | docx |
| Изображения | Есть |
 Расчёт констант скоростей первого и второго порядка. Расчёт энергии активации».
Расчёт констант скоростей первого и второго порядка. Расчёт энергии активации».
Цель работы: Математически рассчитать энергию активации и константы скоростей реакций по заданным условиям.
Теоретическая часть:
Энергия активации - это минимальное количество энергии, которая требуется сообщить системе, чтобы произошла химическая реакция.
Согласно теории активных соодарений, для того, чтобы произошла химическая реакция происходят следующие условия:
-
Молекулы должны столкнуться.
-
Молекулы должны быть правильно ориентированы относительно друг друга.
-
Молекулы должны обладать необходимой энергией (энергией активации).
Уравнение Аррениуса устанавливает связь между энергией активации и скоростью протекания реакции.
Еа = -RT ln(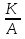 )
)
K - const скорости реакции;
А - фактор частоты для реакции;
R - универсальная газовая постоянная;
Т - температура в градусах Кельвина.
Для количественного описания температурных эффектов используют правило Вант - Гоффа: повышение температуры на каждые 10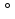 увеличивает скорость хим. Реакции в 2-4 раза.
увеличивает скорость хим. Реакции в 2-4 раза.
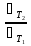 =
= 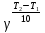
Правило Вант- Гоффа является не точным, гораздо точнее описывает зависимость температуры и скорости уравнения Аренниуса
K(T) = Aexp 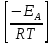
При низких температурах реакция почти не протекает К(Т)→0; при высоких температурах constскорости К(Т) →А.
Энергию активации можно определить измерив constскорости, при двух разных температурах.
EA = 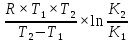
Для реакции первого порядка const скорости К(Т) выражается
через степень превращения К = 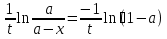
Aexp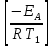 =
= 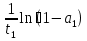 (1)
(1)
Aexp 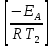 =
= 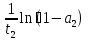 (2) поделили первый уровень на второй и прологарифмировали.
(2) поделили первый уровень на второй и прологарифмировали.
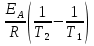 = ln
= ln 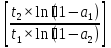
Задание 1:
Используя уравнение Аррениуса, оцените при каких температурах и энергиях активации справедливо правило Вант - Гоффа.
.
Задание 2:
При какой температуре завершается на 80% реакция, если энергия активации равна 60 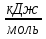 и время 120 мин.
и время 120 мин.
Принять необходимым условием, что эта реакция имеет первый порядок и при температуре 70 завершается на 40% за 60 мин.
завершается на 40% за 60 мин.
Задание 3:
Скорость гидролиза удваивается при переходе от температуры - 1,1  к температуре 2,2
к температуре 2,2  . Найдите энергию активации реакции.
. Найдите энергию активации реакции.


