- Преподавателю
- Химия
- Методическая разработка урока по теме Железо строение, свойства, получение и применение
Методическая разработка урока по теме Железо строение, свойства, получение и применение
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Лепешенко Т.И. |
| Дата | 18.10.2014 |
| Формат | docx |
| Изображения | Есть |
|
| ||||
| Тема урока | Железо, его строение, свойства, применение, способы получения | |||
| Дисциплина | Химия | |||
| Курс 1 | Группа 15 | |||
| Автор урока | Лепешенко Татьяна Ивановна преподаватель химии и биологии высшей квалификационной категории | |||
| Образовательное учреждение | Государственное бюджетное образовательное учреждение начального профессионального образования Ростовской области профессиональное училище №61 им. Героя Советского Союза Вернигоренко И.Г. | |||
| Республика/край, город/поселение | Россия, Ростовская область, город Новошахтинск | |||
| Методическая информация | ||||
| Тип урока
| Изучение нового материала | |||
| Цели урока
| Образовательная: Рассмотреть историю появления железа, строение атома железа, нахождения железа в природе. Изучить свойства железа, способы получения применения железа. Развивающая: Развить навыки самостоятельной работы и умения применять полученные знания на конкретных примерах; активизировать обучающихся к дальнейшему изучению химии. Воспитательная: Научить обучающихся вырабатывать свое мнение, аргументировано его выражать, уважать мнение товарищей. | |||
| Используемые педагогические технологии, методы и приемы: | Словесно-логические - рассказ, объяснение, беседа; Активные- проблемное изложение материала; Иллюстративные - демонстрация мультимедийной презентации; Практические - работа с опорным конспектом, выполнение тестовых заданий, работа с наглядным пособием, учебниками, конспектом. | |||
| Знания, умения, навыки и качества, которые актуализируют/приобретут/закрепят /др. обучающиеся в ходе урока | Главная задача урока - сформировать знания о возникновении железа, нахождении в природе и ПС, а стержневая - знания о свойствах, способах получения и применения железа. Особенности группы учтены, как при фронтальном опросе, так и в индивидуальной работе с обучающимися.
| |||
| Время реализации урока | 45 минут | |||
| Необходимое оборудование и материалы | Мультимедийное оборудование, раздаточный материал - опорный конспект, учебники, ПК, таблица химических элементов Д.И. Менделеева. Список учебной и дополнительной литературы: Основная:
| |||
|
Подробный конспект урока | ||||
| Этапы урока | Деятельность преподавателя | Деятельность обучающихся | ||
| Организационный
| Здравствуйте. Ребята, на ваших столах опорные схемы, которые помогут сегодня в изучении нового материала и рабочие листы, на которых вы будете отмечать правильные ответы знаками «+» Сегодня нам предстоит познакомиться с удивительном веществом. Это - … Вы сами назовете его. «Громоподобные раскаты И в небе раскаленный след: На землю новый камень падал И ужасался человек» У древних греков и египтян этот металл называли «небесным камнем» Слайд 1 | Приветствие преподавателя. Подготовка к уроку. | ||
| Актуализация знаний
| Вопрос: Что объединяет эти изображения? Вопрос: Откуда появилось название?
«вЕРИТЕ ЛИ ВЫ?» на Каждый вопрос - ответ с аргументом. (группе даётся по одному вопросу для обсуждения 0,5 мин. Затем)
вопрос: Есть ли другие мнения? Слайд 2 Первые образцы железа, попавшего в руки человека, очевидно, были метеоритного происхождения. О знакомстве человека в древности с железом космического происхождения говорит факт наличия у жителей Гренландии, не имевших никакого понятия о железной руде, изделий из железа. В древности у некоторых народов железо ценилось дороже золота. Алхимики обозначали железо в виде копья и щита - характерных атрибутов бога войны Марса. На Землю падают метеориты, состоящие в основном из железа. Метеоритное железо самородное. Железо обнаружено также на Марсе и на Луне. Самородное железо на Земле - редкость. Ядро Земли состоит из железа и никеля, но они не доступны для человека. Мы выяснили тему урока. Как обычно, изучая химию элементов, что мы рассматриваем, какие цели ставим? (при необходимости откорректировать её) Слайд 3 | Предполагаемый ответ: «Железо». Записывают тему урока в тетрадь. Предполагаемый ответ: Железо (лат. Ferrum) - быть твёрдым. В переводе с древнеегипетского название железа означало «Небесное железо». В переводе с древнегреческого - «Звезда», «Небесное тело». отвечают на вопросы.
Слушают преподавателя
Формулируют цель и задачи урока | ||
| Формирование знаний
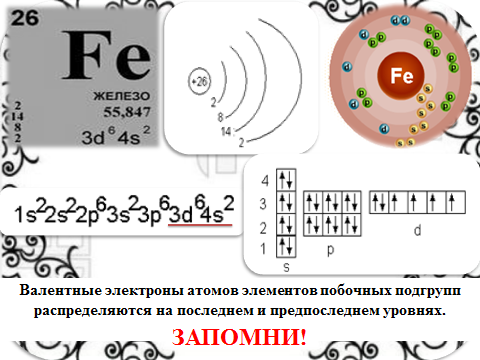
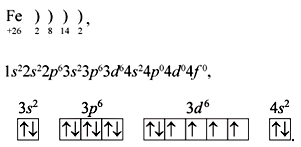
| Дайте характеристику железа по положению в ПСХЭ. Слайд 4 Строение атома железа как элемента побочной подгруппы (d-элемента). Слайд 5 Особенностью электронного строения элементов побочных подгрупп является - заполнение электронами не последнего, а предпоследнего уровня. Валентные электроны атомов элементов побочных подгрупп распределяются на последнем и предпоследнем уровнях.
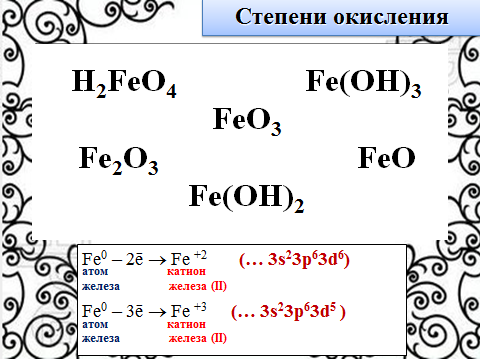
Слайд 6 Вопрос: Какова степень окисления железа? Железо образует соединения с различными степенями окисления: характерны две основные степени окисления: +2, +3. Существуют также малоустойчивые соединения, в которых железо находится в степени окисления +6. Такое разнообразие степеней окисления обусловлено тем, что валентными электронами в атоме железа являются не только электроны внешнего слоя, но и электроны предвнешнего слоя. Fe0 -2e - Fe+2 Fe0 -3e - Fe+3 Давайте подберем генетические пары для каждой из с.о. железа (оксид и соответствующий гидроксид). Характерные соединения железа: FeO основной оксид железа (II) Fe(OH)2 нерастворимое основание гидроксид железа (II) | Fe2O3 амфотерный оксид железа (III) Fe(OH)3 амфотерное основание гидроксид железа (III) | FeO3 кислотный оксид железа (VI) H2FeO4 железная кислота
| |
Слайд 7 - 8
Нахождение в природе. Важнейшие минералы.
Железо (Fe) - 2-й элемент по распространённости в природе металл (после алюминия (Al). В земной коре его массовая доля составляет 5,1%. Входит в состав различных руд. Россия занимает 1-е место по запасам железных руд.
В свободном виде не корродирует только метеоритное железо.
4-е место среди элементов по значимости, второе место по распространенности в природе;
В организме человека содержится около 5 г железа. Из них 57% приходится на гемоглобин крови, 7% - на миоглобин мышц, 16% связаны с тканевыми ферментами, 20% - это запас, отложенный в печени, селезёнке, костном мозге и почках.
Слайд 9
Способы получения железа.
Вопрос: Какие вам известны способы получения металлов?
восстановление железа из его оксида оксидом углерода (II) или водородом; Fe2O3 + 3CO → 2Fe + 3CO2
Fe2O3 + 3H2 → 2Fe + 3H2O
восстановление железа из его оксида алюминотермическим методом; Fe2O3 +2Al → Al2O3 + 2Fe
электролизом водных растворов солей железа (II)
Слайд 10
Применение железа
Вопрос: Каковы же потребительские качества изделий из железа?
Слайд 11
Физические свойства железа.
Вопрос: Какие физические свойства характерны для металлов?
Вы правы. Железо - серебристо-белый или серый металл, твердый, с высокой пластичностью, теплопроводностью и электропроводностью, плотность его равна 7,87 г/см3, тугоплавкий- температура плавления +15400С.
Сплавы на основе железа (чугун и стали) универсальны, технологичны, доступны, дешевы.
Вопрос: Какими ещё свойствами обладает железо?
Демонстрация опыта: намагничивание железного гвоздя.
Да, в отличие от других металлов, железо способно намагничиваться, оно обладает ферромагнетизмом.
Слайд 12
Химические свойства.
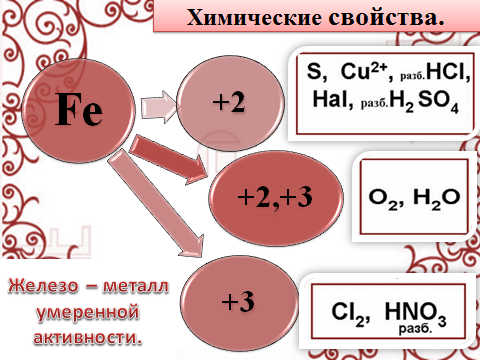
Рассмотрим химические свойства железа. Железо дает два ряда соединений, соответствующих степени окисления +2, +3. Степень окисления Fe зависит от окислительной способности реагирующего вещества. У сильных окислителей железо принимает степень окисления +3, у более слабых +2.
Обратим внимание на характерные для железа реакции:
Взаимодействие с неметаллами
Слайд 13,14
Взаимодействие с водой и разбавленными кислотами Слайд 15, 16,
Взаимодействие с кислотами-окислителями
Слайд 17
Горение железа (видео опыт)
Проблемный эксперимент: (железный гвоздь опустим в медный купорос) Алхимики, не зная состава медного купороса, считали, что его водный раствор может превращать железо в медь. Какое свойство металла демонстрирует этот опыт?
Слайд 18
Задание «Найдите ошибку».
Слайд 19
Решение задачи (у доски)
В 150,0 г. 9%-ного раствор хлорида меди (II) опустили железный гвоздь. Масса образовавшейся меди равна ___ г.. (Запишите число с точностью до десятых) (64 г.)
Слайд 20
Характеризуют положение железа в ПСХЭ (проверка на слайде)
Записывают в тетрадь электронные схему и формулу атома железа.
Предполагаемый ответ: (+2, +3)
Записывают в тетрадь схемы.
(пояснение - восстановительные свойства)
Выполняют задание в тетради (проверка на слайде)
Записывают в тетрадь формулы природных соединений железа.
Предполагаемый ответ: Восстановление металлов из их оксидов восстановителями.
Просмотр видео алюмотермический метод
Предполагаемый ответ:
Примерно 90% используемых человечеством металлов - это сплавы на основе железа. Железа выплавляется в мире очень много, примерно в 50 раз больше, чем алюминия, не говоря уже о прочих металлах. Сплавы на основе железа (чугун и стали) универсальны, технологичны, доступны, дешевы.
Предполагаемый ответ: Металлический блеск, Пластичность Ковкость, Электро- и теплопроводность…
Предполагаемый ответ:
Способность притягиваться магнитом -намагничивание.
Записывают физические свойства железа в тетрадь.
Записывают реакции в тетради по мере просмотра слайдов, используя опорные схемы.
Просматривают видеоопыты «Качественные реакции на ион Fe2+
и Fe3+»
Смотрят видеоопыт «Горение железа»
Предполагаемый ответ:
Взаимодействие железа с растворами солей.
Предполагаемый ответ: Железо не будет взаимодействовать с раствором хлорида натрия.
Закрепление знаний


Следующие задания вы выполняете в рабочем листе.
Восстановите деформированный текст, представляющий собой генетические ряды железа Fe+2, Fe+3.
-
Fe …. Fe(OH)2 FeO
-
Fe FeCI3 …. Fe2O3
Установите соответствие между реагирующими веществами и продуктами их взаимодействия:
РЕАГИРУЮЩИЕ ПРОДУКТЫ
ВЕЩЕСТВА ВЗАИМОДЕЙСТВИЯ
А) Fe + Cl2 → 1) FeSO4 + H2
Б) Fe + HCl → 2) Fe2(SO4)3 + H2
B) Fe + H2SO4 (разб.) → 3) Fe2(SO4)3 + SO2 + H2O
Г) Fe + H2SO4 (конц.), t → 4) FeCl2 + H2
5) FeCl3 + H2
6) FeCl3
«Да/нет» (на карточках, с проверкой на слайде. Взаимопроверка)
-
Железо - это активный щелочной металл.
-
Железо легко куется.
-
Железо входит в состав сплава бронзы.
-
На внешнем энергетическом уровне атома железа 2 электрона.
-
Железо взаимодействует с разбавленными кислотами.
-
С галогенами образует галогениды со степенью окисления +2.
Вариант 2.
-
Железо - это металл серебристо-белого цвета.
-
Железо не обладает способностью намагничиваться.
-
Атомы железа проявляют окислительные свойства.
-
На внешнем энергетическом уровне атома железа 1 электрон.
-
Железо вытесняет медь из растворов ее солей.
С галогенами образует соединения со степенью окисления +3.
Слайд 21
Предполагаемый ответ:
1) Fe FeCI2 Fe(OH)2 FeO
2) Fe FeCI3 Fe(OH)3 Fe2O3
Предполагаемый ответ:
А) 6; Б) 4;
В) 1; Г) 3.
Подведение итогов


Домашнее задание
§43, упр. 1-4.
-
Составьте текст рекламы изделий из железа
-
Приготовьте вопрос для интервью у Железа.
Слайд 22
Вернемся к изображениям, с которых начали.
Что Вам стало понятным в ходе занятия.
Что бы Вы добавили после сегодняшнего занятия?
Оценивание работы учащихся.
Записывают домашнее задание.