- Преподавателю
- Химия
- Уроки химии по технологии критического мышления
Уроки химии по технологии критического мышления
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Григоренко Е.В. |
| Дата | 24.03.2015 |
| Формат | doc |
| Изображения | Есть |
Развитие критического мышления на уроках химии
Разработки уроков на основе технологии развития критического мышления
Урок №1
Теория электролитической диссоциации - 9 класс
Цели урока:
1. Сформировать основные понятия: электролиты, неэлектролиты, электролитическая диссоциация, катионы, анионы.
2. Дать представление о механизме электролитической диссоциации.
3. Привести учащихся к умению создавать проблемные ситуации и видеть пути их решения.
4. Обучать аргументировано защищать свою точку зрения.
5. Развитие коммуникативных способностей.
Оборудование: прибор для проверки проводимости водных растворов электролитов.
Водные растворы: дистиллированная вода, кристаллы поваренной соли, раствор соляной кислоты, раствор щелочи, водный раствор спирта.
План урока
I. Стадия "Вызова"
Вступление
Мы приступаем к изучению проводимости растворов некоторых классов веществ. Электрический ток в металлах и растворах некоторых веществ вы изучали в курсе 7-го класса. Новый материал запоминается легче, если он нанизывается на уже полученные знания. Поэтому сейчас предстоит работа с извлечением этого материала из памяти.
а) Стадия " Вызова"
Расчертите листок на три части и подпишите графы.
-
Я знаю
Хочу узнать
Что узнал?
В течение 5-ти минут каждый из вас заполнит графу, отвечая на вопросы: см. приложение №1.
Приложение № 1
Электрический ток в металлах и в растворах щелочей, кислот, солей
а)Прочти следующие вопросы:
1. На какие частицы распадаются при растворении в воде вещества?
2. Какие два рода электрических зарядов существуют в природе?
3. На какие две группы делятся вещества по способности проводить электрические заряды?
4. Что представляет собой электрический ток в водных растворах солей, кислот, щелочей?
5. Как называют растворы этих веществ?
6. Как возникают заряженные частицы в водном растворе этих веществ?
Очень кратко запиши свои ответы в первой колонке таблицы № 1.
б) Перескажите друг другу ваши записи. (15 мин.)
в) Выделите ключевые понятия по теме "Электрический ток" в электролитах и в растворах щелочей, кислот, солей.
г) Какая информация у вас осталась неполной?
Заполните 2-ю графу таблицы «Не знаю».
Как правило, 80% учащихся осознают проблему в том, что открытие вопроса остаётся на пункте: №6. Как возникают заряжённые частицы в одном растворе этих веществ?
Возникает ещё одна проблема - откуда у веществ с молекулярной решёткой в растворе появляются ионы.
Демонстрация опыта и заполнение таблицы приложения №2.
См. приложение №2.
Приложение №2
Демонстрационный опыт
Исследовать электрическую проводимость веществ с различным типом связи.
ЦЕЛЬ: Установить на какие частицы (молекулы, ионы) распадаются при растворении вещества с различным типом связи.
ИНСТРУКЦИЯ
1. Внимательно прочитайте задание и цель исследования.
2. Систематизируйте вещества по характеру химической связи и типу кристаллической решетки.
3. Выскажите предложения, какие из исследуемых веществ при растворении в воде будут распадаться на молекулы, а какие на ионы.
4. Пронаблюдайте опыт.
5. Результаты опыта сформулируйте в виде таблицы.
II. Стадия "Осмысление"
См. опорный конспект.
Сущность процесса электролитической диссоциации
Электролиты - вещества, проводящие в растворенном или расплавленном состоянии электрический ток, вследствие распада их на ионы.
Примеры электролитов: соли, щелочи, кислоты. В этих веществах имеется ионная или ковалентная сильнополярная связь.
Неэлектролиты - вещества, водные растворы которых не проводят электрический ток. К таким веществам относят кислород, водород, сахар, глицерин. Для них характерна ковалентная неполярная или малополярная связь. Процесс распада электролита на ионы при растворении его в воде или расплавлении называется электрической диссоциацией.
Для правильного понимания механизма растворения в воде веществ следует учесть строение молекулы воды и вид связи растворяемого вещества.
В молекулах воды между атомами водорода н кислорода имеются ковалентные сильнополярные связи:
Поэтому молекулы воды полярны: 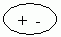 диполь.
диполь.
Вследствие этого, например, при растворении хлорида натрия молекулы воды притягиваются отрицательными полюсами к положительно заряженным ионам натрия кристаллической решетки, а положительными полюсами - к отрицательно заряженным ионам натрия. Такой процесс называется гидратацией, он идет с выделением энергии. Энергия гидратация приводит к разрушению кристаллической решетки и вещество распадается на ноны.
Притяжение и действие полярных молекул воды на кристаллическую решётку хлорида натрия.
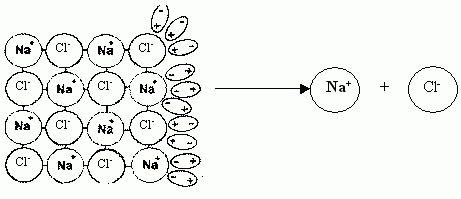
При растворении в воде веществ с ковалентной сильнополярной связью, например хлороводорода НС1, происходит изменение характера химической связи, т.е. под влиянием энергии гидратации ковалентная связь превращается в ионную и далее процесс протекает как у веществ с ионной связью.
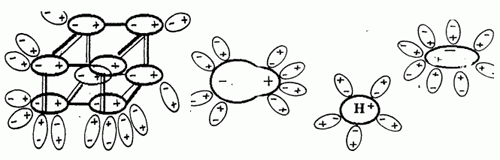
При расплавлении электролитов усиливаются колебательные движения частиц, что приводит к ослаблению связи между ними. В результате также разрушается кристаллическая решетка и образуются ионы.
В растворе и расплаве электролита ионы движутся хаотически.
Идёт работа с текстом и его маркировка, учащимся предлагается по ходу текста ставить следующие знаки:
V - уже известно
+ абсолютно новое, неожиданное;
- противоречит твоим представлениям;
? хочется узнать что-то больше.
На данной стадии идёт соотношение уже известного с тем, "что узнал". Происходит структурная организация информации в памяти. Можно спросить, у учащихся какие у них были знаки?
III. Стадия "размышления" (рефлексия)
Учащиеся должны попробовать выразить информацию, которую получили своими словами. (Работа с графой №3 таблицы - "Что узнал?").
Выяснили, какие новые понятия они увидели в тексте. (Эти пояснения записываем в 3-ю колонку).
Рассказать о механизме диссоциации веществ с ионным типом связи.
Рассказать о механизме диссоциации веществ с ковалентным типом связи.
Домашнее задание: § 1. Выучить понятия, знать механизм диссоциации. Ответить на вопрос: процесс растворения физический или химический. Подобрать доказательства в пользу каждого процесса.
Урок №2
Тема: Глюкоза. Строение глюкозы. 10 класс
Тип урока: Изучение нового материала
Цели:
I. Обучающие
1. изучение структуры глюкозы - структурной формулы
2. закрепление навыков проведения лабораторных опытов
II. Развивающие
1. овладение универсальными методами познания -
критическим мышлением.
2. научить ученика самостоятельно мыслить, осмысливать,
структурировать и передавать информацию.
3. умение формулировать проблему и находить пути ее
решения
III. Воспитывающие
1. Создание повышенной мотивации изучения нового
материала.
Оборудование:
Глюкоза (тв), вода в стаканчике, раствор сульфата меди (II),
гидроксид калия, держатель, спиртовка, спички, магниты,
транспаранты с фразами
"Знаю"
"Хочу знать"
"Узнал"
"Синквейн"
Особенности урока:
Урок по технологии «Развитие критического мышления»
Ход урока.
1.Рассказ (вступительное слово учителя)
1.0рганизационный
момент
П.
1 .Ответы на вопросы учителя и заполнение
колонки "Знаю"
Постановка проблемы учащихся и начало
заполнения "Хочу знать"
2.Проведение лабораторного опыта
"Изучение свойств глюкозы" и
заполнение колонки "Узнал"
Постановка новой проблемы в
колонке "Хочу знать" и работа с книгой
Продолжение колонки "Узнал"
2.Изучение нового
материала
1 .Стадия "Вызова"
2. Стадия "Осмысление" (добыча знаний)
III.
1 .Анализ колонки "Узнал", сравнение ее с
колонкой "Знаю", "Хочу знать"
2.Построение структурной формулы
глюкозы на основе изученных свойств.
3.Написание синквейна на тему
"Строение и свойства глюкозы"
Ш.Стадия "Рефлексия"
IV.
1 .На основе полученной структуры
и изученных свойств глюкозы
записать уравнения реакций
4.Домашнее задание
Вступительное слово учителя.
На прошлом уроке мы познакомились с общим представлением об углеводах,
их классификацией. Одним из представителей класса моносахаридов
является глюкоза. Наша цель - изучить строение глюкозы, т.е. вывести ее
структурную формулу. Добывать знания вы будете сами - строить гипотезы и
искать им доказательства. Работаем сегодня с вами в стиле " развития критического мышления" (Учащиеся работают по этой технологии не в первый раз, т.е. знают этапы и некоторые приемы). Откройте тетради и запишите тему « Глюкоза. Строение глюкозы.»
Разделите тетрадный лист на 3 части и подпишите колонки: "Знаю", "Хочу
знать", "Узнал".
Работаем с 1-ой колонкой.
Из курса биологии вы знаете молекулярную формулу глюкозы.
Назовите формулу и запишите в первую колонку. О наличии каких функциональных групп мы можем сделать предположение исходя из состава.
Учащиеся заполняют колонку «хочу знать». После постановки гипотезы проделывают лабораторную работу на наличие многоатомности и обнаружение альдегидной группы.
На основе опытов учащиеся строят структурную формулу глюкозы.
Вид доски.
Тема: Глюкоза. Строение глюкозы.
Знаю
Хочу узнать
Узнал
Синквейн
Гипотезы:
1. Глюкоза - кислородосодержащее вещество
2. Глюкоза - углевод
3. С6Н12О6
1 .К какому классу
веществ можно
отнести глюкозу?
а)к альдегидам
б)к многоатомным спиртам
в)к карбоновым кислотам
2.Какая углеродная цепь - линейная или разветвленная?
3.Сколько
гидроксильных групп
содержит глюкоза?
Лабораторная работа
"Изучение свойств глюкозы"
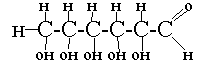
существительное
три прилагательных
два глагола
крылатая фраза
существительное
По данной технологии записей больше у учащихся, поэтому представляю вид записей у учащихся (см. следующую стр.) записи в тетради у учащихся. На доске я только напоминаю форму и распределение записей в колонках у
учащихся (ступенчатый)
Вид записи в тетради у учащихся.
Тема: Глюкоза. Строение глюкозы.
Знаю
Хочу узнать
Узнал
Гипотезы:
1. Глюкоза - кислородосодержащее вещество
2. Глюкоза - углевод
3. С6Н12О6
1 .К какому классу
веществ можно
отнести глюкозу?
а)к альдегидам
б)к многоатомным спиртам
в)к карбоновым кислотам
2.Какая углеродная цепь - линейная или разветвленная?
3.Сколько
гидроксильных групп
содержит глюкоза?
Лабораторная работа:"Изучение свойств глюкозы"
1.гидроксидмеди (II) от раствора
глюкозы синеет -> глюкоза многоатомный спирт
2. раствор глюкозы с гидроксидом
меди (II) при нагревании
краснеет -> глюкоза содержит
альдегидную группу
3. присоединяет до 5 молекул
уксусной кислоты-> 5
гидроксильных групп
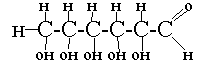
Синквейн:
Глюкоза
Сладкая, растворимая, энергетическая
Краснеет и синеет от Cu(OH)2
Хочешь лучше думать - съешь глюкозу
Альдегидоспирт.
Домашнее задание:
Учебник Габриелян О.С. 10 кл. §22, моносахариды
Записать уравнения реакций по третьей колонке «Узнал»:
1. Глюкоза - альдегид 2. Глюкоза - многоатомный спирт (На основе лабораторной работы).


