- Преподавателю
- Химия
- Расчёт теплоёмкости системы по табличным термодинамическим данным
Расчёт теплоёмкости системы по табличным термодинамическим данным
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Матюгина И.И. |
| Дата | 19.02.2014 |
| Формат | docx |
| Изображения | Есть |
Практическая работа №3
Тема: «Расчёт теплоёмкости системы по табличным термодинамическим данным».
Цель работы: Практически рассчитать мольную и изобарную теплоёмкость.
Теоритическая часть:
Теплоёмкость - это отношение количества теплоты, сообщённой системе в каком - либо процессе, к соответствующему изменению температуры.
В зависимости от условия протекания процесса, различают теплоёмкость при постоянном объёме (Cv)
Теплоёмкость при постоянном давлении равна:
Cv= 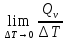 Cv=
Cv= 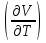 v
v
Cp= 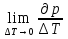 Cp=
Cp= 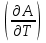 p
p
Следовательно, теплоёмкость Cv и Cp показывают как изменяются с температурой соответственно внутренняя энергия и энтольпия вещества, следовательно, теплоёмкости являются температурными коэффициентами этих величин.
Теплоёмкость, отнесённую к одному молю вещества называют, молярной теплоёмкостью, измеряют 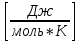
Разность между молярной теплоёмкостью идеального газа, равна универсальной газовой постоянной: Cp - Cv = R
Теплоёмкость является функцией температуры и она равна: Cp = a+вТ+с'T-2 коэффициенты а,в,с являются табличными данными и найдены для всех известных веществ.
Ход работы:
Задача №1:
Найдите мольную теплоёмкость при температуре Т=298 К, для твёрдого вещества FeSiO2.
Дано: Решение:
Т= 298 К C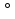 (FeSiO2) = C(Fe) + C(Si) 2*C(O) = 6,3+3,8+ 2*4=18,1
(FeSiO2) = C(Fe) + C(Si) 2*C(O) = 6,3+3,8+ 2*4=18,1 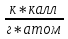
FeSiO2 Ответ: С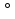 (FeSiO2) = 18,1
(FeSiO2) = 18,1 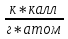
C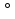 (FeSiO2) = ?
(FeSiO2) = ?
Задача №2:
Определите изобарную теплоёмкость веществ H2 и CO2, при температуре 295 К.
Дано: Решение:
H2 Ср= а + в*Т+ с'*Т-2
CO2 Ср (H2) = 6, 95 - 0, 2 * 10-3 * T +0, 48 * 10-6 * T-2 =
T= 295 К = 6, 95 - 0,2 * 10-3 * 295 + 0, 48 * 10-6 * 295-2 =
Ср(СО2)=? 6, 95 - 0,2 * 10-3 * 295 + 0, 48 * 10-6 * 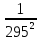 =
=
Ср(Н2)=? 6, 95 - 59 + 0,00552 = -52, 044 * 10-9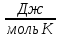
Ср (CO2) = 6, 396 + 10, 1 * 10-3 * 295 - 3,405 * 10-6 *
295-2 = 6, 396 + 10, 1 * 10-3 * 295 - 3,405 * 10-6 * 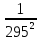 =
=
6, 396 + 2979, 5 - 0, 03912 = 1985, 856 * 10 -9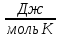
Ответ: Ср (H2) = -52, 044 * 10-9 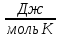 ; Cр (CO2) = 1985, 856 * 10-9
; Cр (CO2) = 1985, 856 * 10-9 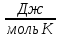
Вывод: Я практически рассчитала мольную и изобарную теплоёмкость.


