- Преподавателю
- Химия
- ОРТА МЕКТЕПТЕ КЕШЕНДІ ҚОСЫЛЫСТАРДЫ ОҚЫТУДЫҢ ЕРЕКШЕЛІКТЕРІ
ОРТА МЕКТЕПТЕ КЕШЕНДІ ҚОСЫЛЫСТАРДЫ ОҚЫТУДЫҢ ЕРЕКШЕЛІКТЕРІ
| Раздел | Химия |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Еспенбетова Ш.О. |
| Дата | 19.05.2014 |
| Формат | docx |
| Изображения | Есть |
ОӘЖ 37.05:367.8:373.854
ОРТА МЕКТЕПТЕ КЕШЕНДІ ҚОСЫЛЫСТАРДЫ ОҚЫТУДЫҢ ЕРЕКШЕЛІКТЕРІ
ТҰРМАХАНОВА Н.А.
Қорқыт Ата атындағы Қызылорда
мемлекеттік университетінің
4-курс студенті
ЕСПЕНБЕТОВА Ш.О.
Қорқыт Ата атындағы Қызылорда
мемлекеттік университеті
Педагогикалық ғалым мен озық тәжірибенің бүгінгі даму деңгейінде белгілі болғандай оқытудың әдіс-тәсілдерінің бәрін де еркін игеріп, әрбір нақтылы жағдайларға орай ең тиімдісін таңдап алу және олардың бірнешеуінің жиынтығын түрлендіре тиімді, үйлесімді әрі шығармашылықпен қолдану - сабақтың сәтті өтуінің кепілі. Осы ретте мына мәселелерге баса назар аударған жөн:
1.Мұғалім сәтсіз өткен сабақтарға өзіндік талдау жасап өз кемшілігін іздеуге әрекет жасау керек.
2.Білім мен тәрбие беруде жариялылық, педагогикалық, ынтымақтастық, ғылыми-әдістемелік, тың ізденістерге сүйене отырып жаңашылдыққа талпыну қажет.
3.Мұғалім күнделікті әр сабағына шығармашылықпен дайындалуы керек. Өйткені, сабақ-мұғалімнің өнері, шығармасы. Сондықтан әр сабақты тиімді ұйымдастыруда оқушыны жалықтырмайтын, қабілетін арттыратын жағдай туғызуға ықпал етуміз керек деп ойлаймыз [1].
Ақпараттық технологияның және химия пәнінің ерекшеліктерін пайдалана отырып сабақты қызықты өткізуге болады. Бұл әдістер тұлғаның химия пәнінен алған білім сапасы мен сауаттылығын кеңейтуге жәрдемдеседі, мысалы: интернет сайты арқылы жоғары деңгейдегі көрнекіліктерді пайдалануға болады. Заман ағымына қарай сабаққа видео, аудио қондырғылары мен теледидарды, компьютерді қолдану оқушыны дүниетанымын кеңейтеді. Әсіресе, оқулықтағы тарауларды қорытындылау кезінде оқушылар қосымша материалдар жинақтап, білімдерін кеңейтіп, танымдық белсенділігін арттырып қана қоймай, қисынды ойлау жүйесін қалыптастырып, шығармашылығын дамытады. Тестік тапсырмалар орындайды. Компьютер көмегімен оқыту оң нәтижелер береді. Ақпараттық мәдениет дегеніміз - тек компьютермен дұрыс жұмыс істей білу ғана емес, кез-келген ақпарат көзін: анықтамаларды, химиялық формулалар, сөздіктерді, теледидар бағдарламаларын т.с.с. дұрыс пайдалана білу деген сөз. Мысалы, бір ғана химиялық формуланың өзінен көп ақпарат алуға болады. Химиялық формула - химиялық тілдің ең маңызды бөлігі болып есептелінеді, себебі сол заттың химиялық құрамын ажыратып береді. Осыған орай химия пәніне арналған бір сабақтың жоспарын ұсынып отырмыз.
Тақырыбы: Кешенді қосылыстар
Сабақтың мақсаты мен міндеттері:
білімділік:
Комплексті қосылыстар жайында білімді қалыптастыру және комплексті қосылыстардың химиялық қасиеттерін қарастыру;
дамытушылық:
Комплексті қосылыстардың алыну жолы мен номенклатурасы жайлы білімді тереңдету;
тәрбиелілік:
Қосылыстың құрамы мен қасиеттері жайлы себеп- салдарлық байланыстың қалыптасуын жалғастыру; оқушылардың танымдық белсенділіктері мен ой өрісін дамыту;
құрал-жабдықтар мен реактивтер:
презентация «Комплексті қосылыстар», демонстрация көрсетілген бейнефрагменттер, шыны таяқша, пробиркалар, штатив.
реактивтер:
аммиак ерітіндісі, тұз қышқылы, мыстың (ІІ) тұзы, натрий гидроксиді, алюминий хлориді, қызыл қан тұзы, сары қан тұзы, темірдің (ІІ) және (ІІІ) тұздары.
сабақтың типі:
жаңа сабақты түсіндіру;
Ұйымдастыру кезеңі
«Отсыз түтін» атты қызықты тәжірибе көрсетіледі, ол үшін (аммиак ерітіндісі мен тұз қышқылы) екі затты бір - біріне қосып аммоний хлориді алынады;
Реакция теңдеуін жазайық:
NH4ОН + HCl = [NH4]Cl + H2O
алынған қосылыс - тұз (аммоний хлориді ) деп аталады, оны комплексті қосылыстар түрінде жазуға болады.
Бүгінгі сабақта мына сұрақтарға жауап беруге тырысамыз.
1.Қандай қосылыстар комплексті қосылыстар деп аталады?
2.Олардың құрамы қандай?
3.Мұндай қосылыстарды қалай алуға болады?
4.Қайда қолданылады?
5.Қандай химиялық қасиет көрсетеді?
6.Берілген қосылыстарды номенклатура бойынша қалай атауға болады?
Комплексті қосылыстар (латынша complexus - үйлесімділік, қамту), немесе координациялық қосылыстар (латынша со - «бірге» және ordinatio - «реттілік») - бөлшектер (бейтарап молекулалар немесе иондар), берілген комплекс түзушіге ионға (немесе атомға) лиганда деп аталатын бейтарап молекуланың немесе басқа ионның қосылу нәтижесінде түзілетін қосылыс.
Комплексті қосылыстардың шығу тарихына тоқталайық: 1871 жылы Д.И.Менделеев комплексті қосылыстар жайлы баяндама жасады. Комплексті қосылыстардың құрылысы жайлы өз көзқарасын білдірді. Әртүрлі қосылыстар (аммиакаттар, кристаллогидраттар, қос тұздар) арасында ұқсастық бар екендігін дәлелдеп, соның нәтижесінде осы заттардың құрылысы жайлы баяндады. Ол: бұл заттардың табиғаты бірдей болады деген мынадай қорытындыға келді. Комплексті қосылыстар орталығында металл атомы орналасады, ал оның айналасы атомдар, молекулалар топтарымен «қоршалады». Бірақ ол орталық металл атомының айналасына қанша атом, молекуланы орналастыруға болады? Бұл сұрақтың жауабын тек қана А.Вернер ғана берді.
Швед ғалымы А.Вернер негізгі және қосымша валенттілік теориясын ұсынды. Осы теория комплексті қосылыстардың алғы шарты болды. Бұл теорияны орыс ғалымдары Л.А.Чугаев, И.И.Черняев және А.А.Гринберг еңбектерінде толықтырды. Координациялық теорияның негізін қалаушы Швед химигі Альфред Вернер болды. 1911 ж. құрамында көміртек атомы кездеспейтін, 40 жуық оптикалық белсенді молекулаларды синтездеді. 1913 г. Вернерге ертеректе өткізген зерттеу нәтижелеріне байланысты Нобель сыйлығы берілді [2].
Комплексті қосылыстар туралы бейне фильм көрсетіледі.
Комплексті қосылыстардың қолданылуы.
1.Полимерлер синтездеуде катализатор ретінде қолданылады;
2.Атмосфералық азотты байланыстыру үшін қолданылады;
3.Синтетикалық жуғыш заттарды алу үшін;
4.Металдар коррозиясымен күресу үшін;
5.Лак пен бояғыш заттарды алу үшін;
6.Гемоглобин - қанға қызыл түс береді;
7.Хлорофилл - өсімдіктерге жасыл түс береді
Комплексті қосылыстардың құрылысы. Қазіргі кезде комплекс қосылыстарындағы химиялық байланысты мына үш түрлі теория түсіндіреді: валенттік байланыс әдісі; кристалл өрісі теориясы; молекулалық орбитальдар әдісі. Бұл теориялар комплекс қосылыстарының құрылысын, қасиетін түсіндіруде бір-бірін толықтырып тұрады.
Валенттік байланыс (ВБ) әдісі негізінде жұп ортақ электрондар көмегімен және көбінесе донорлық-акцепторлық механизм арқылы комплекс иондар түзілетіні анықталды. Осы әдіс көмегімен көптеген комплекс қосылыстарының түзілуі, олардың магниттік қасиеттері, координациялық санның мәні жақсы түсіндіріледі. Осы әдіс арқылы комплекс қосылыстарға түсінікті анықтама берілген [3].
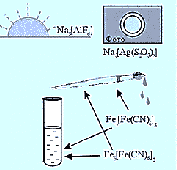
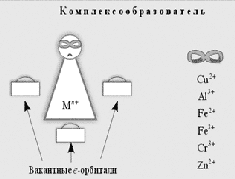
Кристалл өрісі теориясы бойынша комплекс түзуші ион мен лигандалар арасында ионаралық не ион - дипольдік және электрстатискалық тартылыс күштері арқылы байланыс түзіледі. Бұл теория комплекс қосылыстарының оптикалық қасиеттерін жақсы түсіндіреді, ал ковалентті байланысы бар болған кезде қиыншылыққа кезігеді. Молекулалық орбитальдар әдісі комплекс түзуші мен лигандаларды біртұтас алып қарастырады. Комплекстің қасиеті ядролармен электрондардан тұратын жүйе математикалық есептеу жолымен анықталады. Ядролар сыртында электрондар байланыстырушы және босаңдатқыш орбитальдар бойымен атомдық орбитальдардың сызықтық комбинациясы негізінде орналасады. Аяқталмаған d - деңгейшесі бар қосымша топша металдарынан түзілген координациялық қосылыстарда: Валенттік байланыс әдісі (ВБ) донорлық- акцепторлық механизм арқылы комплекс иондар түзілетіні анықталды. Комплексті ионның түзілуі d - металдары үшін s-, p-, d- және f- деңгейшедегі вакантты орбитальдар арқылы түсіндіруге болады. Ішкі комплексті қосылыстарда берік байланыс түзілуі үшін электрондарды жұптастыру арқылы екі d-орбитальді босату тиімді болады. Кобальт атомының бос орбитальдары, аммиак молекуласындағы азот атомдарының бөлінбеген электрон жұптары үшін ваканция болып табылады. Комплексті қосылыстағы ішкі координациялық сфераның түзілуі осылай түзіледі.
Комплексті ион мен комплекс түзушінің зарядын анықтау
Комплексті қосылыс молекуласының заряды болмайды, яғни электробейтарап бөлшек болып табылады.
1. Егер лиганда болып молекула табылатын болса, онда комплексті ионның заряды комплекс түзушінің зарядына тең болады.
2. Егер лиганда болып молекула және ион табылатын болса, онда комплексті ионның заряды комплекс түзуші мен лигандалардың зарядтарының алгебралық қосындысына тең болады.
3. Комплексті ионның заряды арқылы комплекс түзушінің зарядын есептеуге болады.
4. Ол үшін барлық лигандалардың зарядын ескеру қажет:
K3[Fe3+(CN)6]3- (-3)-(-1*6)=-3+6=+3
K4[Fe2+(CN)6]4- (-4)-(-1*6)=-4+6=+2
Комплекс қосылысындағы изомерия. Заттардың сандық және сапалық құрамы бірдей, бірақ қасиеттері әртүрлі болатын құбылысын изомерия деп атайды. Изомерия құбылыс комплекс қосылыстарына тән. Мұндай изомерияны бірнеше түрі кездеседі: геометриялық, оптикалық, гидраттық, ионизациялық және басқа. Геометриялық изомерия комплекс құрамындағы лигандалардың өзара орналасуына байланысты. Егер лигандалар біріне - бірі жақын орналасса - цис, қарама-қарсы орналасса транс изомер болады.
Егер комплекс қосылыста су молекулалары болса, оның ішкі және сыртқы сферада орналасуына қарай әртүрлі гидратты изомерия болады. Комплекс қосылыстарында қышқыл қалдықтарының ішкі және сыртқы сферада орналасуына байланысты ионизациялық изомерия болады [4,5].
Комплексті қосылыстардың жіктелуі: Аквокомплекстер. Олардың құрамындағы лигандалар су молекулалары болады. Кей аквокомплекстер құрамындағы су молекулалары сыртқы сферада болуы мүмкін. Олар кристалданған кезде құрамына су молекулалары да кіреді. Алайда, су молекуласы қыздырғанда бөлініп кетеді.
Ациодокомплекстер. Олардың құрамындағы лигандалар қышқыл қалдықтары болып табылады. Кейбір қышқылдарды комплекс түрінде көрсетуге болады. Гидросокомплекстерді де осы типке қосады.
Аммиакаттар және амминнаттар. Комплекс ион құрамында аммиак не амминдер болады. Аммиандер әртүрлі болады.
Көпядролы комплекстер қосылыстар. Құрамында екі немесе одан да көп бір элемент не әртүрлі элемент комплекс түзуші болып кіреді. Ол комплекс түзушілер бір-бірімен топтар көмегімен байланысады.
Циклді немесе хелат комплекс қосылыстар Ішкі сферада лигандалар цикл түзеді.
Комплексті қосылыстардың химиялық қасиеттері
2K3[Fe(CN)6] + 3FeSO4 = Fe3[Fe(CN)6]2↓ + 3K2SO4
[CoCl2(NH3)4]Cl + AgNO3 = [CoCl2(NH3)4]NO3 + AgCl↓
K4[Fe(CN)6] + 4HCl = H4[Fe(CN)6] + 4KCl
H2[PtCl6] + 2CsOH = Cs2[PtCl6] + 2H2O
Fe4[Fe(CN)6]3 + 12 KOH = 4Fе(OH)3↓ + 3K4[Fe(CN)6]


Сыртқы сфера бойынша комплексті қосылыстардың диссоциациясы
(біріншілік диссоциация)
K3[Fe(CN)6] ↔ 3K+ + [Fe(CN)6]3-
[Ag(NH3)2]Cl ↔ [Ag(NH3)2]+ + Cl-
Қорытынды
• Комплексті қосылыстар - құрамына комплексті иондар кіретін күрделі заттар.
• Комплексті ион - бұл d-металдар мен лигандалардан тұратын иондар.
• Лиганда - d-металмен донорлы-акцепторлы байланыс түзетін комплексті ионның құрамына енетін молекула немесе ион.
• Координациялық сан - комплексті ионның құрамына енетін лигандалар саны.
Үй тапсырмасы
1. Мына төменде берілген қосылыстар үшін қосылыстың ішкі және сыртқы сферасын анықтап, металдың координациялық санын, орталық металл ионының зарядын, комплексті ион зарядын анықтаңдар:
H4 [PtCl 6] [Cu(NH3)2] SO4 [Cr(H2O)6 ]Cl2
2. Егер молекула құрамында мынадай иондар
Ni (+2), 3Cl (-), сонымен қатар молекулы NH3 болса, қосылыстың формуласын құрастырыңдар.
Қолданылған әдебиеттер
1. Ә.Н. Бөрібекова. Химия пәнін оқытуда ақпараттық технологияны пайдалану. Астана қаласы №49 орта мектеп.
2.Н.С. Ахметов. Общая и неорганическая химия. М.: Высшая школа . 2003. С. 107-113.
3.Чернобельская Г.М. Методика обучения химии в средней школе. М.: ВЛАДОС, 2000.
4.Учебная программа по дисциплине «Общая и неорганическая химия». 2001. 19 с.
5.М.И. Сафарова. Общая и неорганическая химия в схемах и таблицах. Ч.1. Теоретические основы неорганической химии. Учебное пособие. Саратов. СВИРХБЗ. 2006. С. 80.
Резюме
В данной статье автором был рассмотрен актуальные проблемы инновационных технологии в процессе обучения химии в средней школе. В статье аргументировано, обоснованы преимущества инновационного подхода в сравнении с традиционными формами обучения школьников. Предложен оптимизация современных методов обучения и внедрение их в образовательный процесс.
Summary
In this article the author was considered topical issues of innovative technology in teaching chemistry in high school. The article argued, justified the benefits of innovative approach in comparison with traditional forms of student learning. Optimization of modern teaching methods and their implementation in the educational process.


