- Преподавателю
- Химия
- Алканы. Гомологический ряд алканов. Номенклатура и изомерия алканов
Алканы. Гомологический ряд алканов. Номенклатура и изомерия алканов
| Раздел | Химия |
| Класс | - |
| Тип | Рабочие программы |
| Автор | Мукатаев К.Т. |
| Дата | 02.12.2014 |
| Формат | docx |
| Изображения | Есть |
Дата: ____________
11-11
Алканы. Гомологический ряд алканов. Номенклатура и изомерия алканов
ТЕМА
ЦЕЛЬ
Дать учащимся понятие о предельных углеводородах, их химическом, пространственном и электронном строении. Ознакомить с понятием гомологии, правилами названия веществ и составления формул по современной номенклатуре. Продолжить формирование мировоззренческих понятий: о познаваемости природы, причинно-следственной зависимости между составом, строением, свойствами и применением предельных углеводородов.
СОДЕРЖАНИЕ
Гомологический ряд алканов и их строение
ТЕРМИНЫ
Алкан , гомологи, изомеры
ХИМ ЭКСПЕРИМЕНТ
-
ОБОРУДОВАНИЕ
Интерактивная доска
ДОМ ЗАДАНИЕ
§3.1 пересказ, №3,4,6,8 стр. 67
ПЛАН УРОКА.
Опрос домашнего задания. Актуализация знаний
-
Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы - углеводороды в молекулах которых все атомы углерода связаны одинарными связями (-) и имеют общую формулу:
CnH2n+2 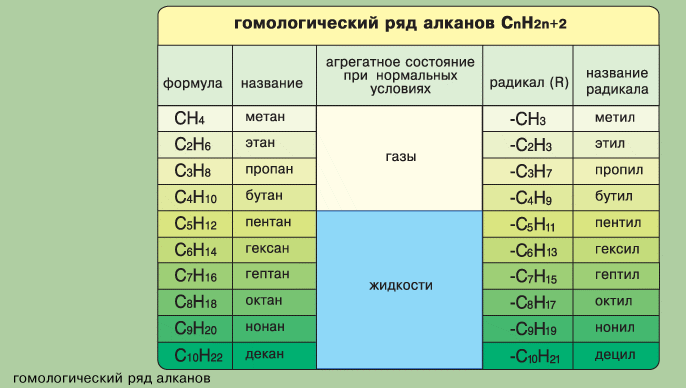
-
Что такое гомологи? (учащиеся отвечают на данный вопрос)
Гомологический ряд алканов
Алканы, имея общую формулу СnH2n+2, представляют собой ряд родственных соединений с однотипной структурой, в котором каждый последующий член отличается от предыдущего на постоянную группу атомов (-CH2-). Такая последовательность соединений называется гомологическим рядом (от греч. homolog - сходный), отдельные члены этого ряда - гомологами, а группа атомов, на которую различаются соседние гомологи, - гомологической разностью.
Гомологический ряд алканов легко составить, прибавляя каждый раз к предыдущей цепочке новый атом углерода и дополняя его оставшиеся валентности до 4-х атомами водорода. Другой вариант - добавление в цепь группы -СН2-:
CH4 или Н-СН2-Н - первый член гомологического ряда - метан
(содержит 1 атом углерода);
CH3-CH3 или Н-СН2-СН2-Н - 2-й гомолог - этан (2 атома С);
CH3-CH2-CH3 или Н-СН2-СН2-СН2-Н - 3-й гомолог - пропан (3 атома С);
CH3-CH2-CH2-CH3 или Н-СН2-СН2-СН2-СН2-Н - бутан (4 атома С)
Суффикс -ан является характерным для названия всех алканов. Начиная с пятого гомолога, название алкана образуется из греческого числительного, указывающего число атомов углерода в молекуле, и суффикса -ан: пентан С5Н12, гексан С6Н14, гептан С7Н16, октан С8Н18, нонан С9Н20, декан С10Н22 и т.д.
-
Виды изомерии для алканов:
Изомерия - явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение. Такие соединения называются изомерами.
Различия в порядке соединения атомов в молекулах (т. е. в химическом строении) приводят к структурной изомерии. Строение структурных изомеров отражается структурными формулами. В ряду алканов структурная изомерия проявляется при содержании в цепи 4-х и более атомов углерода, т. е. начиная с бутана С4Н10. Если в молекулах одинакового состава и одинакового химического строения возможно различное взаимное расположение атомов в пространстве, то наблюдается пространственная изомерия (стереоизомерия). В этом случае использование структурных формул недостаточно и следует применять модели молекул или пространственные (стереохимические) формулы. Алканы, начиная с этана С2Н6, существуют в различных пространственных формах, обусловленных внутримолекулярным вращением по s-связям С-С, и проявляют так называемую поворотную изомерию.
Кроме того, при наличии в молекуле 7-ми и более углеродных атомов, возможен еще один вид пространственной изомерии, когда два изомера относятся друг к другу как предмет и его зеркальное изображение (подобно тому, как левая рука относится к правой).
Такие различия в строении молекул называют зеркальной или оптической изомерией.
-
Алгоритм.
-
1. Выбор главной цепи:
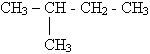
2. Нумерация атомов главной цепи:
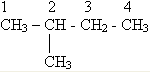
3. Формирование названия:
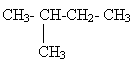
2 - метилбутан
-
Строение алканов.
Атом углерода во всех органических веществах находится в "возбуждённом" состоянии, т. е. Имеет на внешнем уровне четыре неспаренных электрона.
Каждое электронное облако обладает запасом энергии: s- облако имеет менший запас энергии, чем р-облако, в атоме углерода они находятся в разных энергетических состояниях. Поэтому при образовании химической связи происходит гибридизация, т. е. выравнивание электронных облаков по запасу энергии. Это отображается наформе и направленности облаков, происходит перестройка (пространственная) электронных облаков.
В результате sp3 - гибридизации все четыре валентных электронных облака гибридизованы: валентный угол между этими осями гибридизованных облаков 109° 28', поэтому молекулы имеют пространственную тетраэдрическую форму, форма углеродных цепей зигзагообразна; атомы углерода не находятся на одной прямой, т. к. при вращении атомов валентные углы остаются прежними.
Все органические вещества построены в основном за счёт ковалентных связей. Углерод - углеродные и углерод - водородные связи относятся к сигма - связям - это связь, образующаяся при перекрывании атомных орбиталей по линии, проходящей через ядра атомов. Возможно вращение вокруг сигма - связей, поскольку эта связь имеет осевую симметрию.
Для закрепления материала ответить на вопросы в конце параграфа, а также выполнить задания по задачнику
Домашнее задание: §3.1 пересказ, №3,4,6,8 стр. 67


