- Преподавателю
- Химия
- Интегрированный урок по химии на темуКислород. Оксиды. Горение. (8 класс)
Интегрированный урок по химии на темуКислород. Оксиды. Горение. (8 класс)
| Раздел | Химия |
| Класс | 8 класс |
| Тип | Конспекты |
| Автор | Муратова З.Р. |
| Дата | 18.10.2015 |
| Формат | docx |
| Изображения | Есть |
Северная общеобразовательная школа
Щербактинского района
Павлодарской области
ИНТЕГРИРОВАННЫЙ УРОК ХИМИИ
Разработал урок
учитель химии и биологии 1 категории
Муратова Зульфия Рашитовна
Павлодар, 2015
8 класс. Тема: «Горение, окисление. Оксиды».
Цель: 1. Сформировать химические понятия и сведения об окислении веществ, оксидах. Изучить горение веществ в кислороде. Научить составлять уравнения реакций окисления, уметь делать выводы из полученных химических знаний. Научить учащихся проводить наблюдения, объяснять явления с научной точки зрения, анализировать и толковать данные на научной основе, используя химические термины и методы сравнения, показать свою мыслительную способность, умение разделять главный вопрос на отдельные составляющие. Развить умение использовать знания других предметов, связав их в решении проблем, связанных с жизненной ситуацией.
2. Научить легко оперировать предложенным дидактическим материалом и его компонентами, разворачивать и сворачивать информацию, представлять её графически в виде опорных схем, структурно-логическихтблиц. Самостоятельно актуализировать базовые знания на основе вопросов перед изучаемой темой.
3. Воспитывать чувство ответственного отношения к изучаемому материалу на основе формирования представлений о значимости естественнонаучных знаний. Воспитывать бережное отношение к природным веществам к природным явлениям. Показать единство, взаимаосвязь и многообразие веществ. Активизировать работу учащихся стратегиями активного обучения.
Оборудование:простые вещества: уголь, сера, железо, спиртовка, лабораторная посуда. Рисунки, схемы, таблицы, учебник.
План урока.
1.Организационный момент.
2. Вводный этап урока - проверка домашнего задания (игровая форма работы)
3. Усвоение новых знаний. (беседа, демонстрация)
4. Первичное закрепление темы. (работа в группах, с схемами, рисунками, карточками, учебником)
5. Вторичное закрепление. ( тест)
6 Заключение. (итоги урока, домашнее задание)
7.Рефлексия.
I. Организационный этап.
Добрый день, ребята! Сегодня мы продолжим разговор о кислороде и изучим горение, окисление веществ с образованием оксидов. Вам предстоит выполнить несколько упражнений и заданий.
II. Вводный этап урока - проверка домашнего задания (игровая форма работы)
А какие понятия всплывают при изучении данной темы? (Примерные ответы уч-ся: простое, сложное вещество, кислород, его применение, получение, свойства, и т.д.)
Я предлагаю вам выполнить задание.
Для этого вам розданы листочки с 25 предложениями. Вы читаете предложения, и если они подходят к кислороду, то соответствующую цифру обведите кружочком. Выполняете попарно с товарищем по парте. И проверять задание будем в игре «Автобус».
Игра «Автобус».
Каждая пара за партой - это пассажиры, постоянно находящиеся в движении. Ответ произносится вслух по цепочке «пассажирами» первой парты и если он верный пассажиры по сигналу учителя делают шаг вперёд на одну парту по маршруту (проверка домашнего задания).
Текст на соответствие - О2
В промышленности получают из воздуха.
Хорошо растворим в воде.
Взаимодействует с простыми и сложными веществами.
Применяют в качестве топлива.
Сложное вещество.
При обычных условиях - бесцветный газ.
Собирают вытеснением воздуха.
В природе встречается только в связанном виде.
Принимает участие в процессах окисления.
Собирают в перевёрнутый вверх дном сосуд.
Простое вещество.
В лаборатории получают из «марганцовки».
Малорастворим в воде.
Газ, имеющий запах.
Разлагается при нагревании.
Поддерживает горение.
При t = -1830С превращается в жидкость.
Входит в состав минералов, горных пород, песка, воды.
Легче воздуха.
Получают из природного газа.
Применяют для сварки и резки металлов, материалов.
При обычных условиях - жидкость.
Входит в состав воздуха.
Собирают в сосуд, поставленный на дно.
Необходим для дыхания.
III. Усвоение новых знаний. (беседа, демонстрация)
Эксперимент. Перед вами процесс горения свечи. Что вы можете сказать о строении пламени? Чем отличаются зоны пламени? (экспериментальное подтверждение ответа: спичка загорается быстрее во внешней зоне пламени).
- Почему средняя часть пламени ярко светится?
- О чём это говорит? (Фарфоровая чашка вносится в среднюю часть пламени и покрывается копотью).
Вещество, содержащееся в воздухе крупных городов в виде частиц копоти и сажи, и вещество, присутствующее в средней части пламени, придающее пламени красоту и жизнь, - одно и тоже. Как прекрасен этот процесс, при котором такое невзрачное вещество, как уголь, делается таким сияющим!
Что же такое реакция горения?
Опыт: нальём в фарфоровую чашку немного спирта, подожжем его, а затем плотно прикроем листом картона.
Вопрос: почему пламя гаснет, а бумага не горит?
Какие же вещества могут гореть? В кислороде могут гореть такие вещества, которые обычно считаются негорючими, например железо. (демонстрация горения угля, фосфора, серы, железа).
Сравнение процессов горения и дыхания.
Для горения свечи, так же как и для дыхания, необходим кислород и образуются те же продукты реакции: СО2, Н2О +Q. При окислении пищи в организме также выделяется энергия.
Игра «Лото». (в группах)
В группах учащимся предлагается составить и озвучить химические реакции горения (из отдельных карточек в мешочке лото). Задания в мешочке: горение, железа, фосфора, серы, угля).
Какая это реакция?
IV. Этап закрепления знаний.
Перед вами «волшебный цветок». На его лепестках напишите формулы оксидов и назовите их.




Рис. 1. Игра «Волшебный цветок»
По желанию уч-ся выходят к доске и записывают формулы оксидов. Дают им названия.
Остальные уч-ся работают в тетрадях.
- По какому признаку вы определили оксиды?
- Каким образом можно систематизировать данные оксиды?
Ребята, сейчас мы должны разгадать тайну «магических колец». (к магнитной доске прикрепляются «магические кольца»)

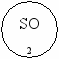

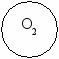

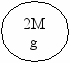
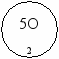


Игра «Магические кольца»
Впишите в кольца отсутствующие формулы веществ с необходимыми индексами и коэффициентами, составьте уравнения реакций.
Задания уч-ся выполняют по группам (кто быстрее), затем озвучивают уравнения химических реакций.
А сейчас откройте учебники и выполните задание 5 стр. 63.
Закончите уравнения приведенных ниже реакций, расставьте коэфициенты.
СuS + O2 = Сu + ?
H2S + O2 = S O2 + ?
Взаимопроверка. Вслух зачитываются уравнения.
Интегрированное задание. (Задание в группах).
В среднем 1 га леса за вегетационный период выделяет 5 т кислорода, поглощает 6-7 т углекислого газа. Но в связи с загрязнением воздуха и большими темпами потребления кислорода возобновление кислорода отстаёт от использования. Что для этого надо предпринять?
(Свободно-конструируемый ответ)
V. Вторичное закрепление. Тестирование.
-
Из перечисленных веществсложным не является
а) кислород;
б) вода;
в) сульфид железа;
г) поваренная соль. -
Кислород можно распознать
Варианты ответов
да
нет
лакмусом
по запаху
известковой водой
тлеющей лучинкой
-
Сопоставь названия оксидов с их формулами
Оксид фосфора
Cu O
оксид железа
P2 O5
Оксид магния
Fe 2O3
Оксид меди
Mg O
-
Вставь пропущенные слова.
В обычных условиях кислород в … виде, необходим живым существам для…, в природе входит в состав …, в лаборатории его получают из …, взаимодействует с простыми веществами с образованием …, таким образом возникает реакция…
-
Для чего тяжелобольному в отделении реанимации подают кислород?
VI. Подведение итогов. Оценка деятельности класса.
Домашнее задание.
VII. Рефлексия.Пришлите мне SMS-ку.
SMS
-
Спасибо за….
-
Я узнал…
-
Хорошо, что…
-
Мне понравилось…
-
Наконец-то…
-
Меня удивило…
Урок я хочу закончить словами великого английского учёного Майкла Фарадея, исследовавшего явления, связанные с горением свечи: «Я могу только выразить вам своё пожелание, чтобы вы могли с честью выдержать сравнение со свечой, т.е. могли бы быть светочем для окружающих, и чтобы во всехваших действиях вы подражали красоте пламени, честно и производственно выполняя свой долг перед человечеством».


