- Преподавателю
- Химия
- Алгоэвристическая программа на тему Кислород
Алгоэвристическая программа на тему Кислород
| Раздел | Химия |
| Класс | 8 класс |
| Тип | Рабочие программы |
| Автор | Шаль О.В. |
| Дата | 03.01.2016 |
| Формат | doc |
| Изображения | Есть |
Алгоэвристическая программа
Д орогой друг,тебе предоставляетсяуникальная возможность изучить самостоятельно тему,а какая тема,ты узнаешь,
орогой друг,тебе предоставляетсяуникальная возможность изучить самостоятельно тему,а какая тема,ты узнаешь,
посмотрев на картинку!

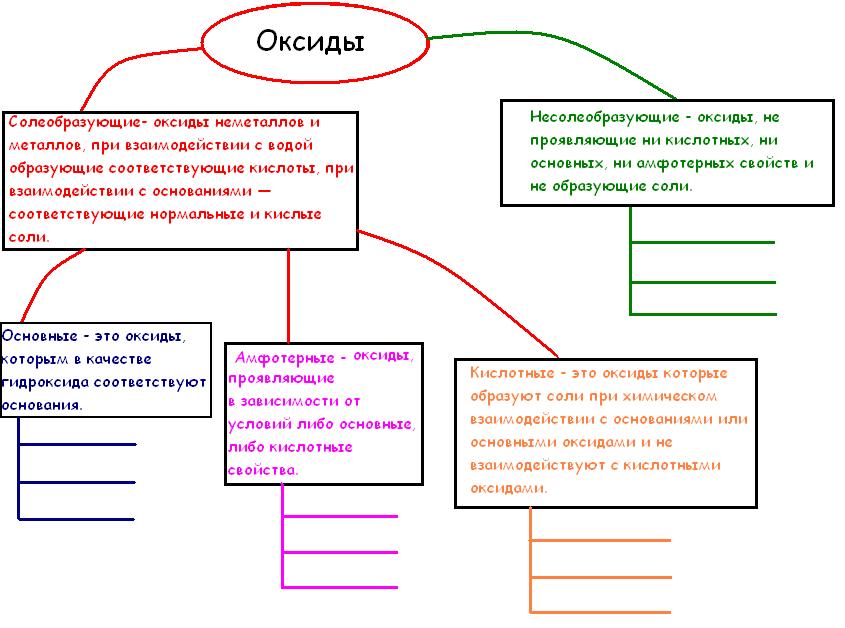
Классификация оксидов, их названия и способы получения.

Немного истории…
ОКСИДЫ или ОКСИЛЫ норо-лат.,
от греч. oxys - кислый
В начале XIX века и
ранее тугоплавкие,
практически
не растворимые в воде
оксиды химики называли
«землями»
Открытие Монооксид углерода -CO
Монооксид углерода был впервые получен французским
химиком Жаком де Лассоном в 1776 при нагревании
оксида цинка с углём, но первоначально его ошибочно
приняли за водород, так как он сгорал синим пламенем.
То, что в состав этого газа входит углерод и кислород,
выяснил в 1800 английский химик Вильям Крукшэнк.
Монооксид углерода вне атмосферы Земли впервые был
обнаружен бельгийским ученым М. Мижотом (M. Migeotte)
в 1949 году по наличию основной колебательно-
вращательной полосы в ИК спектре Солнца.
-
В
 ыберите из предложенных соединений оксиды: (подчеркните правильный вариант)
ыберите из предложенных соединений оксиды: (подчеркните правильный вариант)
NaOH HCl CuO MgSO4
CO2 ZnS Al2O3 NaCl
-
Сформулируйте определение оксиды:
 Оксиды - _____ соединения,
Оксиды - _____ соединения,
состоящие из ___ элементов,
одним из которых является
_______.
-
Классификация оксидов
Соотнесите правильно предложенные оксиды, по их классификации:
О ксиды: SO3, MgO, Al2O3,
ксиды: SO3, MgO, Al2O3,
N2O, ZnO, CO2, NO, Fe2O3,
CaO, MnО2, CO, BaO
-
Названия оксидов
Р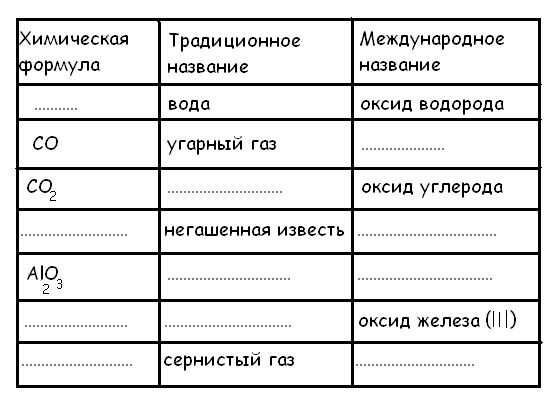 асставьте недостающие элементы, заполните таблицу:
асставьте недостающие элементы, заполните таблицу:



-
Способы получения оксидов
Оксиды образуются при взаимодействии простых и сложных веществ с кислородом, при разложении нерастворимых оснований и солей.

а) Напишите формулы
образовавшихся оксидов.
б) Дайте им названия.
в) Напишите самостоятельно
примеры получения оксидов.
-
Взаимодействие простых веществ с кислородом:
C + O2 ____
+ O2 ____
_ ___+ О2 ____
___+ О2 ____
-
Горение сложных веществ:
C H4 + O2 ____+____
H4 + O2 ____+____
_ ___+O2____ ____+____
___+O2____ ____+____
-
Разложение нерастворимых оснований:
Cu(OH)2 = ____+____
____=____+____
-
Какие еще способы получения оксидов Вы знаете? Приведите примеры, напишите уравнения реакций.
-
А
 знаете ли вы…..
знаете ли вы…..
В 1992 году на одном из крупнейших производителей окcида ртути(II), заводе Алтайхимпром рабочими по заказу неизвестных было похищено 3 мешка этого вещества. Заказчики полагали, что это и есть та самая "красная ртуть", вымышленного вещества, которому часто приписывались свойства вроде огромной плотности, радиоактивности, и высокой токсичности, которое используется не то в «детонаторе термоядерной бомбы», не то в гаусс-пушках, не то в «сверхмощных военных лазерах.
1992 году на одном из крупнейших производителей окcида ртути(II), заводе Алтайхимпром рабочими по заказу неизвестных было похищено 3 мешка этого вещества. Заказчики полагали, что это и есть та самая "красная ртуть", вымышленного вещества, которому часто приписывались свойства вроде огромной плотности, радиоактивности, и высокой токсичности, которое используется не то в «детонаторе термоядерной бомбы», не то в гаусс-пушках, не то в «сверхмощных военных лазерах.
Оксид железа Fe2O3 в составе гематита придаёт марсианской поверхности красноватый оттенок.


Поздравляю!!!
Ты самостоятельно изучил тему!




