- Преподавателю
- Химия
- В удивительном мире углеводородов
В удивительном мире углеводородов
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Грацианова Е.А. |
| Дата | 04.05.2015 |
| Формат | doc |
| Изображения | Есть |
Cеминар на тему «В мире углеводородов»
Цели урока: обучение, развитие, воспитание. Проверить качество усвоения учебного материала, стимулировать познавательную активность учащихся, реализуя межпредметные связи курсов химии, биологии, истории, экологии; формировать умение выделять существенные признаки и свойства, развивать умение классифицировать факты, делать обобщающие выводы, применять знания на практике; развивать память, внимание, эрудицию, умение работать с дополнительной литературой, логически рассуждать, воспитывать чувство сопричастности к общему делу, умение работать в коллективе.
Оборудование и реактивы: коллекции «Нефть и нефтепродукты», «Каменный уголь», схема промышленного применения бензола, компьютер, проектор; штатив с пробирками, стакан с водой, стакан со свечей, спички, лучина, карбид кальция, смесь для получения этилена, реактив Толленса, раствор известковой воды.
Девиз: «Мощь и сила науки - во множестве фактов, цель - в обобщении этого множества» (Д.И.Менделеев)
Ход урока.
-
Вниманию учащихся представляются интригующие вопросы:
-
использование современной международной номенклатуры для названия сложных веществ по составу;
-
умение определять окислитель и восстановитель при написании уравнений реакций органического синтеза методом полуреакций;
-
доказать экспериментально как различить на конкретном примере алкен от алкина;
-
обосновать противоречивость химических свойств пестицидов.
-
что интересного за страницами учебника можно встретить о строении атома углерода.
-
-
Класс делится на две группы для работы с дифференцированными программами уровней «А» и «B» (по выбору учащихся с последующим самоконтролем). Программа «А» - это усложненный вариант заданий в отличие от программы «В».
Разминка. Хронология значимости ученых в химии.
Программа «А».
1. Кто ввёл в химию термин «изомерия», «органические вещества»? Шведский ученый Иене Якоб Берцелиус (1779-1848гг.)
2. Кто осуществил реакцию, которая позволит увеличить углеродный скелет молекул алканов?
Французский химик, член Парижской академии наук Шарль Адольф Вюрц в 1885 г
3. Кто назвал пяти- и шестичленные циклоалканы нафтенами?
Русский химик-органик Владимир Васильевич Марковников (1837-1904гг.)
4. Кто первый получил из светильного газа бензол?
Английский ученый Майкл Фарадей (1791-1867гг.) В 1825г. он исследовал побочные продукты коксования каменного угля и выделил из светильного газа бензол, который назвал «газойлем», «газовым маслом».
5. Назовите лауреата Нобелевской премии, создавшего теорию цепных реакций.
Академик Николай Николаевич Семенов (1896-1986гг.) В 1956г. получил Нобелевскую премию; внес большой вклад в изучение механизма цепных реакций.
6. Кто предложил гипотезу гибридизации электронных облаков атома углерода в момент его возбуждения?
Американский химик Лайнус Полинг в 30-е годы XX в.
Программа «В».
1. Назовите создателя теории строения органических веществ. Александр Михайлович Бутлеров (1828-1836гг.) В 1861 г. впервые выступил с сообщением « О химическом строении веществ».
2. Какой учёный установил, что в реакции гомологов этилена с галогеноводородами водород присоединяется к более гидрированному атому углерода при двойной связи?
Русский химик-органик Владимир Васильевич Марковников (1837-1904гг.)
3. Имя какого учёного носит реакция между алканами и азотной кислотой?
Русского химика-органика Михаила Ивановича Коновалова (1858-1906гг.)
4. Кто был победителем международного конкурса на получение синтетического бутадиенового каучука?
Русский химик, академик Сергей Васильевич Лебедев (1874-1934гг.) Впервые в 1910 году получил образец синтетического бутадиенового каучука.
5. Какой учёный предложил первую структурную формулу бензола в виде карбоциклического сопряженного шестиугольника?
Немецкий химик-органик Фридрих Август Кекуле (1829-1896гг.) В 1865 г. предложил циклическую структурную формулу бензола, распространив тем самым теорию химического строения Бутлерова на ароматические соединения.
6. Кто использовал соли ртути, исследуя свойства ацетилена? Что он получил в результате этой реакции?
Русский химик-органик Михаил Григорьевич Кучеров (1850-1911гг.) В 1881 г. открыл реакцию каталитической гидратации ацетиленовых углеводородов с образованием карбонилсодержащих соединений, в частности, превращения ацетилена в уксусный альдегид в присутствии солей ртути (реакция Кучерова).
Изучение гомологических рядов и изомеров по классам.
Программа «А».
1. Как называется международная номенклатура химических соединений?
Современная международная номенклатура, функционирует с 1957г. 2. Вещества каких гомологических рядов при одинаковом числе атомов в молекулах изомерны друг другу? Какие вещества называются изомерами? Составьте структурные формулы веществ (по одному примеру), которые являются изомерами внутригрупповой (межклассовой) изомерии.
CnH2n алкены CnH2n-2 алкины
CnH2n цикланы CnH2n-2 диены
3. Назовите вещества, укажите к каким гомологическим рядам они относятся.
а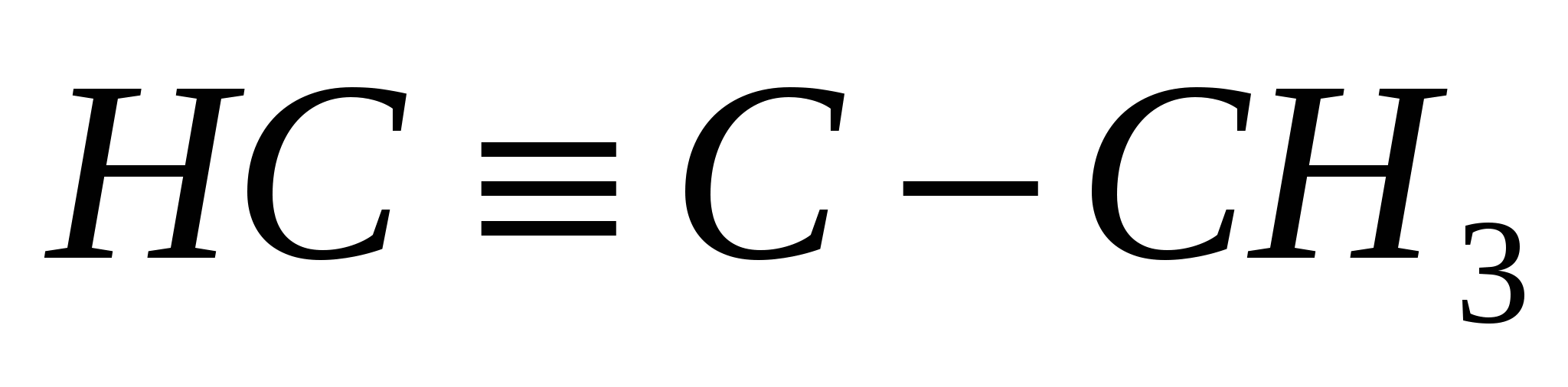 )С11Н24 б)С6Н6 в)СН3-СН=СН-СН3 г)
)С11Н24 б)С6Н6 в)СН3-СН=СН-СН3 г)
д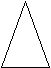
-СН-СН3)СН2=СН-СН=СН2 е)
а)Ундекан (алкан),б) бензол (арен), в)бутен - 2 (алкен), г)пропин-1(алкин), д)бутадиен-1,3(диен),е) метилциклопропан (циклопарафин)
4. Назовите вещества по современной международной номенклатуре:
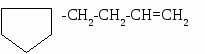
 а) б)
а) б)
а) 5-винилгептадиен-1,3-ин-6 Б) 4-циклопентил-бутен-1
Программа «В»
-
Как сокращенно называют организацию, предложившую правила этой номенклатуры?
ИЮПАК или IUPAC (Международный союз теоретической и прикладной химии).
2. Приведите общие формулы известных вам гомологических рядов углеводородов. Какие вещества называются гомологами? Для каждого класса углеводородов укажите пару веществ, которые являются по отношению к друг другу гомологами.
СnH2n+2 CnH2n CnH2n-2 CnH2n-6
Алканы алкены диены арены
цикланы алкины
Изучение химических свойств углеводородов по классам.
Программа «А»
1. Что происходит с веществами при химических реакциях с позиции атомно-молекулярного учения? С позиции учения о химической связи?
При химических реакциях молекулы разрушаются, атомы - сохраняются, разрыв химической связи - это процесс, обратный ее образованию.
2. Какие химические реакции характерны для:
а) алканов; б) алкенов; в) алкинов; г) аренов.
Каковы механизмы протекания этих реакций?
3. Составить схемы трёх стадий развития реакции между метаном и хлором, протекающей с обрывом цепи:
а) инициирование цепи
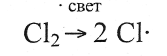
б) развитие цепи
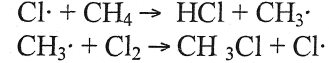
в) обрыв цепи
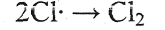
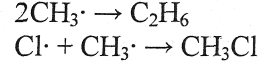
4. Составьте схемы стадий развития реакции между хлороводородом и пропиленом, протекающей по механизму электрофильного присоединения.
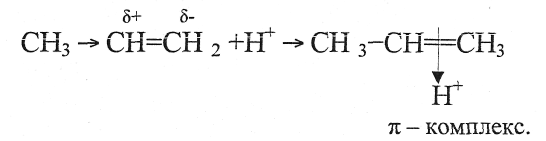
Промежуточная частица называется π-комплексом. При этом π -комплекс превращается в карбокатион - частицу с положительным зарядом на атоме углерода.
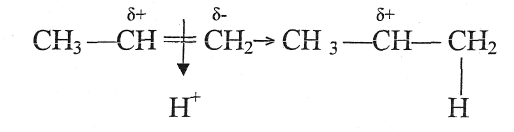
На заключительной стадии карбокатион присоединяет бромид-анион
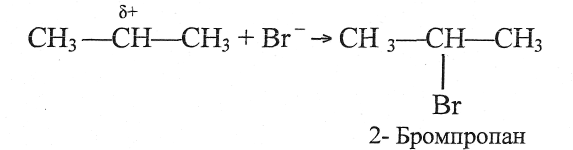
5. В чем выражается взаимное влияние атомов в молекуле толуола? Какие реакции подтверждают это влияние?
СН3
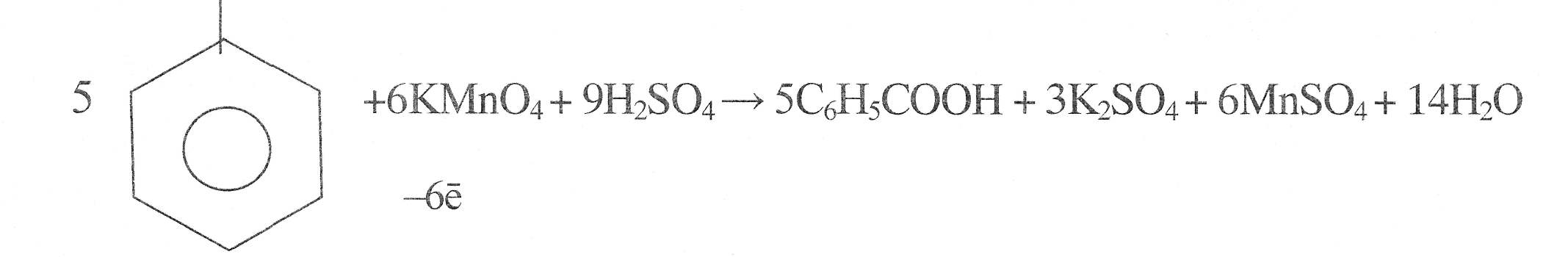

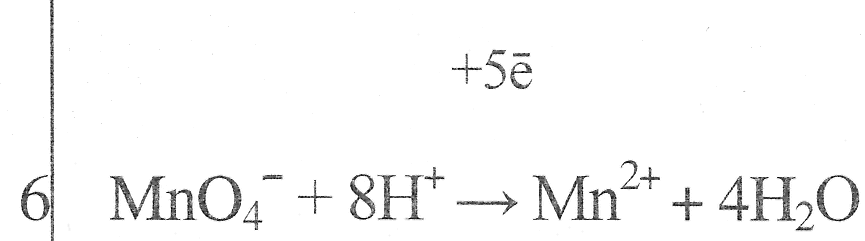
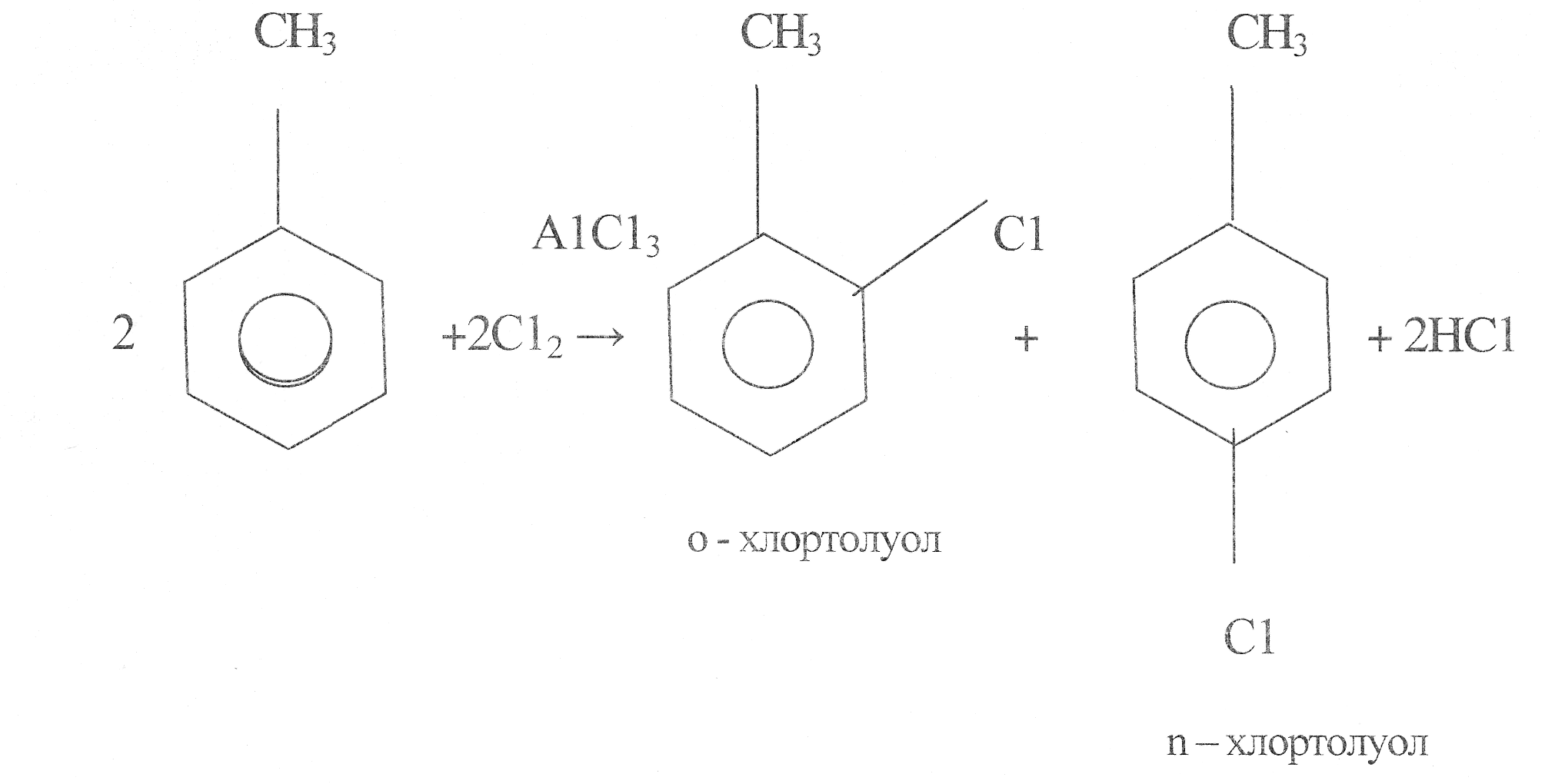
Алкильный заместитель не только активирует ядро, но и направляет вновь входящий заместитель в орто- и пара- положение цикла.
Заместители такого типа называют ориентами первого рода.
6. Записать уравнение реакции окисления пропилена раствором КМпО4 в нейтральной среде. Определите коэффициент перед окислителем.
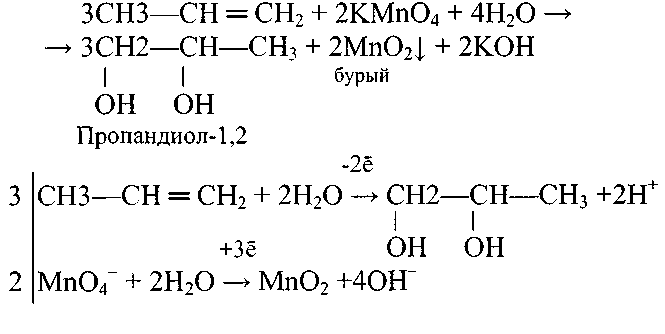
Коэффициент перед окислителем равен 2.
7. Запишите уравнение реакции окисления пропилена с подкисленным раствором перманганата калия. Определите коэффициент перед восстановителем.
СН3-СН=СН2+2KMnO4+3H2SO4 → CO2+CH3COOH+ K2SO4+2MnSO4+ +4H2O
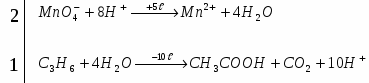
Коэффициент перед восстановителем равен 1.
Программа «В»
1. Что называют химическими реакциями?
Превращение одних веществ в другие.
2. Какие виды разрыва химической связи в веществах вы знаете?
Гомолитический, гетеролитический
3. На примере пропена-1 объясните правило В.В.Марковникова.
СН2=СН-СН3+HCl→СН3-СHCl-CH3
Водород присоединяется к наиболее гидрогенизированному из ненасыщенных атомов углерода, а галоген - к другому.
4. Напишите уравнение реакции нуклеофильного замещения для хлорметана.
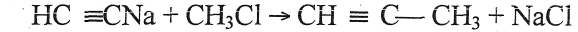
Эта реакция представляет собой пример нуклеофильного замещения, а нуклеофилом в ней является ацетилидный карбанион (дикарбид-ион)
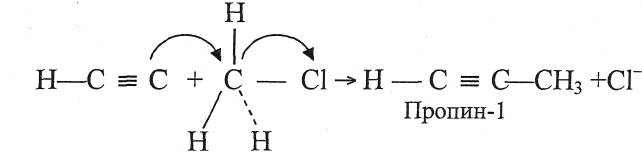
С помощью химического эксперимента установите качественный состав углеводородов, взяв парафин, и различите алкены от алкинов на примере этилена и ацетилена.
Опыт 1. Качественное определение углерода и водорода в органическом веществе.
В широкий химический стакан поместите небольшой кусочек парафиновой свечи и подожгите ее с помощью горящей лучины. Что наблюдаете? Объясните наблюдения.
Погасите свечу и выньте ее из стакана. Влейте в стакан немного известковой воды и осторожно взболтайте. Что наблюдаете? Объясните наблюдения.
На стенках стакана появляются капельки воды. Известковая вода мутнеет. Таким образом, парафин состоит из атомов углерода и водорода, о чем свидетельствуют образовавшиеся продукты.
2С18H38+55O2→36CO2↑+38H2O
CO2+Ca(OH)2→CaCO3↓+H2O
Какие качественные реакции характерны для непредельных углеводоров?
Взаимодействие с растворами бромной воды и перманганата калия.
Что происходит с растворами бромной воды и перманганата калия при пропускании через них газов этилена и ацетилена?
Они быстро обесцвечиваются.
Опыт 2. Докажите экспериментально как можно различить алкены от алкинов на примере этилена и ацетилена.
а) Поместите в пробирку небольшой кусочек карбида кальция и прилейте 2 мл воды. Быстро закройте отверстие пробирки пробкой с газоотводной трубкой. Выделяющийся газ пропустите через реактив Толленса. Что наблюдаете? Объясните наблюдения.
СaC2+2H2O→C2H2↑+Ca(OH)2

ацетиленид
серебра
Идет образование серого осадка.
б) Соберите прибор для получения этилена. В пробирку поместите 3 мл смеси для получения этилена и несколько крупинок пемзы. Закройте пробирку пробкой с газоотводной трубкой и нагрейте в пламени спиртовки. Выделяющийся газ пропустите через реактив Толленса. Что наблюдаете? Объясните наблюдения.
H2SO4(конц.)
C
>1400C 2H5OH C2H4↑+H2O
2H5OH C2H4↑+H2O
С H2=CH2+[Ag(NH3)2]OH→
H2=CH2+[Ag(NH3)2]OH→
При пропускании этилена через реактив Толленса визуальных изменений не происходит.
Роль Д.И.Менделеева для развития химической промышленности.
Программа «А»
1. Что означает слово «генезис»?
Происхождение, процесс возникновения и развития.
2. Расскажите о двух точках зрения на происхождение нефти.
а)Неорганическая теория происхождения нефти, «карбидная» гипотеза (Д.И.Менделеев, 1887г): Нефть - это продукт гидролиза различных карбидов железа FeC,Fe2C, Fe3C и т.д., например,
2FeС+3Н2O→Fe2O3+C2H6
б)органическая теория происхождения нефти (Н.Д.Зелинский, М.В.Ломоносов):Нефть - это превращение продуктов жизнедеятельности флоры и фауны, погребенных в осадочных породах в результате: 1) микробиологического гидролиза углеводов, белков, жиров; 2) термокаталитического преобразования жирных кислот, спиртов, кетонов и т.п. в углеводороды.
3. Почему Д.И.Менделеев осуждал сжигание попутных нефтяных газов, эмоционально высказываясь: «Топить можно и ассигнациями».
В каждой капле нефти содержится более 900 различных химических соединений, более половины химических элементов периодической системы. Это чудо природы является основой нефтехимической промышленности; 90% всей добываемой нефти используется в качестве топлива; 10% нефти идет на нефтехимический синтез.
4. Каков состав нефти?
В нефти, добываемой из разных месторождений, содержатся как углеводороды нормального строения, так и их изомеры. Кроме углеводородов, нефть содержит кислородные, сернистые и азотистые органические соединения. Состав нефти различных месторождений различен.Так, нефти Татарии и Западной Украины содержат преимущественно алканы, нефть Азербайджана богата аренами, а нефть Америки и Саудовской Аравии - циклопарафинами. По преобладанию того или иного класса углеводородов нефтехимики подразделяют нефти на метановые, нафтеновые, ароматические.
Программа «В»
1. Назвать два основных направления переработки каменного угля.
Коксование, газификация
2. Какую идею выдвинул Д.И.Менделеев в 1888 году?
О подземной газификации углей
3. Запишите уравнение реакции в общем виде угля с водородом. Где используют смеси полученных углеводородов?
0C,p
nC+(n+1)H2→CnH2n+2
В качестве топлива для двигателей внутреннего сгорания вместо продуктов нефтепереработки.
Использование схем для усвоения знаний по химическим реакциям.
Программа «А»
1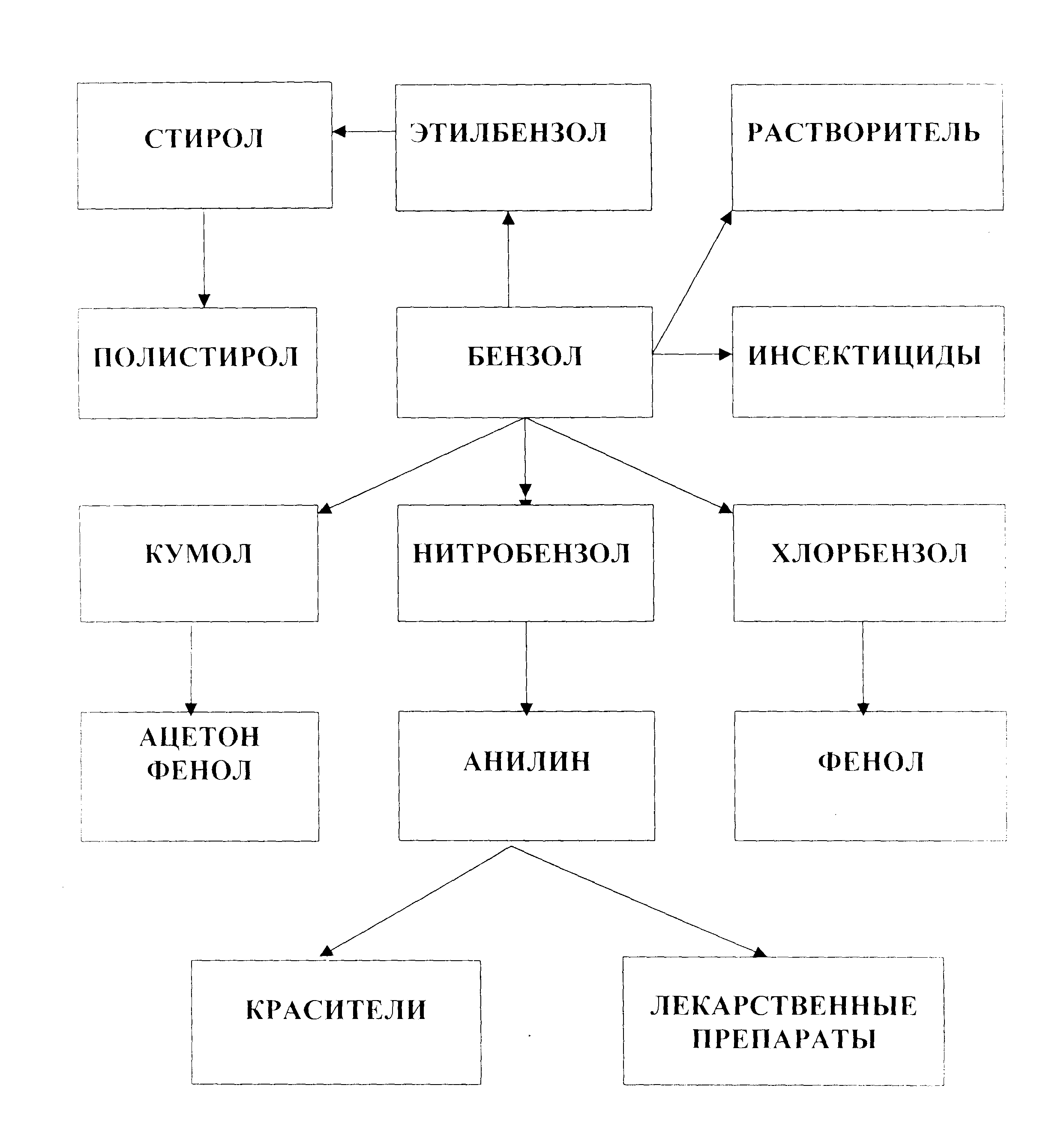 . Используя схему применения углеводородов, напишите уравнения реакций, при помощи которых можно осуществить известные вам превращения.
. Используя схему применения углеводородов, напишите уравнения реакций, при помощи которых можно осуществить известные вам превращения.
600-7000C

 -CH2-CH3
-CH2-CH3
1
AlCl3 )CH2=CH2+
)CH2=CH2+

 -CH2-CH3 6000C -CH=CH2
-CH2-CH3 6000C -CH=CH2
2) → +H2
ZnO
-CH=CH2  t,кат
t,кат
3)n → [-CH-CH2-]n
\
4) C6H5
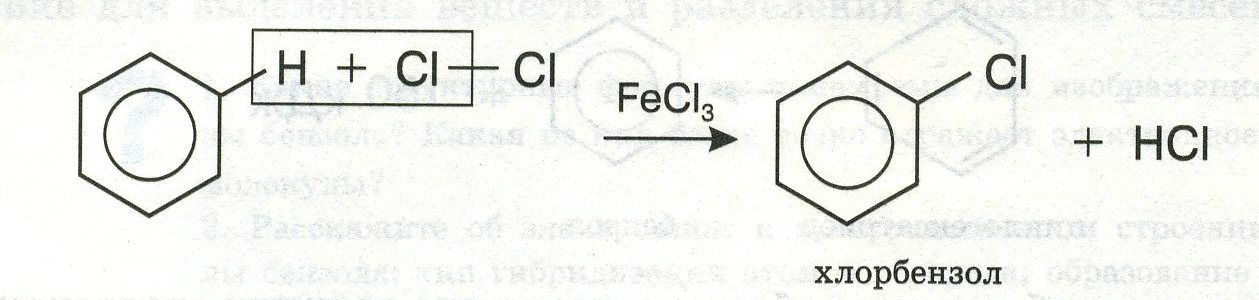
5)
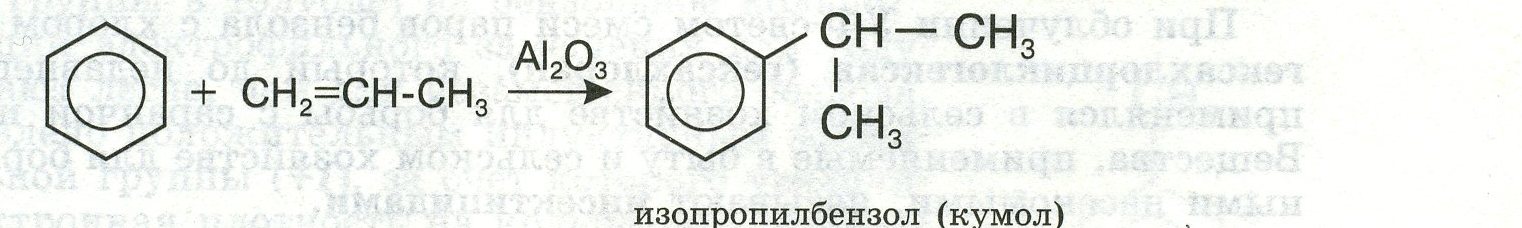
6)
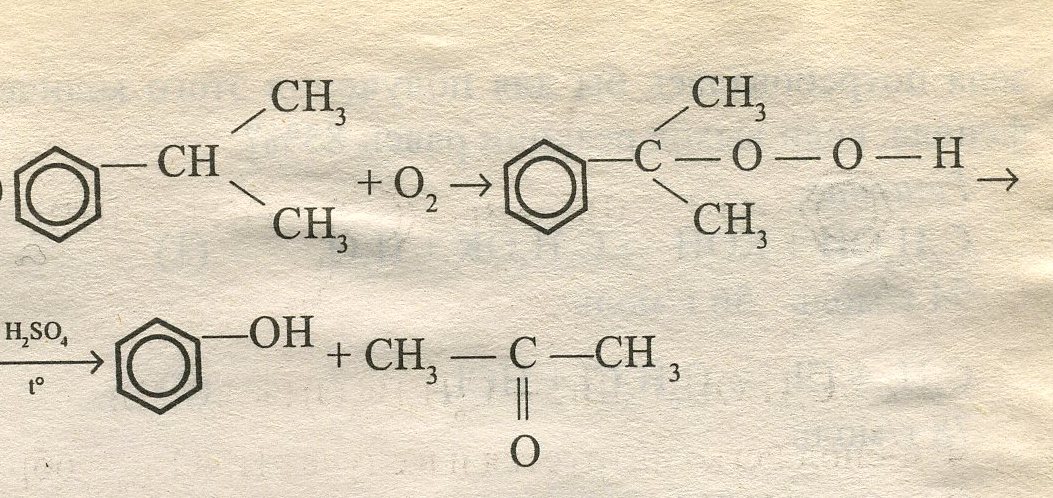
7)
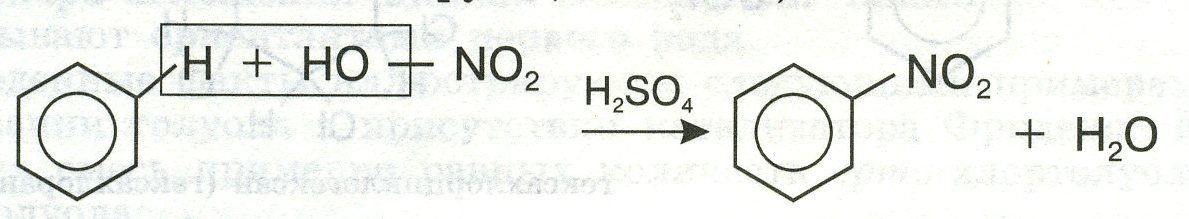
2. Составьте генетические переходы, иллюстрирующие применение природного газа на примере метана
C+H2
↑
СH4→CO+H2→CH3OH
↓
C2H2→CH3-COH
Программа «В»
1. Генетические ряды каких веществ вы изучили в курсе неорганической химии? Приведите по одному примеру на каждый случай и напишите соответствующие уравнения реакции для них.
а) металл→оксид металла→гидроксид металла→соль;
б) неметалл→оксид неметалла→кислота→соль.
а) S→SO2→H2SO3→Na2SO3
б) Li→Li2O→LiOH→Li2SO4
2. Составьте генетические ряды в органическом синтезе, используя компонент попутного нефтяного газа (на примере этана)
полиэтилен
↑
C2H6→C2H4→этанол
↓
этиленгликоль
Предлагаю учащимся проверить свою готовность к сдаче Единого Государственного Экзамена с помощью теста по дифференцированным программам, предложенным в интерактивном режиме. Выбор программ «А» или «В» осуществляют сами учащиеся в соответствии с уровнем их подготовки.
Программа «А»
I .Изобутан вступает в реакцию:
а) изомеризации
б) присоединения
в) замещения
г) полимеризации
II. С раствором КМпО4 взаимодействуют все вещества:
а) этан, пропан, этин
б) бутен-1, бутадиен, ацетилен
в) пропан, этилен, пропилен
г) хлорэтан, этилен, пропилен.
III. Объем порции бутена (в л, н.у.), в которой содержится 1,505*1024 атомов углерода, равен: а) 5,6 в) 56 6)14 г) 220
IV. В цепочке превращений вещество - Х3 - это:
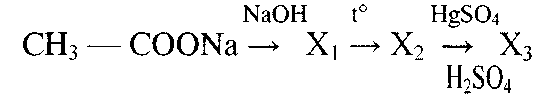
а) бутин
б) уксусный альдегид
в) бензол
г) этиловый спирт.
Программа «В».
I. Метилциклопропан и бутен-2 являются:
а) структурными изомерами
б) внутригрупповыми изомерами
в) одним и тем же веществом
г) гомологами.
II. Способ получения бензола - это
а) дегидрирование бутана
б) дегидратация и дегидрирование этанола
в) дегидрирование и одновременно циклизация гексана
г) действие натрия на 1,6-дихлоргексан.
Ш. Число ϭ - связей в молекуле бутена-1: а)3; 6)6; в) 9; г) 12.
IV. В цепочке превращений вещество - Х3 -это:
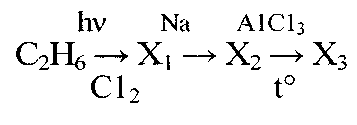
а) пропилен
б) пропан
в) изобутан
г) циклопропан.
Предлагаю учащимся сделать вывод по проделанной работе
а) многообразие органических веществ проявляется в форме существования гомологов и изомеров;
б) способность углеводородов к взаимным превращениям свидетельствует о единстве разнообразных по строению органических соединений;
в) возможность превращения неорганических веществ в органические. и наоборот, свидетельствует о единстве материального мира.
Экологические проблемы, связанные с использованием природных источников углеводородов и их производных.
а) сжигание топлива.
Природные источники углеводородов - каменный уголь, нефть, природный газ -сгорая, выделяют углекислый газ, различные сернистые соединения, оксиды азота и т.д. Попав в атмосферу, они превращают влагу дождей в мертвую кислую воду. От кислых дождей снижается плодородие почв, уменьшается урожайность сельскохозяйственных культур. Кислотные дожди разрушают здания, памятники архитектуры, вызывают коррозию металлов.
б) повреждение нефтепроводов, гибель танкеров;
в) ядохимикаты - пестициды: инсектициды, фунгициды, зооциды, гербициды.
В производстве и использовании инсектицидов и других химических средств защиты растений существует много проблем: их не хватает, не везде они эффективно используются, их применение связано с нарушением экологического равновесия. По биологической цепи почва-растение-человек или почва-растение-животное-человек, а также через воду и воздух они могут попасть в организм человека. С одной стороны, пестициды повышают урожайность сельскохозяйственных культур (до 30%) экономически они выгодны. С другой стороны, их применение ведет к появлению вредных насекомых, устойчивых к многократно увеличенным дозам ядохимикатов, отрицательно влияет на почву, угнетая почвенную фауну и микроорганизмы. Отсюда возникла проблема создания инсектицидов нового поколения, которые уничтожают насекомых на стадии размножения, имеют небольшую продолжительность жизни и нетоксичны для теплотворных животных, птиц и человека.
К инсектицидам относятся, например, гептахлорциклопентадиен (промышленное название - гептахлор)
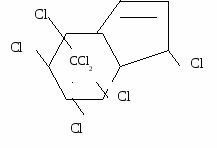
Им обрабатывают семена сахарной свеклы и кукурузы.
Для борьбы с филлоксерой винограда используется гексахлорбутадиен-1,3 CCl2=CCl-CCl=CCl2
Фунгицид гексахлорбензол применяется для протравления семян пшеницы - защита от твердой головни:
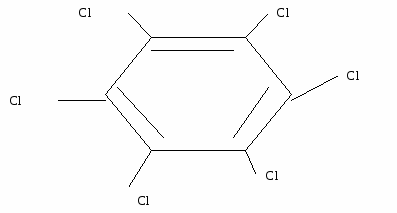
За страницами учебника.
Ограничения, налагаемые L-оболочкой.
Углерод не образует комплексов.
При образовании четырех ковалентных связей у углерода возникает октет электронов. Этим объясняется инертность многих соединений углерода. При полном октете и отсутствии неподеленных пар - углерод не может быть ни донором, ни акцептором электронов, и поэтому не образует комплексных соединении.
На основе рефлексии подвожу итог урока, и учащиеся оценивают свою работу на уроке.
Выводы:
-
Используя общие формулы углеводородов можно установить их принадлежность к различным классам органических соединений.
-
На основании структурных формул органических веществ можно дать им название по систематической номенклатуре.
-
Особенности строения органических веществ определяют их химические свойства соединений.
-
Единство материального мира раскрывается на основе взаимных превращений органических и неорганических веществ.
-
Идеи Д.И.Менделеева оказали существенное влияние на развитие химической промышленности России.
-
Создание современных химических препаратов на основе использования источников углеводородов и их производных для решения экологических проблем.
Домашнее задание
Повторить гл.П § 13, гл. Ш §§ 17,18,23,24
Решить следующие задачи:
-
Природный газ одного из месторождений содержит 92% метана, 4% этана, 1% пропана, 2% углекислого газа и 1% азота (по объему). Какой объем кислорода потребуется для сжигания 200л этого газа?
-
При сжигании углеводорода массой 29г образовалось 88г оксида углерода (IV) и 45г воды. Относительная плотность вещества по воздуху равна 2. Найдите молекулярную формулу углеводорода.
-
При пропускании смеси этилена и этана объемом 30л (н.у.) через бромную воду, ее масса увеличилась на 7г. Рассчитайте объемные доли газов в смеси.
Литература.
1. Габриелян О.С.Химия: Органическая химия: Учеб. для 10 кл. общеобразовательных учреждений с углубленным изучением химии/ О.С.Габриелян, И.Г.Остроумов, А.А.Карцова. - 2-е изд. - М.: Просвещение, 2004.
2. Габриелян О.С. Органическая химия в тестах, задачах, упражнениях. 10 класс.: Учебное пособие для общеобразовательных учреждений / О.С.Габриелян, И.Г.Остроумов, Е.Е. Остроумова . - М.: Дрофа, 2003.
3. Габриелян О.С. Химический эксперимент в школе. 10 класс: учебно - метод. пособие/ О.С.Габриелян, Л.П.Ватлина. - М.: Дрофа, 2005.
15


