- Преподавателю
- Химия
- Ашык сабак (Открытый урок) на каз языке
Ашык сабак (Открытый урок) на каз языке
| Раздел | Химия |
| Класс | - |
| Тип | Рабочие программы |
| Автор | Молдабаева Ж.Е. |
| Дата | 08.03.2014 |
| Формат | doc |
| Изображения | Есть |
Осакаров ауданы. №23 орта мектеп.
Ашық сабақ
Тақырыбы: «Кальций, атом құрылысы, қасиеттері. »
( 9 «в»-сынып )
Химия-биология мұғалімі: Молдабаева Ж.Е
2011-2012 оқу жылы.
Сыныбы: 9в-сынып
Тақырыбы: § 35. Кальций, атом құрылысы, қасиеттері
Мақсаты :
1. Білімділік. Кальций,атом құрылысы,қасиеттері,периодтық жүйедегі орны,ашылу тарихы,табиғатта таралуы,алынуы,физикалық,химиялық қасиеттері жайында мәлімет беру.
2. Тәрбиелік. Кальций,атом құрылысы,қасиеттерін түсіндіре отырып, оқушыларды тазалыққа, қоршаған ортаны қорғауға, адамгершілік қасиеттерін қалыптастыруға,металдарды тиімді пайдалануға тәрбиелеу.
3. Дамытушылық. Кальций,атом құрылысы,қасиеттерін түсіндіре отырып, химия пәнінен алған білімдерін жетілдіру, өз бетінше іздену қабілетін дамыту.
Сабақтың типі: Жаңа сабақты меңгерту
Сабақтың түрі: Аралас сабақ (тірек сызба, )
Сабақтың әдісі: Түсіндіру, химиялық диктант
Сабақтың көрнекілігі: Интерактивті тақта,Д.И.Менделеев кестесі
Пән аралық байланыс: физика,математика,биология
Сабақтың барысы:
І. Ұйымдастыру кезеңі:
-
Сәлемдесу, түгелдеу
-
Оқушылардың құрал - жабдығын тексеру
-
Оқушылар назарын сабаққа аудару
ІІ. Оқушы білімін жан-жақты тексеру:
1. Активтік қатары дегеніміз не?
2. Металдар коррозиясы?
3. Алюминий құймасы?
4. Металдардың қышқылдарға қатынасы?
ІІІ. Жаңа түсінік беру.
Кальций IV-период, II топтың негізгі топшасының элементі,реттік нөмірі 20,ядросында 20 протонмен 20 нейтроны бар.Ar =406электрондарыны4 жалпы саны да 20.Кальцийдің электрондық формуласы 1s22s2 2p6 3s23p64s2,валенттілік электрондары 4s2болғандықтан кальций қосылыстарында II валентті.
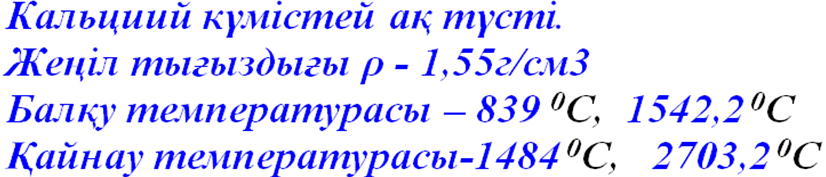
-
Жаңа түсініктер мен іс-әрекеттер тәсілін қалыптастыру.
Жаңа ұғымдар: Маңызды химиялық элементтер.
Сульфаттар - CaSO 4 *2H2O Доломит - CaCO3*2MgCO3
Карбонаттар - CaCO3 Апатит - Ca5(PO4)3OH
Фосфоттары -фосфорит -Ca3(PO4)2
Электртерістігі аз-1,04, металдық қасиеттерін байқатады, көптеген тұздар және бинарлы қосылыстар түзеді. Химиялық таралуы бойынша табиғатта алтыншы элемент, көптеген қосылыстар түрінде кездеседі. Көптеген минералдар мен тау жыныстарының құрамына енеді.
Ағзалар үшін маңызды элемент. Сүйекте және тісте әр түрлі фосфаттар түрінде жинақталады, тәулігіне адамға қажетті норма-1г кальций. Қанның ұйылуы Са2+ ионымен байланысты. Бұл металдың жетіспушілігі сүйектерді жұмсартады және рахиттің себебі болады. Коралл және моллюскілердің қабығы кальций карбонатынан тұрады. Кальцийді 1808 жылы ағылшын химигі, физигі Г.Дэви сынап катодында ылғалды сөндірілген әктасты Са(ОН)2 электролиздегенде алған.
V.Мұғалімнің проблемалық және ақпараттық сұрақтар
1. Кальцийдің периодтық жүйедегі орны
2. Калицийдің электрондық формуласы?
3. Кальцийдің табиғатта таралуы
-
Жаңа түсінікті тексеру:
-
Кальцийдің физикалық қасиеттері
-
Калицийдің химиялық қасиеттері
-
Кальцийдің алынуы
Зертханалық тәжірибе көрсету: кальцийдің химиялық қасиеті, кальцийдің сумен, тұз қышқылымен әрекеттестіру.
Са+Н2О=Ca(OH)2+H2↑
Ca+HCL=CaCL2+ H2↑
-
Жаңа сабақты бекітуге арналған жаттығулар.
Химиялық диктант
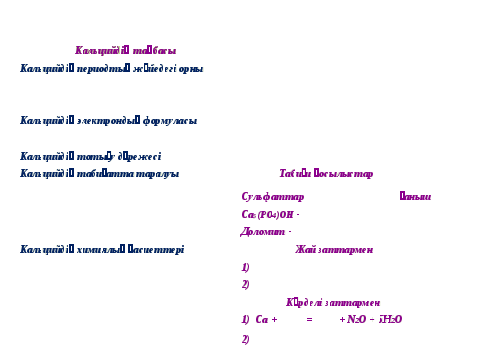
-
Жаңа сабақты қорытындылау
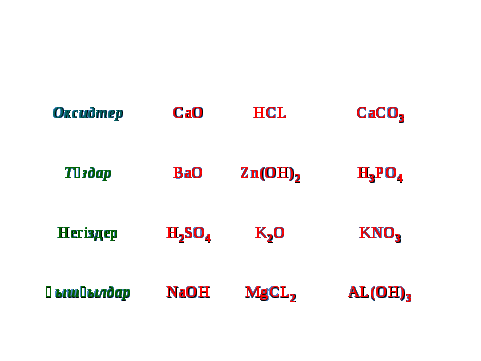
Эстафеталық есеп шығару.
Мына айналуларды іске асыратын реакция теңдеуін жазыңдар
Ca→CaO→Ca(OH)2→CaCL2→CaCO3
-
2Ca+O2→2CaO
-
CaO+H2O→ Ca(OH)2
-
Ca(OH)2+2HCL=CaCL2+2H2O
-
CaCL2+Na2CO3=CaCO3↓+2NaCL
-
Оқушылардың еңбегін бағалау.
-
Үй тапсырмасы: §35.Кальций,атом құрылысы қасиеттері
№ 1 есеп (104-бет)
Білім деңгейі жоғары
Металдардың қышқылдармен әрекеттесу реакция теңдеуін жаз.
Zn+H2SO4→
Mg+ H2SO4→
Ag+HNO3→
Білім деңгейі жоғары
Металдардың тұздармен әрекеттесу реакция теңдеуін жаз.
Cu+Hg(NO3)2→
Zn+CuSO4→
Mg+CuCL2→
Білім деңгейі жоғары
Металдардың оксидтермен әрекеттесу реакция теңдеуін жаз.
AL+Fe2O3→
Mg+CO2→
Білім деңгейі жоғары
Электрохимиялық кернеу қатарында металдар орналасуына қарай нешеге бөлінеді?
Ең қиын балқитын металды тауып, электрондық (конфигурация) формуласын жаз?
Білім деңгейі орташа
Ең жеңіл металлды тауып, электрондық формуласын жаз?
Сілтілік металдарды жаз ?
Білім деңгейі орташа
Массасы 5,4 г алюминий металы үлгісіндегі алюминийдің зат мөлшерін есепте.
Жауабы:0,2 моль
Білім деңгейі орташа
5,6 г темірдегі зат мөлшерін, атом санын анықтаңдар.
Жауабы: 0,1 моль
Білім деңгейі орташа
Al2O3 алюминийдің массалық үлесін анықта.
Жауабы: 52,9 %
Білім деңгейі төмен
Алюминий құймасы қандай металдардан құралады?
Білім деңгейі төмен
Магний қүймасы қандай металдардан құралады?
Білім деңгейі төмен
Мыс негізіндегі құймаларды ата?


