- Преподавателю
- Химия
- Урок в 8 классе на тему: Оксиды
Урок в 8 классе на тему: Оксиды
| Раздел | Химия |
| Класс | 7 класс |
| Тип | Конспекты |
| Автор | Узенькова А.В. |
| Дата | 05.01.2016 |
| Формат | doc |
| Изображения | Есть |
12.02.2016 г
Тема урока «ОКСИДЫ»
Краткое описание урока: урок изучения нового материала по теме «Оксиды» и первичного закрепления знаний обучающихся. Урок составлен в соответствии с требованиями ФГОС второго поколения, на основе деятельностного подхода к организации образовательного процесса.
Описание урока
Тип урока: урок изучения нового материала и первичного закрепления знаний.
Цель урока: Формирование представлений об оксидах, их номенклатуре.
Задачи:
-
Научить выделять общие признаки класса оксиды, составлять формулы оксидов и давать им названия.
-
Продолжить формирование естественно-научного мышления, развитие коммуникативных умений через работу в парах, привитие навыков самоконтроля и взаимоконтроля через самопроверку.
Планируемые результаты:
-
Личностные:
Развитие познавательных интересов, интеллектуальных и творческих способностей.
-
Метапредметные:
-
познавательные:
Находить сходство и различие между объектами, обобщать полученную информацию, вести наблюдения, классификация объектов по предложенным критериям
-
информационно-коммуникативные:
Умение формулировать определение, подбирать аргументы.
-
регулятивные:
Выполнять учебное задание в соответствии с целью.
Соотносить учебные действия с известными правилами.
Выполнять учебное действие в соответствии с планом.
Оценка своих учебных достижений.
-
Предметные умения:
Давать определение «оксиды», распознавать оксиды среди других веществ, составлять формулы оксидов и называть их, описывать свойства оксидов.
Методы обучения: объяснительно - иллюстративный, репродуктивный, частично - поисковый, проблемный, беседа, устный опрос, организация упражнений по применению знаний (групповая, индивидуальная), самопроверка обучающихся.
Организация образовательного пространства:
Ресурсы - мультимедийный проектор.
Оборудование: учебники, дидактические карточки для дифференцированного задания на дом. Демонстрационные образцы на учительском столе: бутылка с газированной водой, стакан с водой, стеклянная ваза, фарфоровая чашка. На ученических столах раздаточный материал для лабораторного опыта.
Технология изучения темы
Звучит тихая музыка: моцарт-турецкий марш
1 этап: Самоопределение к деятельности (1 минута) Учитель: -Здравствуйте, ребята! Рада видеть вас на нашем уроке, и думаю это взаимно! Проверьте, все ли у вас готово для плодотворной работы на уроке: учебник, тетрадь, дневник, ручка и ваши светлые головы.
Психологический настрой на урок: «Подари улыбку» Слайд1
Улыбка ничего не стоит, но много дает. Она обогащает тех, кто ее получает, не обедняя при этом тех, кто ею одаривает. Она длится мгновение, а в памяти остается порой навсегда. Она создает счастье в доме, порождает атмосферу доброжелательности в деловых взаимоотношениях и служит паролем для друзей. Подарите друг другу улыбку. Улыбайтесь, и вы будите нравиться людям.
Учитель: на столах у вас по три смайлика. Выберите тот, который соответствует вашему настроению. Поднимите его и покажите вашему соседу. Ну что мы видим, у вас хорошее настроение, настрой и мы можем начинать.
2. Создание проблемной ситуации (2 мин.) Слайд2
(Цель: формирование системно-информационного анализа, развитие умений определять цели и задачи деятельности, выбирать средства реализации цели)
Учитель: На моем столе представлена коллекция предметов из различных веществ: бутылка с газированной водой, стакан с водой, фарфоровая чашка, стеклянная ваза.
-Почему предметы собраны вместе?
-Что их объединяет с химической точки зрения?(состав)
Учитель: Правильно.Эти вещества являются сложными по составу.
3 слайд(формулы этих веществ)
3. Этап целеполагания на уроке (3 мин.)
(Цель: формирование у учащихся способности самостоятельно ставить учебные цели на урок) Учитель: А сейчас я вас прошу прочитать формулы этих веществ (обращаем внимание на слайд, читают формулы веществ)
Учитель: Молодцы! Мы назвали формулы, а теперь посмотрите, что у них общего?
Учащиеся должны сказать:
• в каждой из формул есть кислород
• это сложные вещества
• это оксиды
Учитель может задать наводящие вопросы:
• Какой химический знак есть в каждой из формул?
• Какие это вещества: простые или сложные?
• Как называется этот класс неорганических соединений?
Учитель:Правильно - это оксиды, тема нашего урока : «Оксиды». (Открывают технологические карты, записывают число и тему урока.)
Слайд4 тема с эпиграфом,
Слайд5стих про оксиды.
Учитель: Ребята! Как вы думаете, что мы о них можем узнать? Слайд6
Целью нашего с вами урока является: узнать что такое оксиды, как правильно их называть, рассмотреть классификацию, состав и строение.
Слайд7 план урока
4. Учитель раздает задания по парам.
Ребята! Сейчас 4 парам раздам опережающее задание. Результат их деятельности мы обсудим через несколько минут.
5. Этап «Открытие нового знания» (3 мин.) А пока наши пары работают мы с вами продолжим...
Теперь попробуем сформулировать определение оксидов, ответив на 3 вопроса. Слайд8
а) Оксиды сложные вещества?
б) сколько элементов в составе оксидов?
в) какой элемент обязательно входит в состав оксидов?
Учитель: попробуем сформулировать на основе того, что мы разобрали, что же такое оксиды
Ученики:Оксиды - это …
Слайд 9 оксиды - это ………………….И их общая формула : ЭnOm(Открывают технологические карты, записывают определение)
Слайд 10Первичная проверка усвоения нового материала. (3 мин.) Учащиеся выполняют задание .
1) Какое из двух веществ можно отнести к оксидам: а) N2O3 или Ca3N2 б) Ca(OH)2 или CaO? Ответ мотивируйте
-
А это оксид? H2O2
( учащиеся - это не оксид, т. к. валентность кислорода равна 1)
Слайд 11Игра «Волшебный цветок» на пару
Сорвать все лепестки с формулами оксидов.
(Учащиеся работают в группах, выбирают формулы оксидов, мотивируя свой выбор).
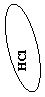
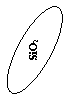


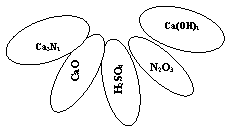
(создание проблемной ситуации и ее решение)
Слайд 12 Поиграйте в «крестики - нолики». Покажите выигрышный путь, который составляют формулы оксидов.
Приложение 2.
Поиграйте в «крестики - нолики». Покажите выигрышный путь, который составляют формулы оксидов.
HCl
NaOH
SO2
O2
Al2O3
Li2S
FeO
H2CO3
NaBr
Слайд 13 Задание 1 пары. Физические свойства. Слайд 14 Физминутка. Трудным оказался путь, надо бы передохнуть. (Зарядка для глаз) Физкультминутка
Проводится на 15 минуте урока
Раз - подняться, потянуться,
Два - нагнуться, разогнуться,
Три - в ладоши, три хлопка,
Головою три кивка.
На четыре - руки шире,
Пять - руками помахать,
Шесть - на место тихо сесть
Слайд 15 Этап «Открытие нового знания» Номенклатура оксидов (7 мин)в парах работают (записи в технологическую карту)
ГРУППА 2, Номенклатура оксидов, см.стр.90-91 Составьте формулы названных в тексте оксидов (работа с текстом в группе, самоконтроль по шаблону)
В земной коре - литосфере - находится оксид алюминия ________ (глина), оксид кремния (IV) _____ (песок), оксид железа (III) ______ (содержится в красном железняке). Водная оболочка Земли - гидросфера - оксид водорода _____. В воздухе есть оксид углерода (IV) ______ (углекислый газ). В результате хозяйственной деятельности человека образуются вещества, загрязняющие атмосферу: оксид углерода (II) _____ (угарный газ), оксид серы (IV) ______ (сернистый газ), оксид азота (II) ____ и оксид азота (IV) ______.
Ответ: оксид алюминия - Al2O3, оксид кремния - SiO2, оксид железа (III) - Fe2O3, оксид водорода - Н2О, оксид углерода (IV) - СО2, оксид серы (IV) - SO2, оксид азота (II) - NO, оксид азота (IV) - NO2
Слайд 16. Упражнение «Не прерви цепочку». (Для каждой пары приготовлена карточка с формулой оксида. Ученик поднимает карточку, показывает всем, и дает название оксиду. Работа по цепочке.)
Слайд 17-20 этап "Открытие нового знания" Классификация оксидов (10 мин)кластер составляют в паре Классификация оксидов пара 3(записи в технологическую карту)
Слайд 21 Дидактическая задача. Из следующего перечня выписать основные и кислотные оксиды.
SiO2,MnO,FeO,SO3,Cu2O,MgO,P2O5,Cl2O7
( у доски один ученик, остальные самостоятельно, затем проверка ).
Слайд 22
Дидактическая задача. Определить лишнее вещество и обосновать, почему эти вещества вы считаете лишними.
А) N2O5 , CaO , CO2
Б) SiO3 , K2O , SO3
В) BaO , P2O5 , Cl2O7
Основные оксиды. CaO
K2O
BaO
Слайд 23-24
А почему называют их основными? Для этого проведём опыт.
Т/б. При работе с оксидами выделяется теплота, поэтому воду приливаем понемногу!
Информация учителя.У вас на столах в чашках Петри оксид кальция, в стакане вода, приливайте по каплям воду, затем фенолфталеин ( индикатор).
Так, что образовалось при взаимодействии оксида кальция с водой.
-Основание. Добавили фенолфталеин, он стал малиновый.
Вывод: характер свойств оксидов в первую очередь зависит от валентности элемента. (записи в технологическую карту)
Например, оксиды хрома:
CrO (II - основный);
Cr2O3 (III - амфотерный);
CrO3 (VI - кислотный)
Слайд 25 Закрепление. Молодцы! А теперь для закрепления полученных знаний выполним тест в 2-х вариантах. Взаимопроверка. Проверяем полученные результаты, сверяем правильные ответы с экраном. Обучающиеся комментируют полученные ответы.
Слайд 26. Составим синквейн по данной теме. Вот и подошло к концу наше путешествие по стране оксидов. Посмотрите ваши записи в тех.карте и поделитесь своими впечатлениями о том, что вы узнали на уроке.
Слайд 27. 4 этап: Рефлексия (Цель: формирование у учащихся способности подводить итоги урока, обобщать, делать выводы, характеризовать свои действия)
Молодцы, вы сегодня хорошо работали. Мы все вместе узнали что-то новое и всё же каждый для себя совершил какое - то открытие. Поделитесь этим открытием, закончите предложение:
Сегодня на уроке
Ø Мне удалось...
Ø Я узнал(а) много нового …
Ø Я научился …
(мы сегодня научились находить формулы оксидов среди других веществ, называть оксиды и составлять формулы по названиям, познакомились с отдельными представителями оксидов.)
Слайд 28Домашнее задание: Открываем дневники и записываем§ 30 + задание в раб.тетр№127,131,132,135стр49-51
Слайд 29Подведение итогов урока Д. Хевелси говорил: «Мыслящий ум не чувствует себя счастливым, пока ему не удается связать воедино разрозненные факты им наблюдаемые», сегодня мы попытались создать «портрет оксидов» из тех фактов, которые были известны и из новых сведений об этом классе неорганических соединений.
Слайд 30 Спасибо за внимание!
Приложение
Задание 1 паре, на 5-7 мин…см.стр.91, физические свойства
Лабораторный опыт в паре. У вас на столе стоят разносы с различными веществами и лежит карточка "Приложение 1". В них вы и будите работать. Вам необходимо будет определить визуально цвет вещества, агрегатное состояние, растворимость и все это занести в таблицу!
Учащиеся заполняют таблицу: агрегатное состояние, цвет оксидов, растворимость в воде.
Приложение 1
1 пара.
Учитель: что от вас требовалось?
Обучающийся(аяся): нам необходимо было определить визуально цвет вещества, агрегатное состояние и его растворимость. (У доски, результаты работы зачитывают и показывают образцы оксидов) Зачитывают вывод.
Лабораторный опыт: « Физические свойства оксидов»
Задание №1: экспериментально опишите свойства оксидов. Заполните таблицу.
Название и состав (химическая формула)
цвет
Агрегатное состояние (твердое, жидкое, газообразное)
Растворимость в воде
оксид меди (II) Cu O
Оксид железа (III) Fe2O3
Оксид кальция СаО
Оксид водорода (Вода) H2O
Оксид марганца (IV)MnO2
темно-коричневый
твердое
нерастворимый
Вывод:оксиды бывают твердые, жидкие и газообразные, различного цвета.
- Учитель: добавим эту запись в технологическую карту
2 пара, Номенклатура оксидов, см.стр.90-91
Оксид + название элемента в родительном падеже (валентность в случае ее переменности)
Составьте формулы названных в тексте оксидов (работа с текстом в паре)
В земной коре - литосфере - находится оксид алюминия ________ (глина), оксид кремния (IV) _____ (песок), оксид железа (III) ______ (содержится в красном железняке). Водная оболочка Земли - гидросфера - оксид водорода _____. В воздухе есть оксид углерода (IV) ______ (углекислый газ). В результате хозяйственной деятельности человека образуются вещества, загрязняющие атмосферу: оксид углерода (II) _____ (угарный газ), оксид серы (IV) ______ (сернистый газ), оксид азота (II) ____ и оксид азота (IV) ______.
Учитель: какое у вас было задание?
Обучающийся (аяся): нам надо было определить номенклатуру оксидов, а также составив формулы оксидов, вставить их в текст (зачитывают текст с формулами)
Учитель: запишите на доске схему определения номенклатуры оксидов.
Обучающийся (аяся): Оксид + название элемента в родительном падеже +валентность (в случае ее переменности)
Учитель: добавим эту запись в технологическую карту.
Задание: составить кластер по классификации оксидов (см. стр.89-90, схема 11)
3 пара Классификация оксидов
Кластер
Выучить к открытому уроку!
Класс оксидов это да!
Ведь без них мы никуда..
Очень важная вода
Без неё кругом беда!
При строительстве идёт
Глина и песок
Ну а красный железняк
В металлургии мастак!
Загрязняют атмосферу,
Отравляют биосферу
Угарный и сернистый газ,
А винить то надо нас!
Чтоб природу не губить
Надо химию учить.
К концу урока их изучим
Новые сведения получим!


