- Преподавателю
- Химия
- Внеклассное мероприятие по химии 175-летию со дня рождения Д. И. Менделеева
Внеклассное мероприятие по химии 175-летию со дня рождения Д. И. Менделеева
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Дышкант Н.А. |
| Дата | 28.09.2015 |
| Формат | doc |
| Изображения | Есть |
Внеклассное мероприятие
К 175-летию со дня рождения Д.И.Менделеева
Жизнь и творчество
Преподаватель: Зимой 1834 г. в семье директора Тобольской гимназии родился последний, семнадцатый ребенок - в будущем краса и гордость русской нации - Дмитрий Иванович Менделеев. Отец его умер в 1847 г., оставив семье скудную пенсию. Но энергичная сибирячка-мать не упала духом. Получив от брата заброшенный стекольный завод, она восстановила его и, кое-как сводя концы с концами, обеспечила младшему и самому любимому сыну безбедное детство. Кучи песка и известняка, палящий жар стеклоплавильных печей остались у Менделеева самыми главными воспоминаниями детства.
Чтец: «...Выросши около стекольного завода, который вела моя мать, тем содержащая детей, оставшихся на ее руках, сызмала пригляделся к заводскому делу... Поэтому, отдавшись такой отвлеченной и реальной науке, как химия, я смолоду интересовался фабрично-заводскими предприятиями...»
Ведущий: Мальчик не подозревал, что «чудо» превращения песка, известняка и соды в сверкающее прозрачное стекло называется химией. Он не узнал этого и в гимназии, куда поступил семи лет. Химии там не обучали. Ее место в учебном плане занимали древние языки. Митя не мог понять, зачем нужно изучать язык, на котором не говорит ни один из ныне живущих народов. Ни вдохновенный эпос Гомера, ни суровая история Тацита не воспламеняли его воображения. Ему грезилось не прошлое, а будущее, не овеянные славой легионы Юлия Цезаря, а межпланетные снаряды, устремляющиеся на завоевание пространства. Его любимым писателем стал со временем Жюль Берн, а любимым героем - Ньютон, подчинивший одной-единственной формуле и полет снарядов на полях сражений, и движение планет, и падение с яблони подточенного червем яблока.
Преподаватель: Впоследствии, когда маленький ученик сделается большим ученым и учителем, голос которого будет звучать на весь мир, он назовет «латынщиной» всякое ложное мудрствование, не приносящее пользы людям. Пока же - ничего не оставалось, как с упорством отчаяния зубрить: «homo homini...».
Ведущий: Но вот уже пролетело безмятежное детство. Наступила новая полоса жизни. Перед 16-летним юношей открылись двери Главного педагогического института в Петербурге. Здесь Дмитрий Менделеев нашел то, что бессознательно искал, а именно - химию.
Учащийся 1: «Если какое-либо тело с массой...» - так начиналось в учебнике физики доказательство ньютоновских теорем. Несмотря на преклонение перед Ньютоном, Дмитрию Менделееву хотелось мысленно увидеть и осязать это «некоторое тело», увидеть его окраску, почувствовать его запах, узнать, из какого материала оно сделано, откуда взялся этот материал...
Учащийся 2: Поразительно было «открытие», что все, казалось бы, бесконечно разнообразные «тела» состоят из крайне ограниченного числа элементов, комбинирующихся по два, по три... в строго определенных весовых отношениях, следуя законам «постоянства состава» и «кратных отношений».
Ведущий: Именно здесь-то и начиналась доселе неведомая, чарующая наука - химия.
Учащийся 3: Для многих юношей увлечение химией начинается со взрывов, бенгальских огней, приготовления пороха... Первые работы студента Менделеева, увидевшие свет, были посвящены анализу минералов. Что может быть скучнее: растворять, осаждать, фильтровать, прокаливать и взвешивать? Но молодой студент не находил это скучным занятием; он пользовался каждым свободным часом, чтобы что-нибудь профильтровать или взвесить. В то же время он проводил бессонные ночи над изучением языков - не «латынщины», а тех языков, на которых говорили и писали статьи по химии современники. Педагогический институт был окончен Менделеевым с золотой медалью.
Ведущий: Год педагогической практики на юге России восстановил подорванное здоровье начинающего ученого - и вот опять петербургские туманы, холодный ветер с Невы. научные журналы и живое общение со старшими товарищами по науке... Менделеев 23 лет от роду после защиты магистерской диссертации на тему «Удельные объемы» стал преподавателем химии Петербургского университета. Его слушатели были немногим моложе его самого, но никому из них не приходило в голову усомниться в авторитете молодого ученого. Он всей душой отдался своим обязанностям: ничто не казалось ему более интересным и важным делом, чем преподавание химии и научная работа. И, оставляя аудиторию, он спешил в свою скромную лабораторию, чтобы продолжить начатые опыты.
Учащийся 4: Спустя еще два года, в 1859 г., Менделеев отправился в двухгодичную научную командировку за границу. Он попал в новый мир. Здешние студенты, по первому впечатлению, были совсем не похожи на его бывших товарищей по институту: они не спорили о судьбах своей родины, не читали тайком запрещенных книг, науке и книгам они предпочитали пышные процессии по городу, пьяные скандалы в пивных и дуэли. Это называлось традициями германских университетов; их ревностно поддерживала «золотая молодежь» - беззаботные дети состоятельных родителей. Но в лабораториях Гейдельбергского университета Менделеев нашел привычную атмосферу научных исканий, близких ему по духу тружеников науки. Своей темой он избрал взаимоотношение жидкого и парообразного состояний веществ.
Учащийся 5: Выбор не случаен: сжижение газов есть проявление взаимного притяжения их частиц; более сложным проявлением тех же сил является образование химических соединений. Чтобы постигнуть образование химических соединений, нужно изучить более простые случаи сцепления частиц - сжижение газов.
Преподаватель: Работа Менделеева завершилась замечательным открытием. Если любую жидкость все сильнее нагревать в запаянном сосуде, из которого выкачан воздух, то наступает момент, когда разделительная грань между жидкостью и ее паром, мениск, внезапно исчезает. Температуру, при которой это происходит, ученый назвал «абсолютной температурой кипения», т.к. при этой температуре (и, конечно, выше ее) никаким давлением нельзя предотвратить превращение жидкости в пар. Чем ниже абсолютная температура кипения (сейчас мы называем ее «критической температурой»), тем труднее происходит обратное превращение - сгущение газа в жидкость. Впоследствии, когда Наттерер будет безуспешно пытаться обратить в жидкое состояние воздух при температурах, значительно превышающих критические температуры кислорода и азота, Менделеев укажет ему на причину его неудач, но пока, удовлетворившись достигнутыми результатами, он оставил эту область исследования и не участвовал в практическом триумфе своих же собственных открытий. Этот триумф заключался в переводе в жидкое состояние газов, которые до сих пор слыли «постоянными газами».
Ведущий: Вместе с Менделеевым мы оставляем эту область его исследований и переносимся на Всемирный конгресс химиков в Карлсруэ, состоявшийся в сентябре 1860 г. Он попал туда не в качестве почетного гостя или докладчика по принципиальному вопросу, а просто в качестве безмолвного свидетеля событий, которыми предопределялась судьба химии как науки.
Учащийся 6: Вместе с тем на конгрессе в Карлсруэ предопределилась и роль, которую сыграл в развитии химии Менделеев, - он сам отметил это впоследствии. В чем же заключалось значение для развития химии съезда химиков в Карлсруэ? Каков был исторический фон эпохи, в которой жил и творил Менделеев?
Преподаватель: Конгресс в Карлсруэ. Химия и ее руководящая атомистическая теория в это время находились в полосе жесткого кризиса. Дж.Дальтон, выдвинув в связи с обоснованной им атомной теорией понятие «атомного веса», не смог дать строго научного решения задачи определения атомных весов. Гипотеза А.Авогадро, представляющая дальнейший шаг атомистики и дальнейшее необходимое звено в ее развитии, пребывала в забвении. В результате таблицы атомных весов, составленные разными авторами, в отношении многих элементов не сходились друг с другом. Авторы принимали различные химические формулы для одного и того же вещества.
Для разрешения этих разногласий по существу и собрались химики всего мира на конгрессе в Карлсруэ. Борьба была ожесточенной, но сторонники атомно-молекулярного учения, возглавляемые молодым итальянским химиком С.Канниццаро, одержали в ней блестящую победу. Бесспорный метод определения атомных весов был найден и утвержден.
Менделеев писал в Россию восторженные письма о конгрессе, а вспоминая о нем впоследствии, так характеризовал его значение для химии:
Чтец: «В 50-х годах одни принимали атомный вес кислорода 8, другие 16, если атомный вес водорода 1. Вода для первых была НО, перекись водорода НО2, для вторых, как ныне, вода Н2О, перекись водорода Н2О2 или НО. Смута, сбивчивость господствовали. Присутствовав на конгрессе в Карлсруэ, где химики всего света собирались для того, чтобы достичь соглашения, единообразия, я хорошо помню, как велико было разногласие, как с величайшим достоинством охранялось корифеями науки условное соглашение и как тогда последователи Жерара, во главе которых встал итальянский профессор, горячо проводили следствия закона Авогадро. При господстве научной свободы (без нее наука не двигалась бы вперед, окаменела бы, как в средние века) и при одновременной необходимости научного консерватизма (без него корни прошлого изучения не могли бы давать новых плодов) условное соглашение не было достигнуто и не должно быть достигаемо, а вместо того истина в виде закона Авогадро-Жерара при посредстве конгресса получила более широкое распространение и скоро затем покорила все умы. Тогда сами собой укрепились новые, так называемые жераровские веса атомов, и уже с 80-х годов они вошли во всеобщее употребление».
Преподаватель: Уже во времена Дальтона было известно, что между химическими элементами существуют не только различия (использованные аналитической химией, основу которой положил Р.Бойль), но и сходства, вследствие которых оказалось возможным сгруппировать элементы в «естественные семейства».
Учащийся 7: Так, исстари была известна сера; в конце XVIII в. был открыт теллур - элемент, имеющий много общего с серой. В начале же XIX в. великий шведский химик Й.Я.Берцелиус, который сыграл очень большую роль в утверждении атомистической теории, был приглашен для консультации на один из сернокислотных заводов в Швеции. Его внимание было обращено на красный ил, осаждающийся в газоочистительных камерах. Исследуя этот ил, Берцелиус, по первому впечатлению принял его за особую разновидность серы. Действительно, ил горел таким же пламенем, так же энергично соединялся с металлами; при действии воды или кислот на эти соединения выделялся газ, даже по запаху не отличимый от сероводорода. Но Берцелиус был достаточно опытным химиком, чтобы недолго оставаться в заблуждении. Все-таки красный ил оказался не серой. Тогда ученый принял его за теллур, но, в конце концов, он убедился, что имеет дело с новым элементом, который удивительным образом по своим свойствам является чем-то средним между серой и теллуром, и назвал его селеном. В самом названии нового элемента (селен в переводе с греческого означает лунный) Берцелиус отметил большое сходство селена с теллуром (от лат. tellus ~ Земля): подобно тому, как Луна является ближайшим небесным телом по отношению к Земле, селен - ближайший по свойствам химический элемент по отношению к теллуру.
Преподаватель: Тотчас после того, как Дальтон опубликовал свою таблицу атомных весов, начались поиски связи между химическим количеством, т.е. количественной характеристикой химического элемента - его атомным весом, и химическим качеством, т.е. всей совокупностью химических свойств элемента.
Учащийся 8: Эти попытки сразу увенчались блестящим успехом. И.Деберейнер, немецкий химик, установил свой знаменитый «закон триад», согласно которому в каждой тройке («триаде») сходных между собой элементов элемент, занимающий промежуточное положение по своим химическим свойствам, обладает и средним атомным весом. Так, в триаде Берцелиуса селен имеет атомный вес, равный 79. что как раз почти составляет среднее арифметическое между атомными весами крайних членов триады - серы и теллура:
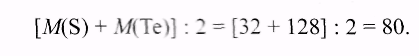
Учащийся 9: Менделеев вновь в России. Блестящая защита докторской диссертации «О соединении спирта с водой» в 1865 г. дала Менделееву профессорское звание. Эта диссертация - результат необычайно кропотливой работы, главным образом состоявшей в приготовлении смесей спирта и воды в различных точно отмеренных весовых пропорциях и в тщательном измерении удельных весов этих растворов. По удельным весам определялась крепость спиртовых растворов, а спирт Россия экспортировала. Поэтому работа имела большое практическое значение, т.к. таблицы Менделеева отличались исключительной точностью.
Учащийся 10: Но характерная особенность - стиль менделеевских работ - заключалась в тесном сплетении практических задач с теоретическими. В данном случае спиртовые растворы заинтересовали Менделеева с теоретической точки зрения, потому что через них он надеялся выяснить таинственную природу растворов вообще. Начиная с этой работы, Менделеев стал одним из главных защитников так называемой химической теории растворов, связывающей растворение с образованием химических соединении между растворяемым веществом и растворителем.
Учащийся 11: В университете лекции молодого профессора пользовались исключительным успехом. Аудитория всегда была набита битком; рядом со студентами-химиками сидели и правоведы, и математики. Тему каждой лекции Менделеев развивал чрезвычайно широко. Он увязывал в единый крепкий узел теорию с практикой, достигнутое с ожидаемым, привлекал множество сведений из смежных с химией отраслей знания, и очарованный слушатель уносил с собой представление о грандиозной борьбе человека с природой, о высокой роли науки в усовершенствовании жизни человеческого общества.
Преподаватель: Жизнь Менделеева - неустанный труд. Лекции и работа в лаборатории заполняли его день. Когда же наступала ночь, свет не гас в рабочем кабинете молодого ученого. В ночной тиши витали творческие мысли, оформлялись новые замыслы, создавался самый замечательный из учебников -«Основы химии», настойчиво разведывались пути к самому важному открытию, увенчавшему мировой славой русского химика, - периодическому закону. Это открытие было сделано 17 февраля (1 марта) 1869 г., т.е. на 35-м году жизни ученого.
Учащийся 12: Ход мыслей Менделеева был примерно таков. С одной стороны, у элементов есть точно измеримое, никакому сомнению после конгресса в Карлсруэ не подлежащее то свойство, которое выражено в весе их атома. С другой стороны, у элементов есть также химическая индивидуальность. Она выражена в разных формах химических соединений, в основности или кислотности окислов, в кристаллических формах и других признаках, частью точно измеримых, частью же таких, которые еще не поддаются выражению мерой и числом. Но разве по смыслу всех точных знаний о природе (здесь перед мысленным взором Менделеева воскресал столь обожаемый им еще в детстве образ Ньютона) не вес (масса) тела есть именно то свойство, от которого должны находиться в зависимости все прочие свойства? Не в атомных ли весах следует поэтому искать причину сходств, различий элементов, их деления на естественные семейства?
Преподаватель: Как уже упоминалось, этот путь к познанию вещества был отчасти испробован; но никто из предшественников Менделеева не пошел дальше предчувствий того великого закона, открытие которого выпало на его долю. Сам Менделеев изложил это открытие (в знаменитых «Основах химии») таким образом:
Чтец: «Невольно зарождается мысль о том, что между массой и химическими особенностями элементов необходимо должна быть связь. Искать же что-либо - хотя бы грибы или какую-либо зависимость нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы, с их атомными весами и характерными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса».
Преподаватель: Если забыть обо всем, что предшествовало раскладыванию карточек, начиная с бессонных ночей в педагогическом институте за работой об изоморфизме, то что могут извлечь для себя отсюда наши будущие Менделеевы? Незачем корпеть над книгами, проводить время в лабораториях, если ты гений; идея придет в свое время сама собой. Тогда посидел, повычислял, почертил - и великое открытие готово. На самом деле, раскладывание карточек - лишь заключительный этап длительной напряженной работы.
Когда шахматист напряжением ума, искусными маневрами доводит партию до безнадежного положения для противника, - сделать мат уже легко, - матовый ход может увидеть даже малоопытный игрок.
Учащийся 13: Однако не следует думать, что во времена Менделеева легко было сделать это открытие, даже подготовив его в результате упорных и длительных поисков. Дело в том, что из 112 ныне известных элементов в то время известно было чуть более 60; атомные веса многих из них из-за того, что идеи, утвердившиеся на конгрессе в Карлсруэ, еще не успели дать своих плодов, были определены неправильно.
Бериллию, который считался трехвалентным элементом, приписывался атомный вес 13,5, вычисленный по известной формуле:
атомный вес = эквивалент • валентность,
4,5 • 3 = 13,5.
Скандий, ныне располагающийся между кальцием и титаном, вообще не был известен.
Учащийся 14: И только из-за того, что атомный вес одного-единственного элемента был установлен неправильно, все нарушалось. Действительно, если поместить бериллий, согласно его принятому атомному весу, между углеродом и азотом, бор окажется над магнием, с которым он не имеет ничего общего, а углерод над алюминием; в ряду лития непосредственно после него - самого ярко выраженного металла - ляжет карточка неметалла бора; за ним последует еще более резко выраженный неметалл углерод, а непосредственно за ним в продолжающийся и далее ряд неметаллов ни с того ни с сего вклинится металл бериллий. Точно так же из-за неизвестности элемента, расположенного между Са и Ti, карточка титана попадет под карточку алюминия, с которым титан не имеет ничего общего по форме образуемых им соединений. Но Менделеев «откапывает» работу русского химика И.В.Авдеева, который утверждает, что соединения бериллия сходны с соединениями магния, поэтому бериллий подобно магнию должен быть признан двухвалентным элементом, а его атомный вес равным 4,5 • 2 = 9. Менделеев соответственно этому исправляет карточку бериллия, и все приходит на этом участке системы в порядок. Для того же, чтобы привести в соответствие ряд, начинающийся калием, Менделеев оставляет между кальцием и титаном пустое место еще не открытого элемента.
Учащийся 15: Первое опубликование периодической таблицы Менделеева не обратило на себя никакого внимания; то же самое ведь было и с его предшественниками. Но, продолжая в течение двух лет размышлять над элементами, не находящими себе, подобно бериллию, места в периодической таблице, и над пустующими клетками, Менделеев все более убеждался в необходимости исправить атомные веса первых и все более явственно представлял химический облик элементов, для размещения которых ему пришлось оставить пустые клетки в таблице. В результате этих размышлений в 1871 г. появилась его новая статья, представляющая собой высший взлет, кульминационную точку его гения. Наиболее важную часть этой работы составляли две главы: одна - посвященная предсказанию свойств еще не открытых элементов, и другая - содержащая перечень элементов, атомные веса которых определены ошибочно, здесь же приводились их предполагаемые истинные атомные веса.
Учащийся 16: Новая статья Менделеева обратила на себя столь же мало внимания, как и предыдущие его публикации, но спустя короткое время произошло замечательное событие. Молодой французский ученый-спектроскопист Лекок де Буабодран вручил секретарю Парижской академии наук закрытый конверт с просьбой сохранить его до ближайшей сессии академии. На сессии Буабодран выступил с докладом. Он полностью подтвердил содержавшиеся в закрытом конверте утверждения. Путем спектроскопического исследования цинковой обманки с Пиренейских гор удостоверено наличие в ней нового металла, который в небольшом количестве удалось выделить уже в свободном виде. Этот элемент образует квасцы; удельный вес нового металла такой-то, и т.д.
Учащийся 17: Менделеев прочитал отчет о докладе Буабодрана в «Известиях Парижской академии наук» и тотчас убедился, что новый элемент, названный Буабодраном галлием, есть не что иное, как предсказанный им самим экаалюминий. Сходилось все, кроме удельного веса. Но Буабодран, извещенный Менделеевым, повторил определение удельного веса галлия, и, оказалось, Менделеев прав! Первое определение было ошибочным из-за примеси натрия, с помощью которого производилось восстановление галлия.
Преподаватель: Это было лишь началом триумфа периодического закона. Другие два предсказанных Менделеевым элемента (германий и скандий) заставили себя ждать дольше, но, в конце концов, также были открыты, и совпадение их свойств с предположениями ученого оказалось еще более поразительным. Одновременно подтверждались одно за другим исправления атомных весов уже известных элементов, сделанные Менделеевым.
Теория проверяется практикой. Теория утверждается через предсказания, т.к. знать - значит предвидеть.
Периодический закон блестяще выдержал это испытание, и только самые закоренелые скептики пытались некоторое время оспаривать его справедливость.
Менделеев и практика. В период 1869-1871 гг. выходит в свет знаменитый учебник Менделеева
Учащийся 18: «Основы химии» - первое изложение этой науки на основе периодического закона. «Эти основы, - писал впоследствии Менделеев, - любимое дитя мое. В них мой образ, мой опыт педагога и мои задушевные научные мысли». Эта книга потом устареет как учебник, но навсегда останется школой научного творчества. И поныне, принимаясь за разработку того или иного научного или научно-технического вопроса, связанного с химией, специалисты перелистывают «Основы», выясняя, что думал и писал по этому вопросу Менделеев.
«Основы химии» были переведены в Англии, Франции, Германии и США; они сделались прообразом всех последующих учебников химии как для высшей, так и для средней школы, на каком бы языке ни писались. Особенно ценно в «Основах химии» то, что теория в них неразрывно сочетается с практикой.
Преподаватель: Начиная с 1872 г. Менделеев, возвратившись к своим юношеским идеям, провел ряд работ по исследованию растворов и сжимаемости газов. Средства на работы по газам он получил от заинтересованного в них Артиллерийского ведомства. В связи с газами научный интерес ученого устремился к проблемам метеорологии и воздухоплавания. В работах этого периода особенно ярко выражена связь научной деятельности Менделеева с интересами молодой тогда капиталистической промышленности России.
Учащийся 19: Отвлекаясь в сторону, он ни на минуту не забывал химии. Начиная с первого посещения Баку в 1863 г., он уделял особенное внимание русской нефти. Сочетая, как всегда, теорию с практикой, он создал химическую теорию происхождения нефти (действием воды на содержащиеся в недрах земли карбиды металлов), а также прилагал все усилия, чтобы научить отечественных нетепромышленников рационально использовать этот дар природы путем переработки нефти, вместо того чтобы топить сырой нефтью паровые котлы. «Топить можно ассигнациями», - негодующе восклицает он. И Менделеев был прав, когда впоследствии писал:
Чтец: «У меня на глазах развилось наше нефтяное дело, и сам я в его развитии занимал такую же роль указательного пальца, какую желал бы занять в нашем каменноугольном деле». В 1888 г. он принялся за изучение Донецкого каменноугольного бассейна - «будущей силы, покоящейся на берегах Донца», - и предложил ряд мер для его рационального использования. «В той постоянной экономической войне, - писал он, -которую ныне ведут все страны и которая всех затрагивает, роль каменного угля громадна потому именно, что вся современная промышленность обосновалась на угле».
Преподаватель: Опала. Имя молодого русского ученого прогремело по всему миру. Перед Менделеевым раскрылись двери старейших академий Старого и Нового Света. И только в русской Академии наук кандидатура Менделеева, выдвинутая в 1880 г. крупнейшими русскими учеными, провалилась. Негодование передовой научной общественности было велико.
Чтец:1 «Давай бог всякому заслуженному ученому так "провалиться", - писалось в одной либеральной газете, - как "провалился" Менделеев. Вот уже две недели, как мы присутствуем при величественном и красноречивом протесте ученых корпораций, общества и печати...»
Чтец:2 «Уважаемый и первоклассный ученый, - писалось в другой газете, - которому по праву принадлежит академическое кресло, произвольно лишен следующего ему почета мелкою, злопамятною кумовскою кликою, насидевшей себе теплые местечки путем еле заметного научного кропательства».
Преподаватель: Но тщетны были протесты: русским академиком Менделеев так и не стал. Это не помешало ему с прежним успехом вести свои курсы и научную работу.
Но вот наступили тяжелые для студенчества 80-е годы. Свыше велено было подтянуть университеты, эти рассадники «свободомыслия». Молодежь сопротивлялась наступлению реакции; бурные сходки следовали одна за другой, и на одной из них петербургским студенчеством было принято специальное обращение к министру просвещения. Но кто же вручит его? Выбор пал на любимого учителя, Менделеева.
Успокоив, как мог, студентов, седовласый ученый на другой день сам поехал к министру. Однако для министра Менделеев не был ни великим ученым, ни популярнейшим среди студентов педагогом; он был только действительным статским советником, преступавшим свои права. Ответ министра был таков, что Менделееву ничего не оставалось, как покинуть университет, выйти в отставку. Произошло это в 1890 г.
И вот в последний раз поднялся он на кафедру и окинул долгим взором притихшую молодежь, переполнившую химическую аудиторию, и его прощальная лекция превратилась в торжественное завещание учителя ученикам.
«Марганец...» - начал Менделеев; он знал, что от него ждут не химической лекции; что именно ждут от него, он читал в испытующих взорах, устремленных на него со всех сторон, но он твердо продолжил очередную лекцию, заканчивая ее так: «...и надобно иметь фонарь науки, чтобы осветить эти глубины и увидеть в темноте. И если этот фонарь знания внести в Россию, то вы сделаете в самом деле то, чего от вас ожидает Россия».
Учащийся 20: Уход из университета сильно потряс Менделеева, но его кипучая натура не могла долго бездействовать. Вместе с новым местом службы -Палатой мер и весов, куда он поступил в 1893 г. и где остался до самой смерти, - появились у него новые интересы. Искусство точных измерений, усвоенное и разработанное им для решения научных проблем, он теперь применил для торговли и промышленности, для экономического развития своей родины.
Ученый возродился. Это был прежний Менделеев - человек с несокрушимой энергией и поразительной работоспособностью.
Учащийся 21: Еще в период между уходом из университета и поступлением в Палату мер и весов Менделеев сделал весьма крупный вклад в дело обороны страны своим изобретением бездымного пороха для перевооружающейся по западноевропейскому образцу русской армии. В этой выполненной в 1891 г. по поручению военного и морского министерства работе ему помогла его же собственная теория растворов.
Из работ, выполненных в Палате, которую он превратил из простого хранилища эталонов единиц меры и веса в кипучую научно-исследовательскую лабораторию, наиболее важны работы о законах колебания весов.
Учащийся 22: Но Менделеев и здесь, на своем новом поприще, не забывал о химии, основную роль которой усматривал в обращении природных минеральных богатств на службу человеческому обществу. Результатом его поездки в 1899 г. на уральские заводы явилась обширная монография о состоянии и мерах к развитию уральской железной промышленности - последний крупный труд Менделеева.
Если подвести общий итог работам Менделеева, то окажется, что максимум их (110 работ) падает на период 1872-1877 гг. Общее же число работ - 431. Из этого числа приходится на долю: химических - 40, физико-химических - 106, технических - 99, физических - 99, экономических -36, геодезических - 22, прочих - 29.
Ведущий: Такова была широта интересов, диапазон деятельности этой исключительной натуры.
Предвидения Менделеева. Весь мир знает и чтит Менделеева именно как творца периодического закона, и лишь специалистам известно, как много других полезных и важных работ вышло из-под его пера; но еще больше, пожалуй, было у него проектов неосуществленных. Его мысль устремлялась к высоким слоям атмосферы, не расставаясь при этом с «земными целями». Для того чтобы достигнуть полной победы над воздухом, необходимо было изучить его. В результате родился труд о сопротивлении воздуха, который долго служил основным руководством для всех, кто занимается кораблестроением, воздухоплаванием и баллистикой. Доход от продажи одной из своих книг он отдал на устройство аэростата для изучения верхних слоев атмосферы.
Чтец:1 «Хочется получить возможность, - писал он при этом, - побывать выше облаков, внести туда измерительные приборы. Меня тянет теперь в эти места». И Менделеев осуществил свою мечту.
Ведущий: В 1887 г. он один на аэростате поднялся выше облаков наблюдать солнечное затмение, а приземлился далеко в другой губернии. Суеверные крестьяне посчитали, что к ним спустился на землю сам Бог.
На закате жизни с такой же неудержимой силой притягивали его загроможденные льдами просторы северных морей.
Чтец:2 «Лучше всего, - писал он, - одним из первых планов поставить завоевание Ледовитого океана. Если победили твердыни гор, надо льды побороть, а у нас их больше, чем у кого-нибудь. А около льдов немало и золота и всякого иного добра - своя Америка».
Преподаватель: Но еще больше влекли Менделеева к себе недра земли таящимися в них неисчерпаемыми богатствами, осветить которые «фонарем науки» завещал он своим ученикам. Он утверждал, что наступит время, когда не будут затрачивать труд на извлечение бедных углей на поверхность земли, а прямо в ее недрах превращать их в генераторный газ.
9


