- Преподавателю
- Химия
- Конспект урока на тему Метан. Состав. Строение молекулы. Свойства. Распространение в природе. Применение
Конспект урока на тему Метан. Состав. Строение молекулы. Свойства. Распространение в природе. Применение
| Раздел | Химия |
| Класс | - |
| Тип | Конспекты |
| Автор | Харичева Л.Н. |
| Дата | 14.01.2015 |
| Формат | docx |
| Изображения | Есть |
Тема:
Метан. Состав, строение молекулы. Свойства.
Распространение в природе. Применение.
Цель урока:
-
Изучить строение молекулы метана. Описать физические и химические свойства метана. Познакомиться с нахождением метана в природе и его применением.
-
Развивать практические умения изготовления модели молекулы метана.
-
Формировать аналитическое мышление, умение фантазировать, сравнивать и обобщать, логически излагать свои мысли.
-
Воспитывать дисциплинированность, положительное отношение к химии как науке.
Оборудование: шаростержневая модель молекулы метана, компьютер, проектор, экран, презентация в программе Power Point.
Методы обучения:
-
Словесные (беседа, объяснение, рассказ).
-
Наглядные (компьютерная презентация, шаростержневая модель метана).
-
Практические (решение задач и уравнений реакций).
-
Моделирование (изготовление модели молекулы).
Тип урока: изучение нового материала.
Структура урока:
-
Организационный момент-------------------------------------------------------------2мин
-
Мотивационный момент------------------------------------------------------------- 1мин
-
Проверка домашнего задания--------------------------------------------------------5мин
-
Изучение новой темы-----------------------------------------------------------------20мин
-
Закрепление---------------------------------------------------------------------------12мин
-
Домашнее задание---------------------------------------------------------------------2мин
-
Итог урока-------------------------------------------------------------------------------3мин
Ход урока
-
Организационный момент
Приветствие учащихся, организация внимания
-
Мотивационный момент.
Ребята! Сегодня мы с вами совершим путешествие в удивительную страну Туркменистан! Эта страна находится в Средней Азии. Граничит с Афганистаном и Ираном на юге, Казахстаном и Узбекистаном на севере, омывается внутренним Каспийским морем на западе. Мы ощутим горячее жерло искусственного кратера с пугающим названием «Врата ада», который находится недалеко от городка Дарваза в пустыне Каракум
Смотреть слайд 1
На марсоходе Curiosity отправимся в космический полёт на Марс.
Смотреть слайд 2
Пройдёмся по топким термокарстовым озёрам Западной Сибири. Спустимся с шахтёрами на глубину до нескольких сотен метров.
Смотреть слайд 3
-
Проверка домашнего задания:
Но, сначала, давайте проверим домашнее задание, а потом совершим экскурсии в чудесный мир природы. На прошлом уроке мы с вами сформировали представление о составе и строении органических соединений.
-
Дайте сравнительную характеристику органическим и неорганическим веществам.
Один ученик с места дает сравнительную характеристику органическим и неорганическим веществам. Используя слайд № 4
Смотреть слайд 4
№
Признаки
Органические вещества
Неорганические вещества
1.
Количество
веществ в природе
Более 20 миллионов,
с каждым годом пополняется 200-300 тысячами новых.
Не более 200 тысяч
2.
Качественный состав
Несколько химических элементов: Карбон, Гидроген, Нитроген, Оксиген, Сульфур, Феррум и некоторые другие
Все химические элементы
3.
Количественный состав
От одного атома Карбона до нескольких тысяч атомов в одной молекуле
Разнообразное количество атомов химических элементов
4.
Валентность элементов
Карбон IV-х валентный
Величина переменная
5.
Виды химических связей
Ковалентная, иногда ионная
Ионная, ковалентная, металлическая
6.
Кристаллические решётки
молекулярные
Атомные, ионные, молекулярные
7.
Физические свойства
Легкоплавкие, частично обладают запахом, преимущественно нерастворимы в воде
Тугоплавкие, устойчивы к нагреванию, растворяются в воде
2. Как вы считаете, актуальны ли в наше время слова выдающегося русского учёного Михаила Васильевича Ломоносова, сказанные ещё в середине XVIII века, в период становления науки химии?
«Широко распростирает химия руки свои в дела человеческие… Куда ни посмотрим, куда ни оглянемся, везде обращаются перед очами нашими успехи её прилежания...»
Смотреть слайд 5
Учащиеся высказывают свои предположения.
-
Изучение новой темы
-
Рассказ учителя с элементами беседы:
А сейчас совершим с вами путешествие в удивительный уголок нашей природы в Туркменистан. Мысленно пристегнём ремни, наденем скафандры и окажемся на планете Марс. Совершим экспедицию по карстовым озёрам Западной Сибири. И вместе с шахтёрами опустимся в недра нашей Земли. Внимание! Поехали!!!
Смотреть слайд 6 (видеоролик)
Ребята! Мы не просто так с вами путешествовали. О каком веществе рассказывали все участники экспедиции?
Правильно. О метане.
Запишите тему урока. Смотреть слайд 7
Метан. Состав, строение молекулы. Свойства. Распространение в природе. Применение.
И давайте определим цели, которые необходимо достигнуть на этом уроке.
Смотреть слайд 8
Просмотрев внимательно ролик, что вы можете сказать о составе метана?
Правильно, простейшим органическим соединением, в составе которого только один атом углерода и четыре атома водорода, является метан, его молекулярная формула СН4.
Для понимания электронного строения молекулы метана вспомним электронное строение атома Карбона.
У доски учащийся записывает электронную формулу атома Карбона:
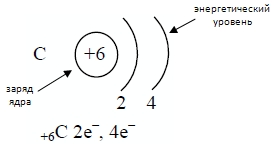
6С 1s22s22p2
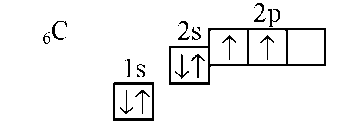
(Далее объяснение учителя): В основном состоянии на внешнем электронном слое атома размещаются 4 электрона: два s- и два p-электрона, а одна р-орбиталь остаётся свободной. При образовании соединения атом Карбона переходит в возбуждённое состояние, а один s-электрон перемещается на свободную р-орбиталь. Таким образом, в атоме Карбона во внешнем слое содержатся четыре неспаренных электрона, благодаря которым образуются четыре связи с другими атомами, то есть углерод проявляет валентность четыре.
Смотреть слайд 9
Атомы Гидрогена имеют по одному электрону и являются одновалентными. Отдавая четыре электрона, атом Карбона образует четыре ковалентных связи с четырьмя атомами Гидрогена. Обозначив валентные электроны точками, получим электронную формулу метана: 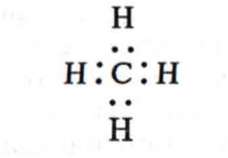
Заменим точки, обозначающие электронные пары, черточками (связями) - получаем структурную формулу метана: 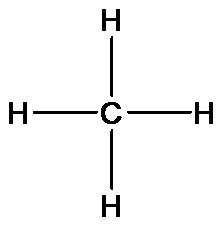
Структурные формулы являются лишь схематическим изображением, реальное же строение молекулы метана имеет форму правильной тригональной пирамиды (тетраэдра). Если атом углерода вписать в эту геометрическую фигуру, то четыре валентных связи будут направлены под углом 109,5º к вершинам тетраэдра, где размещаются атомы водорода.
Смотреть слайд 10
-
Лабораторный опыт: Изготовление моделей молекулы метана.
Смотреть слайд 11
Инструкция.
-
Объединитесь в группы по 4-ре человека.
-
Вам понадобиться пластилин двух цветов.
-
Слепите один шарик большего диаметра и четыре шарика меньшего диаметра.
-
К шарику большего диаметра присоедини, используя спички (химические связи), шарики меньшего диаметра.
-
Соблюдай тетраэдрическое направление химических связей, то есть под углом 109,5º одна к другой.
-
Сделайте вывод о пространственном строении молекулы метана
Группы презентуют свои модели и делают вывод.
3.Самостоятельная работа с учебником.
(Учитель) Путешествуя по карстовым озёрам, совершая полёты на другие планеты, погружаясь с шахтёрами в недра Земли или ощущая на себе горящее пламя жерла кратера, о каких физических свойствах метана вы можете рассказать?
Можно в учебнике рассмотреть рисунок 77. На стр.129.
Учащиеся самостоятельно делают выводы о физических свойствах метана и записывают в тетрадь.
Смотреть слайд 12
Ребята! Метан - газ без запаха, взрывоопасен при несоблюдении техники безопасности. Взрыв может произойти даже от искры, если концентрация метана достигает критической. Поэтому стали добавлять в газ добавки с резким запахом.
Запах газа - это запах специальных добавок.
Цель добавок: ОБЕСПЕЧИТЬ БЕЗОПАСНОСТЬ ЖИЗНИ ЛЮДЕЙ.
Запомните!!!! С природным газом надо обращаться очень осторожно!
Смотреть слайд 13
Фронтальная беседа.
(Учитель.) Что вы можете сказать о распространении метана в природе?
Используя материалы учебника (стр.129-130, данные с видеоролика) учащиеся делают выводы.
Распространение метана в природе:
-
Метан образуется в недрах Земли (природный газ)
-
В процессе гниения растительных остатков без доступа воздуха в озёрах, в болотах (болотный газ)
-
В угольных шахтах (рудничный газ)
-
Метан содержатся в атмосфере планет Солнечной системы: на Юпитере, Сатурне и его спутнике Титане, Уране, Нептуне, на Марсе. На Титане существуют (полярные) озёра метана и метановые дожди.
-
Кроме того, метан найден в хвосте кометы Хиякутаке и в метеоритах.
Учащиеся с места делают сообщения и сравнивают свои данные с текстом слайда № 14
Смотреть слайд 14
Химические свойства метана (рассказ учителя у доски с элементами беседы, учащиеся записывают в тетради)
-
Реакции горения - это одно из важнейших химических свойств метана, которое нам известно из повседневной жизни. Кроме продуктов окисления выделяется большое количество теплоты. (Рис.78. стр.130)
СН4 + 2О2 → СО2 + 2Н2О; ∆Н= ─ 890 кДж/моль
Эта реакция полного окисления. Является экзотермической.
При недостатке кислорода метан окисляется не полностью - протекает реакция частичного окисления с образованием углерода (в виде сажи) и оксида углерода(II). Это очень токсичное вещество без запаха и цвета. При неполном окислении метана в бытовых газовых приборах его пламя приобретает жёлтую окраску, поскольку частицы углерода раскаляются.
-
Реакция разложения. При нагревании метана до высокой температуры (свыше1000ºС) без доступа кислорода протекает реакция с образованием углерода (сажи) и водорода:
СН4 → С + 2Н2
-
Реакция замещения. Метан вступает в реакцию с хлором при освещении. Протекает реакция хлорирования метана.
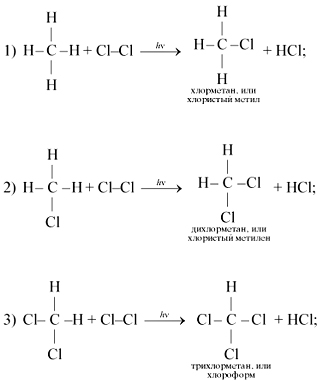
4-тую стадию учащиеся записывают самостоятельно
-
Закрепление
Смотреть слайд 15
Класс разбивается на три группы.
1-я группа «Энергетики»
Решают задачу:
Природный газ содержит 5% (по объёму) негорючих примесей. Сколько необходимо сжечь природного газа (н.у.) для получения 1008 кДж теплоты, чтобы закипятить воду в
3-х литровом чайнике?
2-я группа «Химики»
Записать уравнения реакций замещения, используя молекулярные формулы.
3-я группа «Промышленники»
Используя § 20 учебника и интернет-источники подготовить сообщения о сферах применения метана и его производных.
Презентация своих заданий. Пока представители 1-ой и 2-ой групп записывают решения у доски, ученик 3-ей группы рассказывает о сферах применения метана.
Смотреть слайды 16,17,18
-
Домашнее заданее
Изучить § 20. № 6,7 - устно, №10 - письменно
Подготовить сообщение об использовании биогаза
-
Итог урока
Благодаря виртуальному путешествию по чудесному миру природы мы познакомились с удивительным веществом МЕТАНОМ, изучили его свойства, состав, строение.
Выяснили, что метан является не только дешёвым топливом, а широко применяются и продукты химических превращений метана.
Всем огромное спасибо за урок!


