- Преподавателю
- Физика
- Зачет № 4 по теме «Атомная физика. Физика атомного ядра (бинарный урок)
Зачет № 4 по теме «Атомная физика. Физика атомного ядра (бинарный урок)
| Раздел | Физика |
| Класс | - |
| Тип | Конспекты |
| Автор | Подсосонная О.В. |
| Дата | 31.01.2016 |
| Формат | docx |
| Изображения | Есть |





















 Приложение 2.
Приложение 2.
Тема урока « Зачет № 4 по теме « Атомная физика. Физика атомного ядра».
Тип урока: интегрированный урок; урок повторения, систематизации и обобщения знаний, закрепления умений.
Время урока: 1 час 30 минут.
Форма данного типа урока:
-
повторительно-обобщающий урок;
-
урок-совершенствование.
Структура урока строится на сочетании этапов:
-
организационного,
-
постановки цели,
-
оперирования знаниями и способами деятельности в стандартных и нестандартных ситуациях,
-
рефлексия,
-
формулирования выводов.
Цель: более глубокое усвоение знаний, высокий уровень обобщения, систематизации по теме «Атомная физика. Физика атомного ядра».
Задачи:
-
образовательные: выявить качество и уровень овладения знаниями и умениями, полученными на предыдущих уроках по теме: обобщить материал как систему знаний.
-
воспитательные: воспитывать общую культуру, эстетическое восприятие окружающего; создать условия для реальной самооценки учащихся, реализации его как личности.
-
развивающие: развивать пространственное мышление, умение классифицировать, выявлять связи, формулировать выводы; развивать коммуникативные навыки при работе в группах, развивать познавательный интерес; развивать умение объяснять особенности:, закономерности:, анализировать:, сопоставлять:, сравнивать: и т.д.
Оборудование: проектор, ноутбук, экран; таблица периодической системы химических элементов Д.И.Менделеева; раздаточный материал, презентация по данной теме; физическая модель «Планетарная модель атома».
Эпиграф урока: «Отыщи всему начало и ты многое поймёшь».
(Козьма Прутков)
-
Организационный момент (число, тема).
-
Постановка цели.
-
Основная часть.
Водное слово учителя: «Всем известно, что на одну и ту же проблему или какой-либо факт, можно взглянуть с различных точек зрения, что вы порой и делаете, даже не подозревая об этом, на уроках химии, физики, биология, географии. Сегодня мы решили объединить уроки химии и физики, чтобы раскрыть строение одной очень маленькой частички - атома».
-
Как вы можете прокомментировать слова известного физика Нильса Бора: «Когда мы говорим об атомах, язык можно использовать лишь поэтический»?
-
Первое задание. ( Слайд № 1).
Учащиеся работают в группах ( по рядам), отвечают по очереди на вопросы:
-
Из каких элементарных частиц состоит атом?
-
Как определить заряд атома?
-
Каков заряд атома?
-
Как определить число нейтронов?
-
Что такое изотопы?
-
Определите состав атома хлора Cl.
-
Определите состав атома магния Mg.
-
Как располагаются электроны вокруг ядра?
-
Второе задание. (Слайд № 2).
Учащимся каждому индивидуально предлагается выполнить задание в раздаточном материале, провести самопроверку и самооценку.
Задание: «Привести в соответствие обозначение физической величины и ее название»:
Название физической величины
Ее обозначение
Масса ядра атома
Mя
Протон
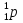
Постоянная Планка
h
Число электронов
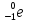
Массовое число
A
Длина волны
λ
Нейтрон
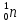
Масса электрона
me
Масса протона
mn
α-частица
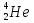
β-частица
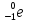
Число протонов (электронов)
Z
Энергия связи
Есв
Число нейтронов
N
Самопроверка: «2 балла» - все верно или 1 ошибка!
1 балл- 2- 3 ошибки!
0 баллов - более 4 ошибок!»
-
Фронтальный опрос (Слайд № 3)
Историческая справка « Развитие представлений о строении атома».
-
Модель Дж. Томсона «пудинг с изюмом»
-
Планетарная модель строения атома Резерфорда.
-
Современная квантовая модель строения атома.
-
Третье задание (индивидуальная работа на раздаточном материале) .
Изобразите схему строения атомов элементов: Са, Мg, Ag, Fe.
ядро (+)
-
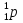 (Z) = ?
(Z) = ? -
(N)= ?
оболочка (-)
-
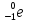 (
(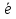 ) (Z) = ?
) (Z) = ?
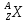
Решение:
-
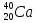
ядро (+)
-
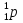 (Z) = 20
(Z) = 20 -
(N)= 40-20=20
оболочка (-)
-
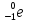 (
(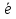 ) (Z) = 20
) (Z) = 20
-
Памятка для учащихся: «Строение всех атомов зашифровано в периодической системе химических элементов. 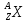 - элемент обозначается как и в химии, общепринятыми символами: заряд записывается в виде индекса внизу символа, а атомная масса - в виде индекса вверху символа. Порядковый номер химического элемента показывает электрический заряд ядра атома Z , этот заряд численно равен сумме протонов в ядре атома
- элемент обозначается как и в химии, общепринятыми символами: заряд записывается в виде индекса внизу символа, а атомная масса - в виде индекса вверху символа. Порядковый номер химического элемента показывает электрический заряд ядра атома Z , этот заряд численно равен сумме протонов в ядре атома 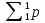 ; т.к. атом в целом электрически нейтральная частица, то суммарный положительный заряд атома равен суммарному отрицательному заряду, следовательно, равен числу электронов в оболочке атома
; т.к. атом в целом электрически нейтральная частица, то суммарный положительный заряд атома равен суммарному отрицательному заряду, следовательно, равен числу электронов в оболочке атома 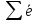 .
.
Z = 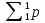 =
= 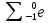 . Чтобы вычислить число нейтронов в ядре из атомной массы атома вычитаем заряд ядра: N = А- Z.
. Чтобы вычислить число нейтронов в ядре из атомной массы атома вычитаем заряд ядра: N = А- Z.
Самопроверка: «2 балла» - все верно!
1 балл- 1 ошибка!
0 баллов - более 2 ошибок!»
-
Решение задач. (Слайд 17-21)
-
Атомная масса изотопа неизвестного элемента равна 39. Число протонов в ядре на 3 меньше, чем нейтронов. Этот элемент имеет символ:
1) К 2) Са 3) Аr 4) Сl.
Дано: Решение
А= 39 А= Z + N
Z= N-3 А= N-3+N=2N- 3
Х-? 39= 2 N -3
42 = 2N
N= 21=> Z=А-N = 39-21 =18
По периодической таблице определяем химический элемент: Аr.
Ответ: Аr.
Самопроверка: «2 балла» - все верно!
1 балл- 1 ошибка!
0 баллов - более 2 ошибок!»
-
Работа по группам. Запишите химически уравнение ядерной реакции:
-
Уравнение реакции Резерфорда. В результате которой он бомбардировал азот α-частицами, при этом получались протон и ядра какого-то другого вещества ( первая группа)
-
При действии α-частицы на бериллий выделяются нейтроны и получается какой-то химический элемент.(вторая группа)
-
Решение:
Уравнение является правильным, если в правой и левой его части соблюдается равенство общего массового числа и равенство общего числа зарядов. Это правило почти полностью совпадает с правилом проверки правильности ионного уравнения.
5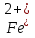 + Mn
+ Mn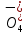 + 8
+ 8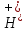 = 5
= 5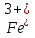 +
+ 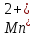 +4H2O
+4H2O
И так, запишем несколько уравнений ядерной реакции и прежде всего уравнение реакции Резерфорда.
-
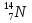 +
+ 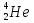 →
→ 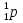 +
+ 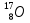
-
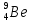 +
+ 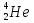 →
→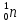 +
+ 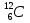
-
Долгое время алхимики пытались превратить в золото «несовершенные» металлы, в частности, в ртуть. Можно ли получить золото (Au) из ртути (Hg) физическим и химическим путем? Как?
Решение:
-
Превратить один элемент в другой химическим путем невозможно.
-
Тайна взаимного превращения элементов разгадана лишь в наше время - и это уже совсем иная, новая область науки физики - ядерные реакции.
Дифференцированная работа:
(зеленый уровень)
-
Запишите ядерную реакцию синтеза золота, облучая нейтронами изотоп ртути
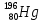 .
.
Решение:
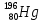 +
+ 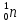 →
→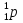 +
+ 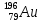
В определенных условиях этим способом можно получить за месяц 1,5г золота, переработав более 1000г природной ртути.
(красный уровень)
-
Запишите получение золота из ртути
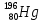 путем α- и β- распада.
путем α- и β- распада.
Решение:
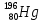 →
→ 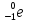 +
+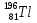
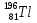 →
→ 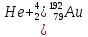
Но стоимость золота, полученного путем ядерных реакций, будет фантастически велика, так что о практическом значении этого способа не может быть и речи.
Самопроверка: «2 балла» - все верно! 1 балл- 1 ошибка! 0 баллов - более 2 ошибок!
-
Дифференцированная работа
(зеленый уровень)
-
Масса нейтрона 1,67 ·10-27кг, а скорость движения его 4 ·102м/с. Определить длину волны де Бройля.
Дано: Решение:
mn = 1,67 ·10-27кг λ = 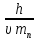 , где h = 6,63 ·
, где h = 6,63 ·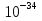 Дж·с
Дж·с
υ =4 ·102м/с λ = 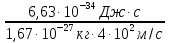 = 0,99·
= 0,99·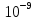 м
м
λ - ?
Ответ: λ= 0,99·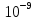 м
м
(красный уровень)
-
Подсчитайте энергию связи ядра гелия (mр = 1.00758 а.е.м., mn= 1,00898 а.е.м., Мя = 4,00274 а.е.м)
Дано: Решение:
mр = 1.00758 а.е.м. 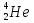 : Z= 2 N = 2
: Z= 2 N = 2
mn= 1,00898 а.е.м.
Мя = 4,00274 а.е.м. ∆ E = ∆mc2
Есв -? ∆m = Z mр + N mn - Мя
∆m = 0.03038а.е.м. = 0.03038а.е.м.·1,67·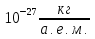 =
=
= 0,05·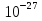 кг
кг
∆ E = 0,05·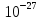 кг ·9·
кг ·9·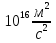 = 0,45·
= 0,45·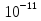 Дж
Дж
Ответ: ∆ E =0,45·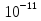 Дж
Дж
Самопроверка: «2 балла» - все верно! 1 балл- 1 ошибка!
0 баллов - более 2 ошибок!»
-
Проблема.
? Слово «атом» придумал очень давно более 2500 лет назад древнегреческий философ Демокрит. С греческого «атом» переводится как «неделимый». Так ли это?
Современное определение атома с точки зрения химии звучит так: «Атом - химически неделимая частица».
Проблемой расщепления атома занимается ядерная физика.
-
Вспомните механизм протекания цепной химической реакции:
CH4 + CL2 →CH3CL + HCL
? Что является основным условием для протекания такой цепной реакции?
( солнечная энергия)
? Что выделяется в результате данной реакции?
(кислота)
-
Вспомните механизм протекания цепной ядерной реакции:
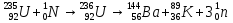
? Что необходимо для стационарного течения цепной реакции?
( коэффициент размножения нейтронов κ =1)
? Что образуется в результате реакции?
( образуются 2,3 нейтрона; выделяется огромная энергия).
-
Рефлексия:
Учащимся предлагается ответить коротко письменно на вопрос:
? Если бы не было открыто строение атома, то……………?
-
Подведение итогов:
-
Подсчет баллов учащимися:
10 - 9 баллов - «5»; 8-7 баллов- «4»; 6-5 баллов - «3»
менее 5 баллов - не отчаивайся, надо еще все повторить!
-
выставление и комментирование оценок обучающимся за урок,
-
благодарность активным обучающимся.
Приложение
«Зачет № 4 по теме « Атомная физика. Физика атомного ядра».
Рабочий лист
-
-
__ класс Ф.И. ученика_________________________________
-
-
Приведите в соответствие обозначение физической величины и ее название:
Название физической величины
Ее обозначение
Масса ядра атома
mn
Протон
me
Постоянная Планка
Z
Число электронов
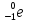
Массовое число
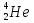
Длина волны
Есв
Нейтрон
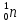
Масса электрона
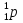
Масса протона
Mя
α-частица
A
β-частица
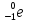
Число протонов (электронов)
N
Энергия связи
λ
Число нейтронов
h
«2 балла» - все верно! 1 балл- 1 ошибка! 0 баллов - более 2 ошибок!
-
Изобразите схему строения атомов элементов:
-
оболочка (-)
-
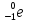 (
(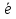 ) (Z) =
) (Z) =
ядро (+)
-
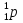 (Z) =
(Z) =
-
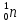 (N)=
(N)=
-
Памятка: «Строение всех атомов зашифровано в периодической системе химических элементов. 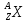 - элемент обозначается как и в химии, общепринятыми символами: заряд записывается в виде индекса внизу символа, а атомная масса - в виде индекса вверху символа. Порядковый номер химического элемента показывает электрический заряд ядра атома Z , этот заряд численно равен сумме протонов в ядре атома
- элемент обозначается как и в химии, общепринятыми символами: заряд записывается в виде индекса внизу символа, а атомная масса - в виде индекса вверху символа. Порядковый номер химического элемента показывает электрический заряд ядра атома Z , этот заряд численно равен сумме протонов в ядре атома 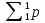 ; т.к. атом в целом электрически нейтральная частица, то суммарный положительный заряд атома равен суммарному отрицательному заряду, следовательно, равен числу электронов в оболочке атома
; т.к. атом в целом электрически нейтральная частица, то суммарный положительный заряд атома равен суммарному отрицательному заряду, следовательно, равен числу электронов в оболочке атома 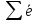 .
.
Z = 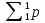 =
= 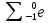 . Чтобы вычислить число нейтронов в ядре из атомной массы атома вычитаем заряд ядра: N = А- Z
. Чтобы вычислить число нейтронов в ядре из атомной массы атома вычитаем заряд ядра: N = А- Z
«2 балла» - все верно! 1 балл- 1 ошибка! 0 баллов - более 2 ошибок!»
-
Решение задач:
-
Атомная масса изотопа неизвестного элемента равна 39. Число протонов в ядре на 3 меньше, чем нейтронов. Этот элемент имеет символ:
1) К 2) Са 3) Аr 4) Сl. ( решите задачу в тетради)
«2 балла» - все верно! 1 балл- 1 ошибка! 0 баллов - более 2 ошибок!»
-
Запишите химически уравнение ядерной реакции:
-
Уравнение реакции Резерфорда. В результате которой он бомбардировал азот α-частицами, при этом получались протон и ядра какого-то другого вещества ( первая группа)
-
При действии α-частицы на бериллий выделяются нейтроны и получается какой-то химический элемент.(вторая группа)
_________________________________________________________________ «2 балла» - все верно! 1 балл- 1 ошибка! 0 баллов - более ошибок!»
Запишите ядерную реакцию
(зеленый уровень)
-
Запишите ядерную реакцию синтеза золота, облучая нейтронами изотоп ртути
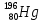 .
.
_____________________________________________________________
(красный уровень)
-
Запишите получение золота из ртути
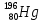 путем α- и β- распада.
путем α- и β- распада.
__________________________________________________________
__________________________________________________________
«2 балла» - все верно! 1 балл- 1 ошибка! 0 баллов - более 2 ошибок!»
-
Закончи предложение: «Если бы не было открыто строение атома, то
______________________________________________________________________________________________________________________________________________
Подсчитай свои баллы и оцени свою работу!
10 - 9 баллов - «5»; 8-7 баллов- «4»; 6-5 баллов - «3»;
менее 5 баллов - не отчаивайся, надо еще все повторить!
Оценка__________________


